a, Proton
b, neutron
c, electron
a) Hạt mang điện tích dương => Proton
b) Hạt được tìm thấy trong hạt nhân và không mang điện => Neutron
c) Hạt mang điện tích âm => Electron
a, Proton
b, neutron
c, electron
a) Hạt mang điện tích dương => Proton
b) Hạt được tìm thấy trong hạt nhân và không mang điện => Neutron
c) Hạt mang điện tích âm => Electron
Thông tin nào sau đây không đúng?
A. Proton mang điện tích dương, nằm trong hạt nhân, khối lượng gần bằng 1 amu
B. Electron mang điện tích âm, nằm trong hạt nhân, khối lượng gần bằng 0 amu
C. Neutron không mang điện, khối lượng gần bằng 1 amu
D. Nguyên tử trung hòa về điện, có kích thước lớn hơn nhiều so với hạt nhân, nhưng có khối lượng gần bằng khối lượng hạt nhân
Điện tích của hạt nhân nguyên tử do thành phần nào quyết định? Từ đó, rút ra nhận xét về mối quan hệ giữa số đơn vị điện tích hạt nhân và số proton.
Nguyên tử natri (sodium) có điện tích hạt nhân là +11. Cho biết số proton và số electron trong nguyên tử này.
Nguyên tử oxygen có 8 electron, cho biết hạt nhân của nguyên tử này có điện tích là bao nhiêu?
Quan sát Hình 2.1, cho biết thành phần nguyên tử gồm những loại hạt nào? 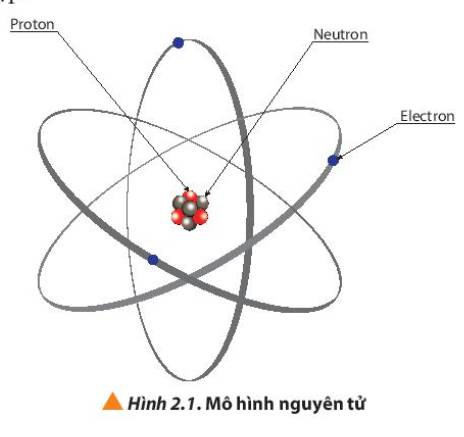
Từ rất lâu, các nhà khoa học đã nghiên cứu các mô hình nguyên tử và cập nhật chúng thông qua việc thu thập những dữ liệu thực nghiệm. Nguyên tử gồm những hạt cơ bản nào? Cơ sở nào để phát hiện ra các hạt cơ bản đó và chúng có tính chất gì? 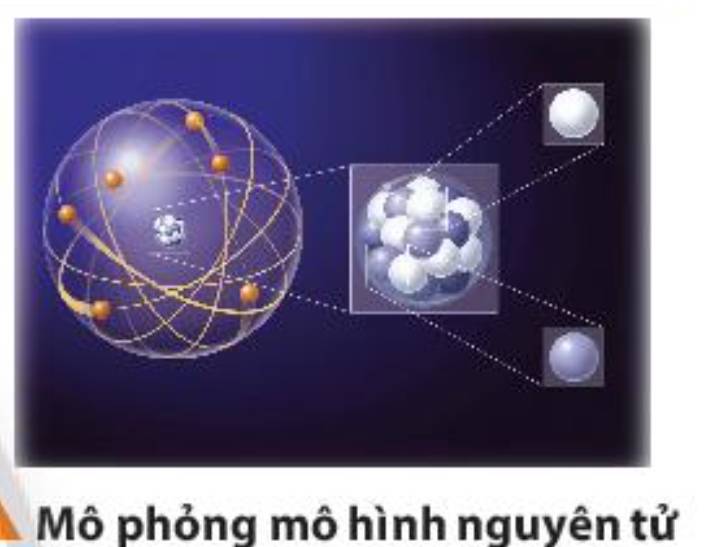
Quan sát Hình 2.6, hãy lập tỉ lệ giữa đường kính nguyên tử và đường kính hạt nhân của nguyên tử carbon. Từ đó, rút ra nhận xét.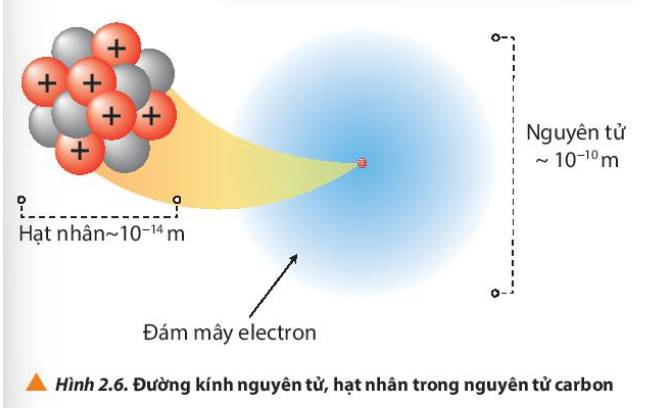
a) Cho biết 1g electron có bao nhiêu hạt
b) Tính khối lượng của 1 mol electron (biết hằng số Avogadro có giá trị là 6,022 x 1023)
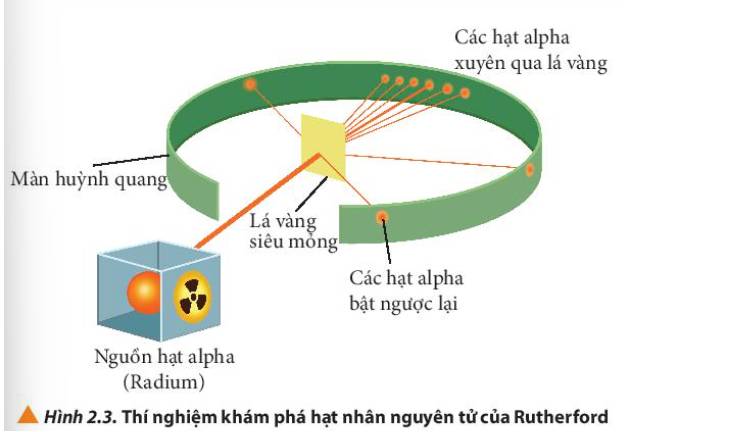
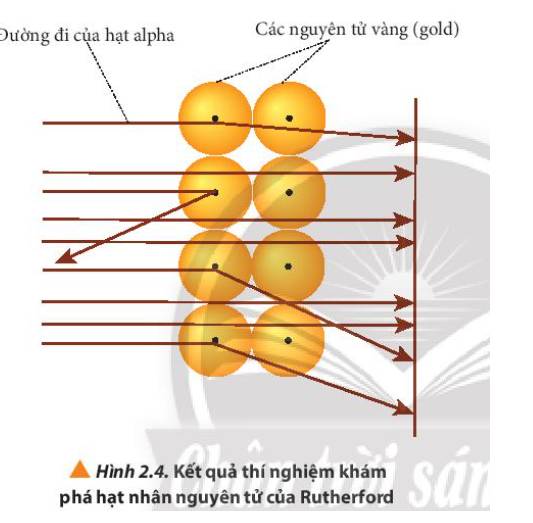
Quan sát Hình 2.3, cho biết các hạt α có đường đi như thế nào. Dựa vào Hình 2.4, giải thích kết quả thí nghiệm thu được.