Bài 4: Luyện tập Este và Chất béo
Nội dung lý thuyết
Các phiên bản khácI. KIẾN THỨC CẦN NHỚ
| Este | Lipit | |
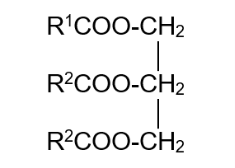
| Thành phần | Khi thay thế nhóm OH của nhóm cacbyxyl trong phân tử axit cacboxylic bằng nhóm OR ta thu được hợp chất este (R là gốc hidrocacbon). | Là trieste của axit béo có mạch cacbon dài với glixerol |
| Công thức | Este no, đơn chức, mạch hở: CnH2nO2 (n≥2). Ví dụ: CH3COOCH3: Metyl axetat |
|
| Tính chất hóa học | Thủy phân trong môi trường axit. RCOOR' + H2O Thủy phân trong môi trường bazơ. RCOOR' + NaOH → RCOONa + R'OH Phản ứng cháy. Phản ứng gốc hidrocacbon. | Thủy phân trong môi trường axit. (RCOO)3C3H5 + 3H2O Thủy phân trong môi trường bazơ. (RCOO)3C3H5 + 3NaOH Phản ứng hidro hóa chất béo lỏng. (C17H33COO)3C3H5 (lỏng) + 3H2 |
II. BÀI TẬP
Bài 1. Để thủy phân hoàn toàn m gam este đơn chức X có khả năng tham gia phản ứng tráng gương cần dùng vừa đủ 200ml dung dịch NaOH 0,25M, sau phản ứng thu được 2,3 gam ancol và 3,4 gam muối. Tìm công thức cấu tạo của X.
Lời giải
Gọi công thức của X là: RCOOR'.
RCOOR' + NaOH → RCOONa + R'OH
Áp dụng ĐLBT khối lượng: meste + mNaOH = mRCOONa + mR'OH
<=> meste + 0,2.0,25.40 = 2,3 + 3,4
<=> meste = 3,7 gam
Mà neste = nNaOH = 0,2.25 = 0,05 mol
➜ Meste = \(\dfrac{3,7}{0,05}\) = 74 g/mol
Mà este có khả năng tham gia phản ứng tráng gương ➜ CTCT của X là HCOOC2H5.
Bài 2. Đốt cháy hoàn toàn 4,2 gam một este E thu được 6,16 gam CO2 và 2,52 gam H2O. Xác định công thức phân tử, công thức cấu tạo, và tên gọi của E.
Lời giải
nCO2 = \(\dfrac{6,16}{44}\) = 0,14 mol và nH2O = \(\dfrac{2,52}{18}\) = 0,14 mol.
Ta thấy khi đốt cháy E thu được CO2 và H2O có số mol bằng nhau, vậy E là este no, đơn chức, mạch hở.
Phương trình cháy:
CnH2nO2 + \(\dfrac{3n-2}{2}\)O2 \(\underrightarrow{t^o}\) nCO2 + nH2O
➜nE = \(\dfrac{nCO_2}{n}=\dfrac{0,14}{n}\)
<=> ME = 4,2 : \(\dfrac{0,14}{n}\)= 30n ➜ n = 2 và ME = 60 g/mol
Công thức phân tử của E: C2H4O2.
Công thức cấu tạo của E: HCOOCH3 (metyl fomat).
Bài 3. Thủy phân hoàn toàn triglixerit X trong NaOH dư, thu được 18,4 gam glixerol và 182,4 gam một muối của axit béo. Xác định tên gọi của X.
Lời giải
nglixerol = \(\dfrac{18,4}{92}\) = 0,2 mol.
(RCOO)3C3H5 + 3NaOH → 3RCOONa + C3H5(OH)3
Theo phương trình ta có: nRCOONa = 3nglixerol = 0,2.3 = 0,6 mol
➜ MRCOONa = \(\dfrac{182,4}{0,6}\) = 304 g/mol
<=> MR = 304 - 67 = 237 (C17H33)
Vậy X là (C17H33COO)3C3H5: Triolein.
Bài 4. Hidro hóa hoàn toàn m gam triolein thì thu được 89 gam tristearin. Tính giá trị của m.
Lời giải
Phương trình hóa học:
(C17H33COO)3C3H5 + 3H2 → (C17H35COO)3C3H5
ntristearin = \(\dfrac{89}{890}\) = 0,1 mol.
=> ntristearin = 0,1 mol, nH2 = 0,3 mol
BTKL => mtriolein = 89 - 0,3.2 = 88,4 gam.
Trong quá trình học tập, nếu có bất kỳ thắc mắc nào, các em hãy để lại câu hỏi ở mục hỏi đáp để cùng thảo luận và trả lời nhé. Chúc các em học tốt!
Danh sách các phiên bản khác của bài học này. Xem hướng dẫn