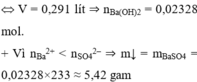Câu 32: Trộn 250ml dung dịch A gồm Ba(OH)2 0,2M và NaOH 0,3M với 250ml dung dịch H_{2}*S*O_{4} có pH = 1 Sau khi trộn thu được dung dịch B và m (g) kết tủa. a) Tính pH của dung dịch A. b) Tính nồng độ các ion trong dung dịch thu được. c) Tính pH của dung dịch thu được d) Tính m Giúp em với ạ

Những câu hỏi liên quan
Trộn 250ml dd H2SO4 0,15M với 250ml dd Na2CO3 0,08M thu được dung dịch A.
a) Tính nồng độ mol các ion trong dung dịch A
b) Trộn 1/2 thể tích dung dịch A với 250ml dung dịch B gồm Ba(OH)2 0,02M và NaOH x(M) thu được dung dịch V(ml) có pH=12 và m (g) kết tủa. Tính x và m?
Trộn 150 ml dung dịch hỗn hợp NaOH 0,2M và KOH 0,2M với 250ml dung dịch HCl 0,4 M thu được dung dịch (X)
a/ Tính nồng độ các ion trong dung dịch (X)
b/ Tính pH của dung dịch (X)a, \(n_{NaOH}=0,15.0,2=0,03\left(mol\right)=n_{Na^+}=n_{OH^-}\)
\(n_{KOH}=0,15.0,2=0,03\left(mol\right)=n_{K^+}=n_{OH^-}\)
⇒ ΣnOH- = 0,03 + 0,03 = 0,06 (mol)
\(n_{HCl}=0,25.0,4=0,1\left(mol\right)=n_{H^+}=n_{Cl^-}\)
\(H^++OH^-\rightarrow H_2O\)
0,06____0,06 (mol) ⇒ nH+ dư = 0,1 - 0,06 = 0,04 (mol)
\(\left[Na^+\right]=\left[K^+\right]=\dfrac{0,03}{0,15+0,25}=0,075\left(M\right)\)
\(\left[H^+\right]=\dfrac{0,04}{0,15+0,25}=0,1\left(M\right)\)
\(\left[Cl^-\right]=\dfrac{0,1}{0,15+0,25}=0,25\left(M\right)\)
b, pH = -log[H+] = 1
Đúng 2
Bình luận (0)
Trộn 3 dung dịch HCl 0,3M, HNO3 0,3M và H2SO4 0,2M vói thể thích bằng nhau thu được dung dịch X. Lấy 360 ml dung dịch X cho phản ứng dung dịch hỗn hợp Y gồm Ba(OH)2 0,08M và NaOH 0,23M thu được m gam kết tủa và dung dịch Z có pH 2. Giá trị của m gần nhất với A. 5,54 B. 5,42. C. 5,59. D. 16,61.
Đọc tiếp
Trộn 3 dung dịch HCl 0,3M, HNO3 0,3M và H2SO4 0,2M vói thể thích bằng nhau thu được dung dịch X. Lấy 360 ml dung dịch X cho phản ứng dung dịch hỗn hợp Y gồm Ba(OH)2 0,08M và NaOH 0,23M thu được m gam kết tủa và dung dịch Z có pH = 2. Giá trị của m gần nhất với
A. 5,54
B. 5,42.
C. 5,59.
D. 16,61.
Trộn lẫn 3 dung dịch HCl 0,3M, HNO3 0,3M và H2SO4 0,2M với những thể thích bằng nhau thu được dung dịch X. Lấy 360 ml dung dịch d X cho phản ứng với V lít dung dịch Y gồm Ba(OH)2 0,08M và NaOH 0,23M thu được m gam kết tủa và dung dịch Z có pH 2. Giá trị của m gần nhất với A. 5,54. B. 5,42. C. 5,59. D. 16,61.
Đọc tiếp
Trộn lẫn 3 dung dịch HCl 0,3M, HNO3 0,3M và H2SO4 0,2M với những thể thích bằng nhau thu được dung dịch X. Lấy 360 ml dung dịch d X cho phản ứng với V lít dung dịch Y gồm Ba(OH)2 0,08M và NaOH 0,23M thu được m gam kết tủa và dung dịch Z có pH = 2. Giá trị của m gần nhất với
A. 5,54.
B. 5,42.
C. 5,59.
D. 16,61.
Đáp án B
Ta có: nHCl = 0,036 mol, nHNO3 = 0,036 mol, nH2SO4 = 0,024 mol
⇒ ∑nH+ = 0,12 mol || ∑nOH– = 0,08×2×V + 0,23×V = 0,39V.
+ Vì pH = 2 ⇒ Sau pứ trung hòa nH+ dư = 102×(0,36+V) = 0,01V + 0,0036
+ Ta có: ∑nH+ = ∑nOH– + nH+ dư Û 0,12 = 0,39V + 0,01V + 0,0036.
⇔ V = 0,291 lít ⇒ nBa(OH)2 = 0,02328 mol.
+ Vì nBa2+ < nSO42– ⇒ m↓ = mBaSO4 = 0,02328×233 ≈ 5,42 gam
Đúng 0
Bình luận (0)
Trộn lẫn 3 dung dịch HCl 0,3M, HNO3 0,3M và H2SO4 0,2M với những thể thích bằng nhau thu được dung dịch X. Lấy 360 ml dung dịch d X cho phản ứng với V lít dung dịch Y gồm Ba(OH)2 0,08M và NaOH 0,23M thu được m gam kết tủa và dung dịch Z có pH 2. Giá trị của m gần nhất với A. 5,54. B. 5,42. C. 5,59. D. 16,61.
Đọc tiếp
Trộn lẫn 3 dung dịch HCl 0,3M, HNO3 0,3M và H2SO4 0,2M với những thể thích bằng nhau thu được dung dịch X. Lấy 360 ml dung dịch d X cho phản ứng với V lít dung dịch Y gồm Ba(OH)2 0,08M và NaOH 0,23M thu được m gam kết tủa và dung dịch Z có pH = 2. Giá trị của m gần nhất với
A. 5,54.
B. 5,42.
C. 5,59.
D. 16,61.
Đáp án B
Ta có: nHCl = 0,036 mol, nHNO3 = 0,036 mol, nH2SO4 = 0,024 mol
⇒ ∑nH+ = 0,12 mol || ∑nOH– = 0,08×2×V + 0,23×V = 0,39V.
+ Vì pH = 2 ⇒ Sau pứ trung hòa nH+ dư = 102×(0,36+V) = 0,01V + 0,0036
+ Ta có: ∑nH+ = ∑nOH– + nH+ dư ⇔ 0,12 = 0,39V + 0,01V + 0,0036.
Û V = 0,291 lít ⇒ nBa(OH)2 = 0,02328 mol.
+ Vì nBa2+ < nSO42– ⇒ m↓ = mBaSO4 = 0,02328×233 ≈ 5,42 gam
Đúng 0
Bình luận (0)
Trộn lẫn 3 dung dịch HCl 0,3M,
HNO
3
0,3M và
H
2
SO
4
0,2M với những thể thích bằng nhau thu được dung dịch X. Lấy 360 ml dung dịch d X cho phản ứng với V lít dung dịch Y gồm
Ba
(
OH
)
2
0,08M và NaOH 0,...
Đọc tiếp
Trộn lẫn 3 dung dịch HCl 0,3M, HNO 3 0,3M và H 2 SO 4 0,2M với những thể thích bằng nhau thu được dung dịch X. Lấy 360 ml dung dịch d X cho phản ứng với V lít dung dịch Y gồm Ba ( OH ) 2 0,08M và NaOH 0,23M thu được m gam kết tủa và dung dịch Z có pH = 2. Giá trị của m gần nhất với
A. 5,54.
B. 5,42.
C. 5,59.
D. 16,61.
Trộn 200 ml dung dịch gồm HCl 0,1M và H2SO4 0,15M với 300 ml dung dịch Ba(OH)2 nồng độ 0,05M, thu được m gam kết tủa và dung dịch (X). a/ Tính m và nồng độ các ion có trong dung dịch (X) b/ pH của dung dịch (X)
Đọc tiếp
Trộn 200 ml dung dịch gồm HCl 0,1M và H2SO4 0,15M với 300 ml dung dịch Ba(OH)2 nồng độ 0,05M, thu được m gam kết tủa và dung dịch (X).
a/ Tính m và nồng độ các ion có trong dung dịch (X)
b/ pH của dung dịch (X)
a, \(n_{HCl}=0,2.0,1=0,02\left(mol\right)=n_{H^+}=n_{Cl^-}\)
\(n_{H_2SO_4}=0,2.0,15=0,03\left(mol\right)=n_{SO_4^{2-}}\) \(\Rightarrow n_{H^+}=2n_{H_2SO_4}=0,06\left(mol\right)\)
\(\Rightarrow\Sigma n_{H^+}=0,02+0,06=0,08\left(mol\right)\)
\(n_{Ba\left(OH\right)_2}=0,3.0,05=0,015\left(mol\right)=n_{Ba^{2+}}\)
\(\Rightarrow n_{OH^-}=2n_{Ba\left(OH\right)_2}=0,03\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
0,03___0,03 (mol) ⇒ nH+ dư = 0,05 (mol)
\(Ba^{2+}+SO_4^{2-}\rightarrow BaSO_4\)
0,015___0,015______0,015 (mol) ⇒ nSO42- dư = 0,015 (mol)
⇒ m = mBaSO4 = 0,015.233 = 3,495 (g)
\(\left[Cl^-\right]=\dfrac{0,02}{0,2+0,3}=0,04\left(M\right)\)
\(\left[H^+\right]=\dfrac{0,05}{0,2+0,3}=0,1\left(M\right)\)
\(\left[SO_4^{2-}\right]=\dfrac{0,015}{0,2+0,3}=0,03\left(M\right)\)
b, pH = -log[H+] = 1
Đúng 2
Bình luận (0)
Trộn 100ml dung dịch B gồm Ba(OH)2 0,05M; NaOH 0,3M với 100ml dung dịch A chứa FeCl2 0,2M và H2SO4 0,1M thì thu được bao nhiêu gam kết tủa?
\(n_{Ba^{2+}}=0.1\cdot0.05=0.005\left(mol\right)\)
\(n_{OH^-}=0.1\cdot0.05\cdot2+0.1\cdot0.3=0.04\left(mol\right)\)
\(n_{Fe^{2+}}=0.1\cdot0.2=0.02\left(mol\right)\)
\(n_{SO_4^{2-}}=0.1\cdot0.1=0.01\left(mol\right)\)
\(n_{H^+}=0.1\cdot0.1\cdot2=0.02\left(mol\right)\)
\(Ba^{2+}+SO_4^{2-}\rightarrow BaSO_4\)
\(0.005....0.005..........0.005\)
\(\Rightarrow SO_4^{2-}dư\)
\(OH^-+H^+\rightarrow H_2O\)
\(0.02.......0.02\)
\(Fe^{2+}+2OH^-\rightarrow Fe\left(OH\right)_2\)
\(0.01....0.04-0.02....0.01\)
\(\Rightarrow Fe^{2+}dư\)
\(m\downarrow=0.005\cdot197+0.01\cdot90=2.065\left(g\right)\)
Đúng 1
Bình luận (0)
Trộn 250ml dung dịch hỗn hợp HCl 0.08M và H2SO4 0.01M với 250ml dung dịch Ba(OH)2 có nồng độ x M thu được m gam kết tủa và 500ml dung dịch có pH=2. Tính x và m( coi Ba(OH)2 phân li hòa toàn cả hai nấc
nBa(OH)2 = 0,25 x mol; nOH-= 0,5x mol
nH+ = 0,025 mol, nSO4(2-) = 0,0025 mol
H++ OH- → H2O
0,025 0,025 mol
Dung dịch sau phản ứng có pH = 12 nên OH- dư
nOH- dư = 0,5x- 0,025
[OH-] dư = nOH- dư/ Vdd = (0,5x- 0,025)/0,5 =10-2 suy ra a = 0,06 M
Ba2++ SO42- → BaSO4
0,015 0,0025 0,0025 mol
mBaSO4 = 0,5825 gam
Đúng 1
Bình luận (0)