nung a gam KMnO4 thu được lượng oxi vừa đủ oxi hóa 7,84 gam S
a) tìm a
Nung a gam KmnO4 thu được lượng oxi vừa đủ oxi hoá 7,84 gam S.
a. Tìm a.
b. Nếu cũng nhiệt phân a gam KClO3 thì sau phản ứng lượng O2 thu được gấp bao nhiêu lần lượng O2 ở trên ?
Trong phòng thí nghiệm, bạn Minh nung 63,2 gam KMnO4.
a/ Tính thể tích khí oxi thu được ở đktc biết hiệu suất phản ứng đạt 90%.
b/ Lượng oxi thu được ở câu a vừa đủ để đốt cháy 6,48 gam kim loại R hóa trị III. Tìm kim loại R.
\(n_{KMnO_4}=\dfrac{63,2}{158}=0,4\left(mol\right)\\
pthh:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
0,4 0,2
=> \(V_{O_2\left(lt\right)}=0,2.22,4=4,48\left(l\right)\\
V_{O_2\left(tt\right)}=\dfrac{90.4,48}{100}=4,032\left(l\right)\)
Đốt cháy 9,6 gam Mg trong bình đựng V lít khí oxi vừa đủ (đktc) thu được x gam sản phẩm (là hợp chất của Mg và oxi).
a/ Viết phương trình hóa học của phản ứng xảy ra.
b/ Tìm x, V.
c/ Để có được lượng oxi trên, cần dùng bao nhiêu gam KClO3, biết khi nung KClO3 ta thu được khí oxi và chất rắn KCl.
\(a,2Mg+O_2\rightarrow\left(t^o\right)2MgO\\ b,n_{Mg}=\dfrac{9,6}{24}=0,4\left(mol\right)\\ n_{MgO}=n_{Mg}=0,4\left(mol\right)\\ n_{O_2}=\dfrac{0,4}{2}=0,2\left(mol\right)\\ b,x=m_{MgO}=40.0,4=16\left(g\right)\\ V=V_{O_2\left(đktc\right)}=0,2.22,4=4,48\left(l\right)\\ c,2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\uparrow\\ n_{KClO_3}=\dfrac{2}{3}.n_{O_2}=\dfrac{2}{3}.0,2=\dfrac{2}{15}\left(mol\right)\\ \Rightarrow m_{KClO_3}=\dfrac{2}{15}.122,5=\dfrac{49}{3}\left(g\right)\)
a, 2Mg + O2 \(\rightarrow\) 2MgO (bạn thêm to trên cái mũi tên nhé)
b, nMg = \(\dfrac{9,6}{24}\) = 0,4 (mol)
PTPƯ: 2Mg + O2 \(\rightarrow\) 2MgO
2g/mol 1g/mol 2g/mol
\(\Rightarrow\) 0,4 0,2 0,4
VO2 = 0,2 . 22,4 = 4,48l
mMgO = 0,4 . (24 + 16) = 16(g)
Câu 5: Đốt cháy a gam Zn trong bình đựng 6,72 lít không khí vừa đủ (đktc) thu được x gam sản phẩm (là hợp chất của Zn và oxi).
a/ Viết PTHH.
b/ Tìm a, x. Biết O2 chiếm 20% thể tích không khí.
c/ Để có được lượng oxi trên, cần dùng bao nhiêu gam KMnO4, biết khi nung KMnO4 ta có phản ứng sau: KMnO4 à K2MnO4 + MnO2 + O2.
\(n_{O_2}=\dfrac{6,72}{5.22,4}=0,06\left(mol\right)\\ PTHH:2Zn+O_2\underrightarrow{t^o}2ZnO\\ Mol:0,03\leftarrow0,06\rightarrow0,03\\ \rightarrow\left\{{}\begin{matrix}a=0,03.65=1,95\left(g\right)\\x=0,03.81=2,43\left(g\right)\end{matrix}\right.\)
\(PTHH:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
0,12 0,06
\(\rightarrow m_{KMnO_4}=0,12.158=18,96\left(g\right)\)
Nung a gam KClO3 và b gam KMnO4 thì thu được cùng một lượng oxi. Tính tỉ lệ a/b.
Giả sử có 1 mol oxi
\(2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2\)
Theo PTHH: \(n_{KMnO_4}=2n_{O_2}=2.1=2\left(mol\right)\)
\(\Rightarrow m_{KMnO_4}=2.158=316\left(g\right)\)
\(2KClO_3\rightarrow2KCl+3O_2\)
Theo PTHH: \(n_{KClO_3}=\dfrac{1.2}{3}=\dfrac{2}{3}\left(mol\right)\)
\(\Rightarrow m_{KClO_3}=n_{KClO_3}.M_{KClO_3}=\dfrac{2}{3}.122,5=\dfrac{245}{3}\left(g\right)\)
Tỉ lệ \(\dfrac{a}{b}\) là:
\(\dfrac{a}{b}=\dfrac{m_{KMnO_4}}{m_{KClO_3}}=\dfrac{316}{\dfrac{245}{3}}=\dfrac{948}{245}\)
Cho 21,4 gam hỗn hợp A gồm: Fe và kim loại X ( có hóa trị II) tác dụng hoàn toàn với 179,3g dung dịch axit clohydric (vừa đủ) ta thu được 7,84 lít khí ở đktc. Mặt khác đốt cùng lượng hỗn hợp A ở trên trong khí oxi thì phải dùng hết 4,48 lít khí oxi đo ở đktc. Xác định kim loại X
Gọi: \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_X=b\left(mol\right)\end{matrix}\right.\) ⇒ 56a + MX.b = 21,4 (1)
- Đốt A trong oxi.
PT: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
\(2X+O_2\underrightarrow{t^o}2XO\)
Theo PT: \(n_{O_2}=\dfrac{2}{3}n_{Fe}+\dfrac{1}{2}n_X=\dfrac{2}{3}a+\dfrac{1}{2}b=\dfrac{4,48}{22,4}=0,2\left(mol\right)\left(2\right)\)
- Cho pư với HCl
+ TH1: X không pư với HCl.
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(n_{Fe}=n_{H_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)=a\)
Thay vào (2) được b = -1/15 → vô lý.
+ TH2: X có pư với HCl.
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(X+2HCl\rightarrow XCl_2+H_2\)
Theo PT: \(n_{H_2}=n_{Fe}+n_X=a+b=\dfrac{7,84}{22,4}=0,35\left(mol\right)\left(3\right)\)
Từ (2) và (3) \(\Rightarrow\left\{{}\begin{matrix}a=0,15\left(mol\right)\\b=0,2\left(mol\right)\end{matrix}\right.\). Thay vào (1) được MX = 65 (g/mol)
Vậy: X là kẽm. (Zn)
Trong phòng thí nghiệm người ta điều chế oxit sắt từ Fe3O4 bằng cách dùng oxi hóa sắt ở nhiệt độ cao.
a) Tính số gam sắt và oxi cần dùng để điều chế được 2,32g oxi sắt từ?
b) Tính số gam kali pemanganat KMnO4 cần dùng để có được lượng oxi dùng cho phản ứng trên, biết rằng khi nung nóng 2 mol KMnO4 thì thu được 1 mol O2.
a) Phương trình hóa học của phản ứng:
3Fe + 2O2 → Fe3O4.
nFe3O4 = 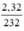 = 0,01 mol.
= 0,01 mol.
nFe = 3.nFe3O4 = 0,01 .3 = 0,03 mol.
nO2 = 2.nFe3O4 = 0,01 .2 = 0,02 mol.
mFe = 0,03.56 = 1,68g.
mO2 = 0,02.32 = 0,64g.
b) Phương trình phản ứng nhiệt phân KMnO4:
2KMnO4 → K2MnO4 + MnO2 + O2
nKMnO4 = 2.nO2 = 0,02.2 = 0,04 mol.
mKMnO4 = 0,04 .158 = 6,32g.
Nung a gam KClO3 và b gam KMnO4 thu được cùng lượng Oxi . tính tỉ lệ a:b
2KCLO3 → 2KCL + 3O2 (1)
2KMnO4 → K2MnO4 + MnO2 + O2 (2)
Vì thu được cùng lượng Oxi
⇒ gọi n02(PT1) = n02(PT2) = c(mol)
Theo PT(1) ⇒ nKCLO3 = 2/3 . n02= 2/3 . c(mol)
✳ MKCLO3 = 39+ 35,5 + (16 . 3) =122,5 g/mol
⇒mKCLO3 = n.M= 2/3 . c . 122,5= 245/3 .c(g)
Theo PT(2) ⇒ nKMnO4 = 2. n02 =2c(mol)
⇒ mKMnO4 = n.M = 2c.158 = 316c(g)
⇒ Tỉ lệ mKCLO3 : mKMnO4 = a : b = 245/3 .c : 316.c = 245 : 948
Trong phòng thí nghiệm, người ta thường dùng KMnO4, KClO3 để điều chế oxi.
1. Nêu và giải thích phương pháp thu khí oxi vào lọ?
2. Khi nung nóng lần lượt a gam KMnO4 và b gam KClO3 sau phản ứng hoàn toàn thu được cùng một lượng khí oxi. Hãy tính tỉ lệ a/b?
-thu oxi có 2 loại
-Đẩy kk ; là ta lật ngửa bình để thu=>O2 nặng hơn kk
-Đẩy nước : ta có thể dời nước =>O2 ko tan trong nước , ko td vs nước
2
cùng 1 lượng oxi
2KMNO4-to>K2MnO4+MnO2+O2
2KClO3-to>2KClO3+3O2
=>\(\dfrac{a}{b}=\dfrac{2.158}{2\backslash3.122,5}=3.869\)
thu khí O2 bằng 2pp :
đẩy nước vì O2 ít tan trong nước
đẩy KK bằng cách đặt ngửa bình vì O2 nhẹ hơn KK
gọi nO2 là x
\(pthh:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
2x x
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
\(\dfrac{2}{3}x\) x
=> \(\left\{{}\begin{matrix}m_{KMnO_4}=2x.158=316x\\m_{KClO_3}=\dfrac{2}{3}x.122,5=81,6x\end{matrix}\right.\)
=> \(\dfrac{a}{b}=\dfrac{316x}{81,6x}=\dfrac{395}{102}\)