Cho hỗn hợp X gồm m(g) Fe và 30,16g Fe3O4 tác dụng với H2SO4 loãng dư được dung dịch gồm FeSO4 và Fe2(SO4)3 và khí H2. Cho tác dụng với 90ml KMNO4 0,57M vừa đủ. Tính phần trăm về khối lượng của Fe trong X

Những câu hỏi liên quan
Cho 19,3 gam hỗn hợp gồm Al và Fe tác dụng vừa đủ với 200 ml dung dịch gồm HCl 2M và H2SO4 2,25M (loãng) thu được V lít khí H2 (đktc) và dung dịch B.
a) Tính thành phần phần trăm khối lượng của Al và Fe trong hỗn hợp ban đầu.
b) Tính tổng khối lượng muối có trong dung dịch B.
\(n_{Al}=a\left(mol\right)\)
\(n_{Fe}=b\left(mol\right)\)
\(m=27a+56b=19.3\left(g\right)\left(1\right)\)
\(n_{H^+}=0.2\cdot2+0.2\cdot2.25\cdot2=1.3\left(mol\right)\)
\(2Al+6H^+\rightarrow2Al^{3+}+3H_2\)
\(Fe+2H^+\rightarrow Fe^{2+}+H_2\)
\(n_{H^+}=3a+2b=1.3\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.3,b=0.2\)
\(\%Al=\dfrac{0.3\cdot27}{19.3}\cdot100\%=41.96\%\)
\(\%Fe=58.04\%\)
\(b.\)
\(n_{H_2}=\dfrac{1}{2}n_{H^+}=0.65\left(mol\right)\)
Bảo toàn khối lượng :
\(m_{Muối}=19.3+0.4\cdot36.5+0.45\cdot98-0.65\cdot2=76.7\left(g\right)\)
Đúng 4
Bình luận (4)
Cho m gam Fe tác dụng với O2 thu được 27,2 gam hỗn hợp A gồm FeO, Fe3O4, Fe2O3, Fe dư. Cho hỗn hợp A tác dụng hết với dung dịch H2SO4 98% đun nóng thu được 6,72 lít khí SO2 (đktc) và dd B chỉ chứa muối Fe2(SO4)3 .Khối lượng m và khối lượng dung dịch H2SO4 đã dùng lần lượt là?
Cho m gam hỗn hợp X gồm Ca,Fe, Al tác dụng với một lượng vừa đủ dung dịch chứa H2SO4 được 11,2(l) khí H2(đktc) và 68 (g) hỗn hợp Y gồm CaSO4, FeSO4, Al2(SO4)3. a) Viết PTHH xảy ra? b) Tìm m?
Xem chi tiết
a) PTHH: \(Ca+H_2SO_4\rightarrow CaSO_4+H_2\uparrow\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\)
b) Ta có: \(\Sigma n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
Theo các PTHH, ta thấy \(n_{H_2SO_4}=n_{H_2}=0,5\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=0,5\cdot98=49\left(g\right)\)
Mặt khác: \(m_{H_2}=0,5\cdot2=1\left(g\right)\)
Bảo toàn khối lượng: \(m_{hh}=m_{muối}+m_{H_2}-m_{H_2SO_4}=68+1-49=20\left(g\right)\)
Đúng 1
Bình luận (0)
Cho m gam hỗn hợp gồm Fe và Fe2O3 tác dụng với dung dịch H2SO4 vừa đủ thu được dung dịch A chứa 55,2 gam muối và 2,24 lit H2. a. Tính m b. Tính khối lượng H2SO4 phản ứngBiết Fe2O3 + H2SO4 ® Fe2(SO4)3 + H2O
Đọc tiếp
Cho m gam hỗn hợp gồm Fe và Fe2O3 tác dụng với dung dịch H2SO4 vừa đủ thu được dung dịch A chứa 55,2 gam muối và 2,24 lit H2.
a. Tính m
b. Tính khối lượng H2SO4 phản ứng
Biết Fe2O3 + H2SO4 ® Fe2(SO4)3 + H2O
5.Cho 0,83 gam hỗn hợp gồm Al và Fe tác dụng với dung dịch H2SO4 loãng dư
theo phản ứng:
Al + H2SO4 → Al2( SO4)3 + H2 ; Fe + H2SO4 → FeSO4 + H2 ; sau phản
ứng thu được 0,56 lít khí ở đktc. Tính khối lượng mỗi kim loại có trong hỗn
hợp ban đầu?
Gọi x, y lần lượt là số mol Al, Fe
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ n_{H_2}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\\ Tacó:\left\{{}\begin{matrix}27x+56y=0,83\\1,5x+y=0,025\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}x=0,01\\y=0,01\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}m_{Al}=0,27\left(g\right)\\m_{Fe}=0,56\left(g\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Cho 30,8 gam hỗn hợp X gồm Fe, FeO, FeCO3, Mg, MgO và MgCO3 tác dụng vừa đủ với dung dịch H2SO4 loãng, thu được 7,84 lít (đktc) hỗn hợp khí Y gồm CO2, H2 và dung dịch Z chỉ chứa 60,4 gam hỗn hợp muối sunfat trung hòa. Tỉ khối của Y so với He là 6,5. Khối lượng của FeSO4 trong dung dịch Z là A. 22,4 gam. B. 30,4 gam. C. 26,8 gam. D. 30,0 gam.
Đọc tiếp
Cho 30,8 gam hỗn hợp X gồm Fe, FeO, FeCO3, Mg, MgO và MgCO3 tác dụng vừa đủ với dung dịch H2SO4 loãng, thu được 7,84 lít (đktc) hỗn hợp khí Y gồm CO2, H2 và dung dịch Z chỉ chứa 60,4 gam hỗn hợp muối sunfat trung hòa. Tỉ khối của Y so với He là 6,5. Khối lượng của FeSO4 trong dung dịch Z là
A. 22,4 gam.
B. 30,4 gam.
C. 26,8 gam.
D. 30,0 gam.
Đáp án B
Dùng phương pháp đường chéo tính được mol CO2 là 0,2 mol và H2 là 0,15 mol.
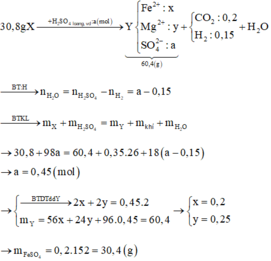
Đúng 0
Bình luận (0)
Cho 4 gam hỗn hợp X gồm Fe và Cu tác dụng với dung dịch H2SO4 loãng dư thì thu được 1,12 lít khí (đktc). Thành phần phần trăm theo khối lượng của Fe và Cu trong hỗn hợp X lần lượt là A. 40% và 60%. B. 30% và 70%. C. 70% và 30%. D. 60% và 40%.
Đọc tiếp
Cho 4 gam hỗn hợp X gồm Fe và Cu tác dụng với dung dịch H2SO4 loãng dư thì thu được 1,12 lít khí (đktc). Thành phần phần trăm theo khối lượng của Fe và Cu trong hỗn hợp X lần lượt là
A. 40% và 60%.
B. 30% và 70%.
C. 70% và 30%.
D. 60% và 40%.
Đáp án C
Trong X, chỉ có Fe tác dụng với dung dịch H2SO4 loãng:

Đúng 0
Bình luận (0)
Cho 1,37g hỗn hợp X gồm Fe và kim loại M hoá trị không đổi tác dụng với dung dịch HCl dư thấy giải phóng 1,232 lít khí H2 (đkc). Mặt khác hỗn hợp X trên tác dụng vừa đủ với lượng khí Cl2 điều chế được bằng cách cho 3,792 gam KMnO4 tác dụng với dung dịch HCl đặc dư. Tỉ lệ số mol của Fe và M trong hỗn hợp là 1: 3. Kim loại M là A. Mg B. Cu C. Al D. Zn
Đọc tiếp
Cho 1,37g hỗn hợp X gồm Fe và kim loại M hoá trị không đổi tác dụng với dung dịch HCl dư thấy giải phóng 1,232 lít khí H2 (đkc). Mặt khác hỗn hợp X trên tác dụng vừa đủ với lượng khí Cl2 điều chế được bằng cách cho 3,792 gam KMnO4 tác dụng với dung dịch HCl đặc dư. Tỉ lệ số mol của Fe và M trong hỗn hợp là 1: 3. Kim loại M là
A. Mg
B. Cu
C. Al
D. Zn
Đáp án : C
X + HCl : Fe -> Fe2+ có nH2 = 0,055 mol
X + Cl2 : Fe -> Fe3+
bảo toàn e : 5nKMnO4 = 2nCl2 => nCl2 = 0,06 mol
Do M có hóa trị không đổi => nFe = ne (2) – ne (1) = 2nCl2 – 2nH2 = 0,01 mol
Giả sử M có hóa trị n => n.nM + 2.0,01 = 2nH2 => n.nM = 0,09 mol
Có : mX = 1,37g = 0,01.56 + nM.M => nM.M = 0,81g
=> M = 9n
Nếu n = 3 => M = 27g (Al) Thỏa mãn
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Fe và Fe3O4 được chia thành 2 phần bằng nhau:
Phần 1: Tác dụng với 90 ml dung dịch H2SO4 loãng 1M
Phần 2: Tác dụng với dung dịch H2SO4 đặc nóng dư thu được 560 ml khí SO2 (đktc)
Tính khối lượng mỗi chất trong X ?
Gọi: \(\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_{Fe_3O_4}=y\left(mol\right)\end{matrix}\right.\) (trong 1 phần)
- Phần 1: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(Fe_3O_4+4H_2SO_4\rightarrow FeSO_4+Fe_2\left(SO_4\right)_3+4H_2O\)
Theo PT: \(n_{H_2SO_4}=n_{Fe}+4n_{Fe_3O_4}=x+4y=0,09.1=0,09\left(mol\right)\left(1\right)\)
- Phần 2: \(n_{SO_2}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\)
BT e, có: 3nFe + nFe3O4 = 2nSO2 ⇒ 3x + y = 0,025.2 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,01\left(mol\right)\\y=0,02\left(mol\right)\end{matrix}\right.\)
→ X gồm: 0,02 (mol) Fe và 0,04 (mol) Fe3O4.
\(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=0,02.56=1,12\left(g\right)\\m_{Fe_3O_4}=0,04.232=9,28\left(g\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)

















