Tìm hiểu cấu tạo một số nguyên tử
Chuẩn bị: Mô hình nguyên tử của các nguyên tử carbon, nitrogen, oxygen theo Hình 2.5.
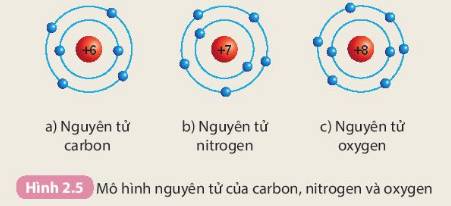
Quan sát các mô hình nguyên tử đã chuẩn bị, thảo luận nhóm và hoàn thành bảng theo mẫu sau:
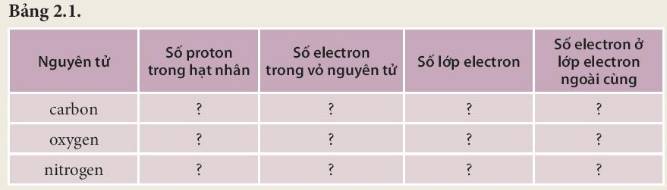
Tìm hiểu mối quan hệ giữa số electron ở lớp ngoài cùng của nguyên tử các nguyên tố với số thứ tự của nhóm
Chuẩn bị: 4 mô hình sắp xếp electron ở vỏ nguyên tử của Li, Na, F, Cl theo mẫu mô tả trong Hình 4.4.
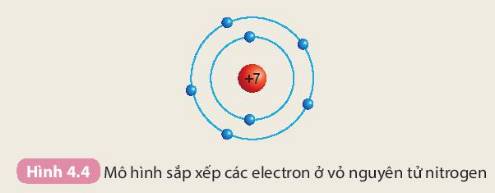
Quan sát các mô hình đã chuẩn bị, thảo luận và trả lời câu hỏi:
1. Hãy cho biết nguyên tử các nguyên tố nào có cùng số electron ở lớp ngoài cùng
2. Hãy so sánh số electron lớp ngoài cùng của nguyên tử các nguyên tố với số thứ tự nhóm của các nguyên tố đó
1:
Nguyên tử Li, Na có cũng số electron ở lớp ngoài cùng
Nguyên tử F, Cl có cũng số electron ở lớp ngoài cùng
2: Số electron lớp ngoài cùng của nguyên tử các nguyên tố chính là số thứ tự nhóm của các nguyên tố
Tìm hiểu mối quan hệ giữa số lớp electron của nguyên tử các nguyên tố với số thứ tự của chu kì
Chuẩn bị: 6 mô hình sắp xếp electron ở vỏ nguyên tử của sáu nguyên tố H, He, Li, Be, C, N theo mẫu được mô tả trong Hình 4.4
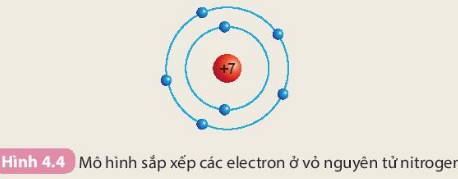
Quan sát các mô hình đã chuẩn bị, thảo luận và thực hiện các yêu cầu sau:
1. Hãy cho biết số lớp electron của nguyên tử các nguyên tố trên.
2. So sánh số lớp electron của nguyên tử các nguyên tố trên với số thứ tự chu kì của các nguyên tố đó.
1. Nguyên tử nguyên tố H , nguyên tử nguyên tố He có 1 lớp e
Nguyên tử nguyên tố Li, Be, C, N có 2 lớp e.
2. STT chu kì của nguyên tử nguyên tố H, He (1) < STT chu kì của nguyên tử nguyên tố Li, Be, C, N (2)
Quan sát Hình 2.2, áp dụng mô hình nguyên tử của Bo, mô tả cấu tạo của nguyên tử hydrogen và nguyên tử carbon
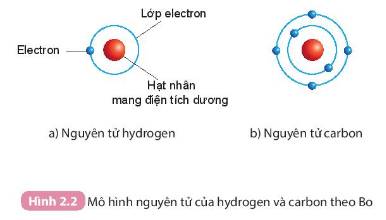
Áp dụng mô hình nguyên tử của Bo
- Nguyên tử hydrogen:
+ Hạt nhân nằm ở tâm, mang điện tích dương
+ Có 1 electron (mang điện tích âm) nằm ở lớp thứ nhất, quay xung quanh hạt nhân
- Nguyên tử carbon:
+ Hạt nhân nằm ở tâm, mang điện tích dương
+ Có 2 lớp electron và 6 electron phân bố ở các lớp: lớp thứ nhất có 2 electron, lớp thứ 2 có 4 electron. Các electron quay xung quanh hạt nhân.
Quan sát hình ảnh mô tả cấu tạo nguyên tử carbon và nhôm (hình 1.5), hãy cho biết mỗi nguyên tử đó có bao nhiêu lớp electron và số electron trên mỗi lớp electron đó.
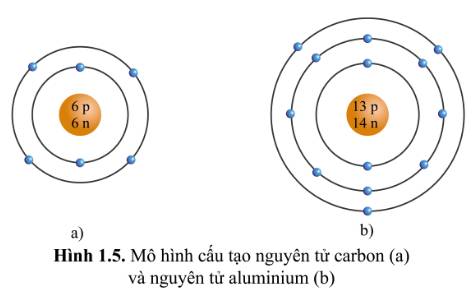
Hình 1.5
a)
-Cấu Tạo nguyên tử Carbon
+nguyên tử Carbon có hai lớp electron
+lớp thứ nhất có 2 electron
+lớp thứ hai có 4 electron
b) -Cấu Tạo nguyên tử Alumunium
+ nguyên tử Alumunium có 3 lớp electron
+ lớp thứ nhất có 2 electron
+ lớp thứ hai có 8 electron
+ lớp thứ ba có 3 electron
Hãy thảo luận để trả lời các câu hỏi dưới đây:
1. Nguyên tử có cấu tạo như thế nào? Hãy vẽ hình mô tả cấu tạo nguyên tử.
2. Electron trong nguyên tử có thể dịch chuyển như thế nào?
Tham khảo!
1. Cấu tạo nguyên tử gồm có hạt nhân và lớp vỏ electron. Trong đó:
Hạt nhân nằm ở tâm nguyên tử, gồm các hạt proton và nơtron.
Vỏ nguyên tử bao gồm các electron chuyển động trong không gian xung quanh hạt nhân.
=> Nguyên tử được cấu tạo bởi 3 loại hạt cơ bản là: electron, proton và nơtron.
2. Electron trong nguyên tử có thể dịch chuyển rời khỏi nguyên tử và di chuyển sang nơi khác.
Trong lịch sử các thuyết về mô hình nguyên tử, có mô hình hành tinh nguyên tử và mô hình hiện đại nguyên tử. Theo em, trong hai hình bên, hình nào thể hiện mô hình hành tinh nguyên tử, hình nào thể hiện mô hình hiện đại của nguyên tử?
- Mô hình hành tinh nguyên tử mô tả về sự chuyển động của electron.
- Hình a không mô tả sự chuyển động của electron
- Hình b mô tả sự chuyển động của electron
=> Hình b thể hiện mô hình hành tinh nguyên tử và Hình a thể hiện mô hình hiện đại của nguyên tử.
Dựa theo mô hình nguyên tử của Rutherford – Bohr, hãy vẽ mô hình nguyên tử các nguyên tố có Z từ 1 đến 11.
Làm được mô hình một số nguyên tử theo mô hình nguyên tử Bo
Câu 2. Hai nguyên tố A và B ở hai phân nhóm chính liên tiếp trong bảng tuần hoàn các nguyên tố hốa học. Tống số hiệu nguyên tử của A và B là 31. Xác định số hiệu nguyên tử, viết cấu hình electron của các nguyên tử của A và B. Viết cấu hình electron của các ion tạo thành
Giả sử \(Z_A< Z_B\)
Theo bài ra, ta có: \(Z_A+Z_B=31\)
\(\Rightarrow Z_A+\left(Z_A+1\right)=31\) \(\Rightarrow\left\{{}\begin{matrix}Z_A=15\\Z_B=16\end{matrix}\right.\)
Cấu hình electron:
A: [Ne]3s23p3
B: [Ne]3s23p4
A3-: [Ne]3s23p6
B2-: [Ne]3s23p6