cho nguyên tử Z có 2 lớp e,lớp thứ 2 có 2 e.xác định số hiệu nguyên tử z

Những câu hỏi liên quan
cho em hỏi thêm bài này đi mọi người
viết cấu hình electron nguyên tử , xác định số hiệu nguyên tử , và tên nguyên tố trong các trường hợp sau :
a) nguyên tử X có 3 lớp e , lớp ngoài cùng có 5e
b) nguyên tử Y có 4 lớp e , lớp ngoài cùng có 1e
c) nguyên tử Z có 4 lớp , lớp thứ 3 có 14e
lớp e : (1s)(2s2p)(3s3p3d)(4s4p4d4f)....
câu a : NT X có 3 lớp e => 1s2s2p3s3p3d
vì có 5 e lớp ngoài cùng => C/h e : 1s22s22p63s23p3
câu b, c tương tự nhé
Đúng 0
Bình luận (2)
a, 1s22s22p63s23p3
b, 1s22s22p63s23p64s1
c, 1s22s22p63s23p63d64s2
Đúng 0
Bình luận (1)
Số Hiệu Nguyên Tử:
a, 15
b,19
c, 26
Tên Nguyên tố:
a, photpho(P)
b, kali(K)
c, sắt(Fe)
Đúng 0
Bình luận (0)
Nguyên tử Z có 2 lớp electron, lớp ngoài cùng có 5 electron. Số hiệu nguyên tử của Z là
Từ dữ kiện đề bài, ta có thể xác định được cấu hình electron của nguyên tử
\(Z:1s^22s^22p^3\)
\(\rightarrow Z_Z=2+2+3=7\)
Đúng 4
Bình luận (0)
Cho những nguyên tố có số hiệu nguyên tử từ Z = 1 đến Z = 36. Tìm những nguyên tố có cấu hình electron thỏa mãn 2 điều kiện :
+ Lớp ngoài cùng có 8e.
+ Lớp ngoài cùng chứa số e tối đa.
Trong những nguyên tố có số hiệu nguyên tử từ Z = 1 đến Z = 36, chỉ có nguyên tố neon là có cấu hình electron thoả mãn 2 điều kiện của đề bài.
Ne : 1 s 2 2 s 2 2 p 6
Các nguyên tố khác :
He : bên ngoài chỉ có 2e.
Ar : 2/8/8 lớp ngoài cùng có 8e, nhưng lớp thứ 3 chưa đủ số e tối đa.
Kr : 2/8/18/8 lớp ngoài cùng có 8e, nhưng lớp thứ 4 chưa đủ số e tối đa.
Đúng 0
Bình luận (0)
Cho biết sự phân bố electron theo lớp của các nguyên tử H, He, Li như sau:
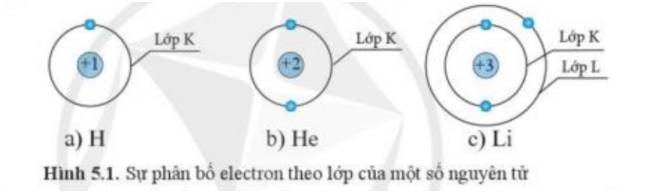
Dựa vào hình 5.1, hãy cho biết số electron tối đa ở lớp K của các nguyên tử có số hiệu nguyên tử Z $ \geqslant $ 2 là bao nhiêu. Theo em, thứ tự phân bố electron vào lớp vỏ nguyên tử như thế nào?
Dựa vào hình 5.1 số electron tối đa ở lớp K của các nguyên tử có số hiệu nguyên tử Z ≥ 2 là 2.
Các electron sẽ được phân bố lần lượt vào các lớp theo chiều từ gần hạt nhân ra ngoài. Mỗi lớp có số electron đối đa xác định, như lớp thứ nhất có tối đa 2 electron, lớp thứ 2 có tối đa 8 electron,…
Đúng 0
Bình luận (0)
1 viết kí hiệu nguyên tử của các nguyên tố có Z lần lượt là 2,4,8,11,21
2 viết cấu hình e của các nguyên tố có Z lần lượt là 8,11,20,15
-cho bt số lớp và số phân lớp e của chúng
Xác định số hiệu nguyên tử trong các trường hợp sau:
a) Nguyên tử X có tổng các electron p là 9.
b) Nguyên tử Y có 4 lớp electron, lớp ngoài cùng có 4 electron
c) Nguyên tử Z có tổng số electron s là 5.
Nguyên tử của nguyên tố Z có 4 lớp electron, lớp ngoài cùng có 6 electron. Số hiệu nguyên tử của Z là
A. 24
B. 34
C. 36
D. 16
Nguyên tử của nguyên tố Z có 4 lớp electron, lớp ngoài cùng có 6 electron. Số hiệu nguyên tử của Z là:
A. 24
B. 34
C. 36
D. 16
Đáp án B
Cấu hình electron của Z là: 1s22s22p63s23p63d104s24p4
Số hiệu nguyên tử của Z là 34
Đúng 0
Bình luận (0)
Cấu hình electron và xác định số hiệu nguyên tử của các nguyên tố sau a) X có tổng số electron trên phân lớp p là 8 b) Y có 2 lớp electron và có 5 electron ở ngoài lớp cùng c) Z có 7 electron thuộc phân lớp S
hãy xác định vị trí trong hệ thống tuần hoàn (số thứ tự, chu kỳ, nhóm)cho các nguyên tố sau
a. Be(Z=4); Al(Z=13); Fe(Z=26)
b. nguên tố Y có tổng số e của các phân lớp p là 11
c.Nguyên tử của nguyên tố R có 3e ở phân lớp 3d
Na(Z=11) 1s2 2s2 2p6 3s1 thuộc ô thứ 11, chu kì 3, nhóm IA
Al(Z=13) 1s2 2s2 2p6 3s2 3p1 thuộc ô thứ 13, chu kì 3, nhóm IIIA
S(Z=16) 1s2 2s2 2p6 3s2 3p4 thuộc ô thứ 16, chu kì 3
Nhóm VIA
Cl(Z=17) 1s2 2s2 2p6 3s2 3p5 thuộc ô thứ 17, chu kì 3,
Nhóm VIIA
Đúng 0
Bình luận (1)




















