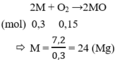đốt cháy hoàn toàn 4,8 gam kim loại A có hóa trị II cần 4,48 lít khí oxi (ở đktc). A là kim loại nào sau đây?

Những câu hỏi liên quan
Đốt cháy hoàn toàn 22,4 g kim loại X có hóa trị II cần dùng hết 4,48 lít khí oxi ở đktc. Xác định tên kim loại X
Số mol của khí oxi ở dktc
nO2 = \(\dfrac{V_{O2}}{22,4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Pt : 2X + O2 → 2XO\(|\)
2 1 2
0,4 0,2
Số mol của kim loại X
nX = \(\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
⇒ MX = \(\dfrac{m_X}{n_X}=\dfrac{22,4}{0,4}=56\) (dvc)
Vậy kim loại x là Fe
Chúc bạn học tốt
Đúng 1
Bình luận (0)
đốt cháy hoàn toàn một kim loại A có hóa trị II cần vừa đủ 2.24 lít khí oxi ở đktc. Sau phản ứng thu được 6.72g Oxit. xác định kim loại A
\(n_{O_2} = \dfrac{2,24}{22,4} = 0,1(mol)\\ 2A + O_2 \xrightarrow{t^o} 2AO\\ n_{Oxit} = 2n_{O_2} = 0,2(mol)\\ \Rightarrow M_{Oxit}= A + 16 = \dfrac{6,72}{0,2}=\dfrac{168}{5}\\ \Rightarrow A = 17,6\)
(Sai đề)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 7,2 gam một kim loại có hóa trị II cần dùng hết 3,36 lít oxi (đktc). Kim loại đó là
A. Zn
B. Cu
C. Fe
D. Mg
Đốt cháy hoàn toàn 4,8 gam kim loại R có hóa trị II bằng khí oxi dư, thu được 8 gam oxit. Kim loại R là
A. Sr
B. Mg
C. Ca
D. Zn
Đốt cháy hoàn toàn 1,08 gam bột nhôm.
a. Tính thể tích khí oxi cần dùng (đktc).
b. Lượng khí oxi đã phản ứng ở trên vừa đủ tác dụng với 3,84 gam một kim loại A có hóa trị II. Xác định kim loại A.
4Al+3O2-to>2Al2O3
0,04---0,03------0,02 mol
n Al=\(\dfrac{1,08}{27}\)=0,04 mol
=>VO2=0,03.22,4=0,672l
b)
2A+O2-to>2AO
0,06--0,03 mol
=>\(\dfrac{3,84}{A}=0,06\)
=>A=64 :=>Al là Đồng
Đúng 2
Bình luận (2)
Đốt cháy hoàn toàn 18,4 gam 1 kim loại A (I) cần dùng hết 4,48 lít khí Oxi (đktc) thu được sản phẩm là AO . Kim loại A là
\(4A+O_2-^{t^o}\rightarrow2A_2O\\ n_A=4n_{O_2}=0,8\left(mol\right)\\ \Rightarrow M_A=\dfrac{18,4}{0,8}=23\left(Na\right)\)
Đúng 1
Bình luận (0)
Câu 36. Khi phân hủy có xúc tác 14,7 gam KClO3, thể tích khí oxi thu được làA. 4,032 lít. B. 8,064 lít. C. 7,092 lít. D. 12, 096 lít.Câu 37. Đốt cháy hoàn toàn 4,6 gam một kim loại M hóa trị I cần sử dụng hết 1,12 lít khí O2 ở đktc. Kim loại M là A. Na. B. K. C. Ca. D. Ba.Cây 38. Cho 8,5 gam oxit kim loại hóa trị II tác dụng vừa đủ với 2,24 khí hidro ở đktc. CTHH của oxit kim loại là A. CuO B. ZnO C. FeO D. MgOCâu 39. Trong các phát biểu sau, phát biểu nào là sai?A. Oxi tan nhiều trong nước. B....
Đọc tiếp
Câu 36. Khi phân hủy có xúc tác 14,7 gam KClO3, thể tích khí oxi thu được là
A. 4,032 lít. B. 8,064 lít. C. 7,092 lít. D. 12, 096 lít.
Câu 37. Đốt cháy hoàn toàn 4,6 gam một kim loại M hóa trị I cần sử dụng hết 1,12 lít khí O2 ở đktc. Kim loại M là
A. Na. B. K. C. Ca. D. Ba.
Cây 38. Cho 8,5 gam oxit kim loại hóa trị II tác dụng vừa đủ với 2,24 khí hidro ở đktc. CTHH của oxit kim loại là
A. CuO B. ZnO C. FeO D. MgO
Câu 39. Trong các phát biểu sau, phát biểu nào là sai?
A. Oxi tan nhiều trong nước. B. Oxi nặng hơn không khí.
C. Oxi chiếm 1/5 thể tích không khí. D. Oxi là chất khí không màu, không mùi, không vị.
Câu 40. Khi đưa que đóm tàn đỏ vào miện ống nghiệm chứ oxi có hiện tượng gì xảy ra?
A. Tàn đóm bùng cháy. B. Tàn đóm tắt dần.
C. Tàn đóm tắt ngay. D. Không có hiện tượng gì.
nhiệt phân hoàn toàn 94,8 gam KMnO4 sau phản ứng thấy thoát ra V (lít) khí oxi (đktc)
a) Viết PTHH của phản ứng trên và giá trị của V
b) để đốt cháy hoàn toàn 5,76 gam kim loại R (có hóa trị II) cần dùng 40% lượng oxi sinh ra từ phản ứng trên. Hãy xác định kim loại R
nKMnO4=94,8:158=0,6(mol)
PTHH: 2KMnO4-t--> K2MnO4+MnO2+O2
0,6----------------------------------->0,3(mol)
=>V= VO2=0,3. 22,4= 6,72(l)
b ) 40%nO2 =40%.0,3=0,12(mol)
2R + O2 -t--->2RO
0,24(mol)<- 0,12
=> M(Khối lượng Mol ) R= m:n=5,76:0,24=24(G/MOL)
=> R là Mg
Đúng 2
Bình luận (1)
a)-\(n_{KMnO_4}=\dfrac{m}{M}=\dfrac{94,8}{158}=0,6\left(mol\right)\)
-PTHH: \(2KMnO_4\rightarrow^{t^0}K_2MnO_4+MnO_2+O_2\uparrow\)
2 1
0,6 0,3
\(\Rightarrow V_{O_2\left(đktc\right)}=n.22,4=0,3.22,4=6,72\left(l\right)\)
b)-\(V_{O_2\left(cd\right)}=6,72.\dfrac{40}{100}=2,688\left(l\right)\)
\(\Rightarrow n_{O_2}=\dfrac{V}{22,4}=\dfrac{2,688}{22,4}=0,12\left(mol\right)\)
-PTHH: \(2R+O_2\rightarrow^{t^0}2RO\)
2 1
0,24 0,12
\(m_R=n.M=5,76\left(g\right)\)
\(\Rightarrow0,24.M_R=5,76\)
\(\Rightarrow M_R=24\) (g/mol)
-Vậy R là Crom
Đúng 0
Bình luận (2)
Đốt cháy hoàn toàn 8,1 gam của một kim loại A hóa trị III cần dùng hết 5,04 lít khí Oxi ( đktc) ở nhiệt độ cao thu được một Oxit. Kim loại A là
A. Fe B. Al C. Cr D. Kết quả khác.
Đốt cháy hoàn toàn 8,1 gam của một kim loại A hóa trị III cần dùng hết 5,04 lít khí Oxi ( đktc) ở nhiệt độ cao thu được một Oxit. Kim loại A là
A. Fe B. Al C. Cr D. Kết quả khác.
Đúng 1
Bình luận (0)
Xem thêm câu trả lời