GIÚP MIK VỚI Ạ!! MIK ĐANG CẦN GẤP!
cho 14,7g hỗn hợp Na và k tác dụng hoàn toàn với nước sau phản ứng cho thấy thoát ra 5,6 lít H2. Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu?
Cho 8,25 gam hỗn hợp kim loại Mg và Fe tác dụng hết với dung dịch HCL,thấy thoát ra 5,6 lít khí H2 (đktc)
a) Viết PTHH của phản ứng hoá học xảy ra
b) Tính khối lượng và thành phần phần trăm về khối lượng của mỗi kim loại trong hỗn hợp ban đầu
a. PTHH:
Fe + 2HCl ---> FeCl2 + H2 (1)
Mg + 2HCl ---> MgCl2 + H2 (2)
b. Gọi x, y lần lượt là số mol của Fe và Mg
Ta có: \(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Theo PT(1): \(n_{H_2}=n_{Fe}=x\left(mol\right)\)
Theo PT(2): \(n_{H_2}=n_{Mg}=y\left(mol\right)\)
\(\Rightarrow x+y=0,25\) (*)
Theo đề, ta lại có: 56x + 24y = 8,25 (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}x+y=0,25\\56x+24y=8,25\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x\approx0,07\\y\approx0,18\end{matrix}\right.\)
=> \(m_{Fe}=0,07.56=3,92\left(g\right)\)
=> \(\%_{m_{Fe}}=\dfrac{3,92}{8,25}.100\%=47,52\%\)
\(\%_{m_{Mg}}=100\%-47,52\%=52,48\%\)
Cho 10,1 gam hỗn hợp Na, K tác dụng với nước dư, sau phản ứng thu được 3,36 lít khí H2 (đktc). (a) Viết phương trình phản ứng xảy ra. (b) Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu
\(n_{H2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
a) Pt : \(2Na+2H_2O\rightarrow2NaOH+H_2|\)
2 2 2 1
a 0,5a
\(2K+2H_2O\rightarrow2KOH+H_2|\)
2 2 2 1
b 0,5b
b) Gọi a là số mol của Na
b là số mol của K
\(m_{Na}+m_K=10,1\left(g\right)\)
⇒ \(n_{Na}.M_{Na}+n_K.M_K=10,1g\)
⇒ 23a + 39b = 10,1g (1)
Theo phương trình : 0,5a + 0,5b = 0,15(2)
Từ(1),(2), ta có hệ phương trình :
23a + 39b = 10,1g
0,5a + 0,5b = 0,15
⇒ \(\left\{{}\begin{matrix}a=0,1\\b=0,2\end{matrix}\right.\)
\(m_{Na}=0,1.23=2,3\left(g\right)\)
\(m_K=0,2.39=7,8\left(g\right)\)
0/0Na = \(\dfrac{2,3.100}{10,1}=22,77\)0/0
0/0K = \(\dfrac{7,8.100}{10,1}=77,23\)0/0
Cho 11,2 lít H2 (dktc) tác dụng vừa đủ với hỗn hợp A gồm Fe3O4 và CuO . sau phản ứng thu được 23,2 g hỗn hợp 2 kim loại .tính phần trăm khối lượng của mỗi oxit trong hỗn hợp ban đầu?
lm nhanh giúp mik vs ạ
Fe3O4+4H2-to>3Fe+4H2O
x---------\(\dfrac{3}{4}x\)
CuO+H2-to>Cu+H2O
y--------y mol
Ta có :
\(\left\{{}\begin{matrix}x+y=0,5\\\dfrac{3}{4}x.56+64y=23,2\end{matrix}\right.\)
=>x=0,4 mol, y=0,1 mol
=>% m Fe3O4=\(\dfrac{0,4.232}{0,4.232+0,1.80}.100\)=92,1%
=>%m CuO=100-92,1=7,9%
\(n_{H_2}=\dfrac{11,2}{22,4}=0,5mol\)
\(Fe_3O_4+4H_2\rightarrow3Fe+4H_2O\)
x 4x 3x
\(CuO+H_2\rightarrow Cu+H_2O\)
y y y
\(\Rightarrow\left\{{}\begin{matrix}4x+y=0,5\\3\cdot56x+64y=23,2\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
\(\%m_{Fe_2O_3}=\dfrac{0,1\cdot232}{0,1\cdot232+0,1\cdot80}\cdot100\%=74,36\%\)
\(\%m_{CuO}=100\%-74,36\%=25,64\%\)
Cho 27,6 gam hỗn hợp 2 kim loại Mg và Ag tác dụng với dung dịch HCl vừa đủ, sau phản ứng thấy thoát ra 5,6 lít khí ở đktc. Thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp ban đầu lần lượt là:
A. 21,74% và 78,26%
B. 78,26% và 21,74%
C. 88, 04% và 11,96%
D. 11,96% và 88, 04%
Đáp án A
Cho Mg và Ag tác dụng với HCl chỉ có Mg phản ứng.
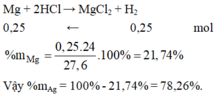
Cho 25 (gam) hỗn hợp gồm Nhôm và Đồng vào dung dịch H2SO4 loãng dư, sau phản ứng thấy thoát ra 5,6 (lít) khí H2 (ở đktc). Tính khối lượng mỗi kim loại có trong hỗn hợp ban đầu.
nH2 = 5.6/22.4 = 0.25 (mol)
2Al + 3H2SO4 => Al2(SO4)3 + 3H2
1/6............................................0.25
mAl = 1/6 * 27 = 4.5 (g)
mCu = 25 - 4.5 = 20.5 (g)
Cho 14,3 gam hỗn hợp gồm Na, Zn vào cốc chứa lượng dư nước. Sau khi phản ứng xảy ra hoàn toàn thu được 2,24 lít khí H2 (đktc). Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu.
Gọi số mol Na, Zn là a, b
=> 23a + 65b = 14,3
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
- Nếu Zn tan hết
PTHH: 2Na + 2H2O --> 2NaOH + H2
______a-------------------->a---->0,5a
2NaOH + Zn --> Na2ZnO2 + H2
__2b<----b-------------------->b
=> \(\left\{{}\begin{matrix}2b\le a\\0,5a+b=14,3\end{matrix}\right.\) => Loại
=> Zn không tan hết => NaOH hết
PTHH: 2Na + 2H2O --> 2NaOH + H2
______a------------------->a---->0,5a
2NaOH + Zn --> Na2ZnO2 + H2
_a--------------------------->0,5a
=> 0,5a + 0,5a = 0,1
=> a = 0,1
=> mNa = 0,1.23 = 2,3 (g)
=> mZn = 14,3 - 2,3 = 12(g)
Cho 26,7 g hỗn hợp gồm Phenol và Metanol tác dụng kim loại Na thấy thoát ra 3,92 lít khí H2 (đkc).Tính khối lượng mỗi chất trong hỗn hợp đầu.
\(Đặt:n_{C_6H_5OH}=a\left(mol\right);n_{CH_3OH}=b\left(mol\right)\left(a,b>0\right)\\ C_6H_5OH+Na\rightarrow C_6H_5ONa+\dfrac{1}{2}H_2\\ CH_3OH+Na\rightarrow CH_3ONa+\dfrac{1}{2}H_2\\ \Rightarrow\left\{{}\begin{matrix}94a+32b=26,7\\22,4.0,5a+22,4.0,5b=3,92\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,25\\b=0,1\end{matrix}\right.\\ \Rightarrow m_{CH_3OH}=0,1.32=3,2\left(g\right)\\ \Rightarrow m_{C_6H_5OH}=94.0,25=23,5\left(g\right)\)
: Cho 2,06 gam hỗn hợp 2 kim loại Na và Ba tác dụng với một lượng nước dư, thấy thoát ra 0,56 lít khí H2 (đktc).
a) Tính tổng khối lượng bazơ sinh ra.
b) Tính khối lượng từng kim loại trong hỗn hợp.
2Na+2H2O->2NaOH+H2
x-------------------x----------0,5x mol
Ba+2H2O->Ba(OH)2+H2
y---------------------y----------y mol
aTa có :)\(\left\{{}\begin{matrix}23x+137y=2,06\\0,5x+y=0,025\end{matrix}\right.\)
=>\(\left\{{}\begin{matrix}x=0,03\\y=0,01\end{matrix}\right.\)
=>mbazo=0,03.40+0,01.171=2,91g
=>m Na=0,03.23=0,69g
=>m Ba=0,01.137=1,27g
Câu 3 : Cho 11,9 gam hỗn hợp gồm 2 kim loại Zn và Al tác dụng với dd HCl dư thấy thoát ra 9,916 lít khí H2 (đkc). a) Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu. b) Tính khối lượng muối tạo thành. c) Tính khối lượng dung dịch HCl 10% cần dùng
a, Ta có: 65nZn + 27nAl = 11,9 (1)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Theo PT: \(n_{H_2}=n_{Zn}+\dfrac{3}{2}n_{Al}=\dfrac{9,916}{24,79}=0,4\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Zn}=0,1\left(mol\right)\\n_{Al}=0,2\left(mol\right)\end{matrix}\right.\)
⇒ mZn = 0,1.65 = 6,5 (g)
mAl = 0,2.27 = 5,4 (g)
b, Theo PT: nZnCl2 = nZn = 0,1 (mol)
nAlCl3 = nAl = 0,2 (mol)
⇒ m muối = 0,1.136 + 0,2.133,5 = 40,3 (g)
c, Theo PT: nHCl = 2nH2 = 0,8 (mol)
\(\Rightarrow m_{ddHCl}=\dfrac{0,8.36,5}{10\%}=292\left(g\right)\)