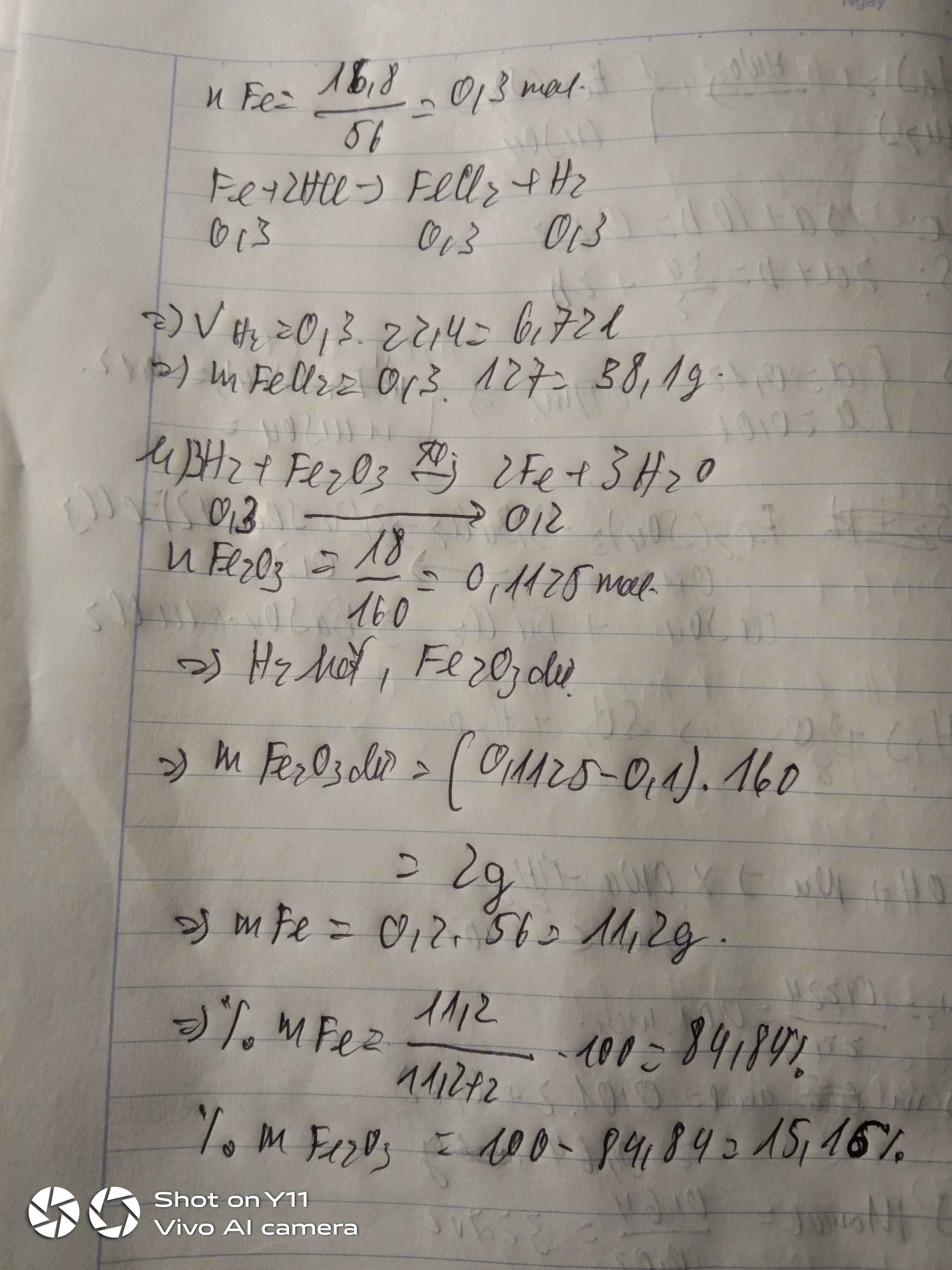cho 13g kém vào dung dịch HCL đến phản ứng hàn toàn thu được FeCl2 và khí H2/
a) Viết phương trình phản ứng
b)Tính khối lượng muối FeCl2 thu được
c)Dẫn Toàn bộ khí H2 tren qua bình đựng bột đồng(II) oxi đun nóng,Tính khối lượng đồng thu được sau phản yuwngs
Giúp Mình với MN ơi
Mai mình ktra rồi
CẢM ƠN MN