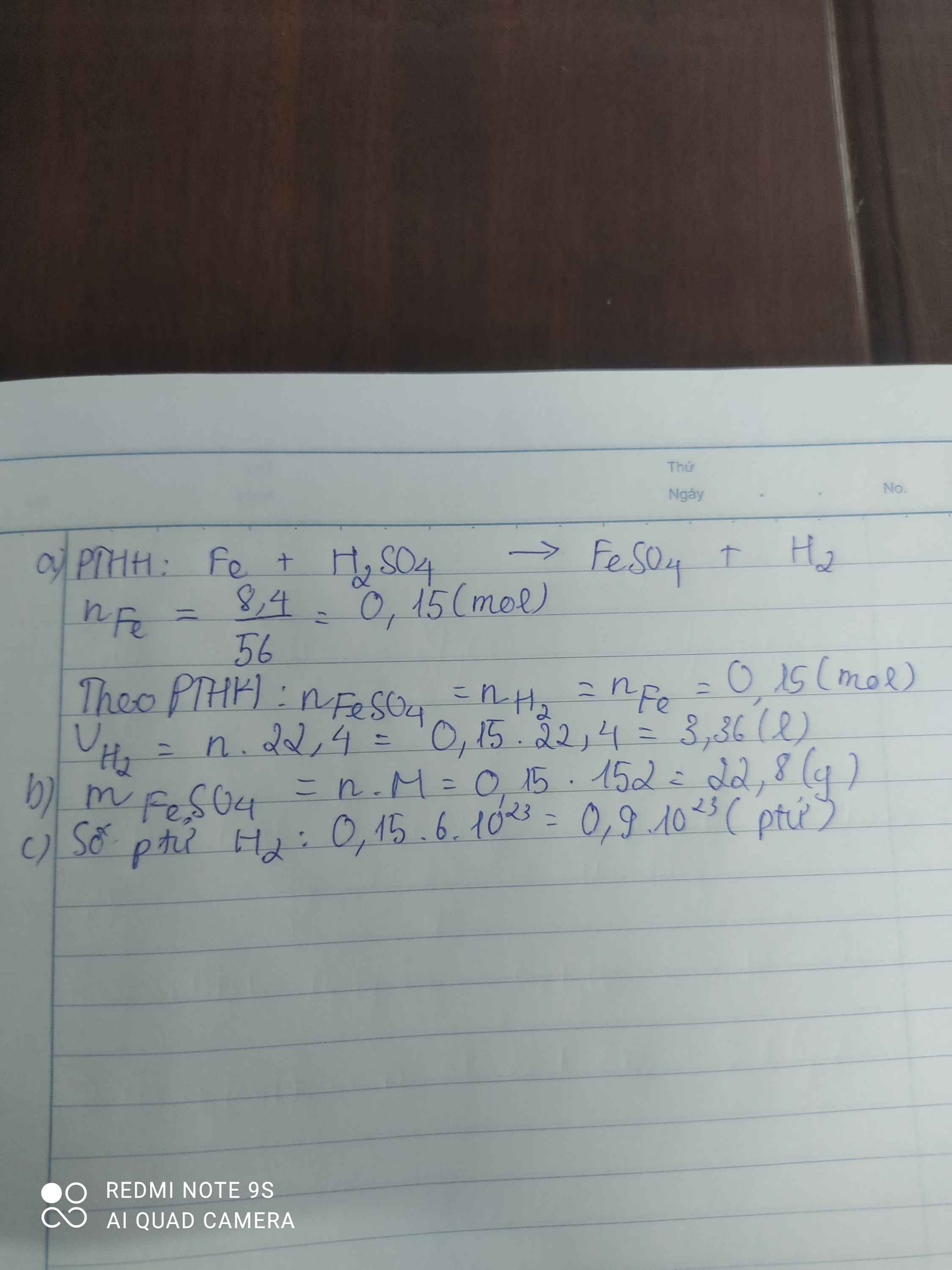mang 46,4g Fe3o4 tác dụng với h2 taoh thành fe và h2o a, tính thể tích h2 ở đktc b, tính khối lượng fe tạo thành

Những câu hỏi liên quan
khử 4,64g fe3o4 ở nhiệt độ cao bằng 8,96 lit h2 ở đktc.
b tính khối lượng các chất sau phản ứng.
c toàn bộ lượng fe tạo thành cho tác dụng với 0,5 mol hcl. tính thể tích khí h2 thu được ở đktc
\(n_{Fe_3O_4}=\dfrac{4,64}{232}=0,02mol\)
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4mol\)
\(Fe_3O_4+4H_2\rightarrow3Fe+4H_2O\)
0,02 0,4 0 0
0,02 0,08 0,06 0,08
0 0,32 0,06 0,08
b)\(m_{Fe}=0,06\cdot56=3,36g\)
\(m_{H_2O}=0,08\cdot18=1,44g\)
c)\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,06 0,5 0 0
\(\Rightarrow\)Tính theo \(Fe\)
\(\Rightarrow V_{H_2}=0,06\cdot22,4=1,344l\)
Đúng 2
Bình luận (0)
cho 5,6 gam sắt (Fe) tác dụng hết với dung dịch HCl, tạo thành muối sắt (II) clorua (FeCl2) và khí hidro (H2)
a. Viết phương trình phản ứng?
b. Tính thể tích khí Hidro (H2) sinh ra ở (đktc)?
c. Tính khối lượng muối FeCl2 tạo thành ?
\(a.Fe+2HCl\rightarrow FeCl_2+H_2\\b.n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\\ n_{H_2}=n_{Fe}=0,1\left(mol\right)\\ \Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\\ c.n_{FeCl_2}=n_{Fe}=0,1\left(mol\right)\\ m_{FeCl_2}=0,1.127=12,7\left(g\right) \)
Đúng 2
Bình luận (0)
CHO 37,2G HỖ HỢP gồm Zn và Fe tác dụng với dung dịch H2SO4 loãng thu đc 13,44l H2 (ĐKTC)
a.Viết pthh?
b.Tính khối lượng mỗi kim loại trong hỗ hợp
c.Cho toàn bộ H2 ở trên tác dụng với 46,4g Fe3O4.Tính khối lượng các chất sau pư
a: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
b: Đặt \(a=n_{Zn};b=n_{Fe}\)
Theo đề, ta có hệ phương trình:
\(\left\{{}\begin{matrix}65a+56b=37.2\\a+b=0.6\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0.4\\b=0.2\end{matrix}\right.\)
\(m_{Zn}=0.4\cdot65=25\left(g\right)\)
\(m_{Fe}=0.5\cdot56=11.2\left(g\right)\)
Đúng 1
Bình luận (0)
cho 56 gram Fe tác dụng hết với Fe + HCL-->FCL2+H2 a) tính khối lượng Iron(II)chloride(FeCL2) tạo thành b)tính thể tích của Hydrogen(H2) thu đc ở 25 độ C 1 Bar
nFe=56/56=1(mol)
Fe+HCl=>FeCl2+H2
a, Theo PTPƯ: nFeCl2=nFe=1(mol)
=>mFeCl2=1.127=127(g)
b,theo ptpu ta có nH2=nFe=0,1(mol)
=>vH2(đktc)=1.22,4=22,4l
VH2(đkc)=1.24,79=24,79l
ko bt tính 25 độ 1 bar
Đúng 0
Bình luận (0)
\(a)n_{Fe}=\dfrac{56}{56}=1mol\\ Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{FeCl_2}=n_{H_2}=n_{Fe}=1mol\\ m_{FeCl_2}=1.127=127g\\ b)V_{H_2}=1.24,79=24,79l\)
Đúng 0
Bình luận (0)
Cho 60,5 g hh 2 kl zn và fe tác dụng hết với dd axit hcl. thành phần % khối lượng của fe trong hh kl là 46,289%. tính:
a) khối lượng mỗi kl trong hh
b) thể tích khí h2 ở đktc thu được
c) khối lượng của các muối tạo thành
Khối lượng sắt:mFe=0,46298*60,5=28 g=>mZn=32,5g
=>nFe=0,5;nZn=0,5
ta có:nCl- =2nFe+2nZn=2 mol =>nHCl=2mol
=>nH2 =1mol.=>V H2=44,8 lit
m muối =m kim loại +m Cl- =60,5 +2*35,5=131,5
Đúng 0
Bình luận (0)
Cho 5,6g Fe tác dụng với dung dịch H2SO4 tạo ra muối Fe(SO4) và khí H2 a) tính thể tích h2 sinh ra (ở đktc) b) tính khối lượng muối thu được c) dùng toàn bộ khí sinh ra tác dụng với 12g CuO.tính khối lượng kim loại sinh ra * em cần gấp ạ 12h em đi thi r
Số mol của 5,6 g Fe:
\(n_{Fe}=\dfrac{m}{M}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
1 :1 : 1 : 1
0,1-> 0,1 : 0,1 : 0,1(mol)
a) thể tích của 0,1 mol H2:
\(V_{H_2}=n.22,4=0,1.22,4=2,24\left(l\right)\)
b) khối lượng 0,1 mol FeSO4:
\(m_{FeSO_4}=n.M=0,1.152=15,2\left(g\right)\)
c) PTHH: \(H_2+CuO\underrightarrow{t^o}Cu+H_2O\)
1 : 1 : 1 : 1
0,1 -> 0,1 : 0,1 : 0,1(mol)
khối lượng 0,1 mol Cu:
\(m_{Cu}=n.M=0,1.64=6,4\left(g\right)\)
Đúng 2
Bình luận (0)
a) Ta sử dụng định luật Avogadro để tính thể tích H2 sinh ra:
1 mol khí ở đktc có thể tích là 22,4 LTính số mol H2 sinh ra:Fe + H2SO4 → FeSO4 + H2
Fe + H2SO4 → FeSO4 + H2
Số mol H2 = số mol Fe = m/FeMM = 5,6/56 = 0,1 molThể tích H2 ở đktc = số mol H2 x 22,4 L/mol = 0,1 x 22,4 = 2,24 L
Vậy thể tích H2 sinh ra là 2,24 L (ở đktc).
b) Tính khối lượng muối thu được:
Viết phương trình phản ứng:Fe + H2SO4 → FeSO4 + H2Tính số mol FeSO4 thu được:
Fe : FeSO4 = 1 : 1
n(FeSO4) = n(Fe) = 0,1 molTính khối lượng muối thu được:
m(FeSO4) = n(FeSO4) x M(FeSO4) = 0,1 x (56 + 32x4) = 27,2 g
Vậy khối lượng muối thu được là 27,2 g.
c) Dùng toàn bộ H2 sinh ra tác dụng với CuO, ta có phương trình phản ứng:
CuO + H2 → Cu + H2O
n(CuO) = m/M = 12/64 = 0,1875 molTính số mol H2 cần dùng:
Theo phương trình phản ứng ta biết: 1 mol CuO cần 1 mol H2
n(H2) = n(CuO) = 0,1875 molTính khối lượng Cu sinh ra:
Theo phương trình phản ứng ta biết: 1 mol Cu cần 1 mol H2
m(Cu) = n(Cu) x M(Cu) = 0,1875 x 63,5 = 11,90625 g
Vậy khối lượng kim loại Cu sinh ra là 11,90625 g.
Đúng 0
Bình luận (0)
\(a)n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\\ Fe+H_2SO_4\xrightarrow[]{}FeSO_4+H_2\\ \Rightarrow n_{Fe}=n_{H_2}=n_{FeSO_4}=0,1mol\\ V_{H_2}=0,1.22,4=2,24\left(l\right)\\ b)m_{FeSO_4}=0,1.152=15,2\left(g\right)\\ c)n_{CuO}=\dfrac{12}{80}=0,15\left(mol\right)\\ CuO+H_2\xrightarrow[]{t^0}Cu+H_2\)
Theo pt: \(\dfrac{0,15}{1}>\dfrac{0,1}{1}\Rightarrow Cu\) \(dư\)
\(CuO+H_2\xrightarrow[]{t^0}Cu+H_2O\\ \Rightarrow n_{H_2}=n_{Cu}=0,1mol\\ m_{Cu}=0,1.64=6,4\left(g\right)\)
Đúng 0
Bình luận (0)
cho 5,6g kim loại sắt tác dụng hết với dung dịch axit clohidric HCI theo phương trình: Fe + HCI ---> FeCI2 + H2. a) Lập phương trình hoá học của phản ứng trên. b) Tính khối lượng sắt ( II) clorua FeCI2 tạo thành. c) Tính thể tích khí H2 sinh ( ở đktc )
Giúp mình với 🥺🥺🥺
Fe+2HCl->FeCl2+H2
0,1--0,2-----0,1-----0,1
nFe=0,1 mol
=>mFeCl2=0,1.127=12,7g
=>VH2=0,1.22,4=2,24l
Đúng 0
Bình luận (0)
Cho 100ml dung dịch HCL 1M tác dụng hết với kim loại Fe tạo thành muối Sắt (II) clorua (FeCl2) và giải phóng khí Hidro
a,Viết PTHH xảy ra
b,Tính khối lượng muối thu được
c,Tính thể tích của H2 thu được ở đktc
(Biết các khí được đo ở đktc:Cl = 35,5; Fe = 56; H = 1 )
\(n_{HCl}=0,1mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 0,2 0,1 0,1
\(m_{FeCl_2}=0,1\cdot127=12,7g\)
\(V_{H_2}=0,1\cdot22,4=2,24l\)
Đúng 5
Bình luận (0)
Cho 8,4gam sắt tác dụng với dung dịch axit sunfurie H2SO4 loãng, theo phương trình phàn ứng sau: Fe + H2SO4 ——> FeSO4 + H2 a) Tính thể tích khí hiđrô thoát ra ở đktc b) Tính khối lượng FeSO4 sinh ra c) Tính số phân tử khí hiđrô tạo thành
a.
n Fe=28562856=0,5 (mol)
Fe+H2SO4→FeSO4+H2↑
0,5→0,5 0,5 0,5 (mol)
b.
V H2(đktc)=0,5.22,4=11,2 (l)
c.
m HCl=0,5.36,5=18,25 (g)
d.
m FeSO4=0,5.152=76 (g)
Đúng 0
Bình luận (1)