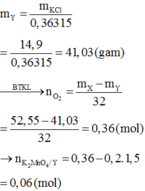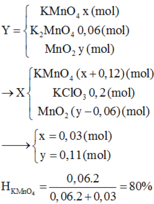Nung 31,6 gam KMnO4 ( hiệu suất 50%) thu được oxi cho tác dụng hoàn toàn với 24,8 gam P. Tìm khối lượng P2O5 thu được?

Những câu hỏi liên quan
Nung 31,6 gam KMnO4 ( hiệu suất 50%) thu được oxi cho tác dụng hoàn toàn với 24,8 gam P. Tìm khối lượng P2O5 thu được?
PTHH: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
Ta có: \(\left\{{}\begin{matrix}n_{O_2}=\dfrac{1}{2}\cdot\dfrac{31,6}{158}\cdot50\%=0,05\left(mol\right)\\n_P=\dfrac{24,8}{31}=0,8\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,8}{4}>\dfrac{0,05}{5}\) \(\Rightarrow\) Photpho còn dư, Oxi p/ứ hết
\(\Rightarrow n_{P_2O_5}=0,02\left(mol\right)\) \(\Rightarrow m_{P_2O_5}=0,02\cdot142=2,84\left(g\right)\)
Đúng 1
Bình luận (0)
PT: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
Ta có: \(n_{KMnO_4}=\dfrac{31,6}{158}=0,2\left(mol\right)\)
Theo PT: \(n_{O_2\left(LT\right)}=\dfrac{1}{2}n_{KMnO_4}=0,1\left(mol\right)\)
Mà: H% = 50%
\(\Rightarrow n_{O_2\left(TT\right)}=0,1.50\%=0,05\left(mol\right)\)
Ta có: \(n_P=\dfrac{24,8}{31}=0,8\left(mol\right)\)
PT: \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
Xét tỉ lệ: \(\dfrac{0,8}{4}>\dfrac{0,05}{5}\), ta được P dư.
Theo PT: \(n_{P_2O_5}=\dfrac{2}{5}n_{O_2}=0,02\left(mol\right)\)
\(\Rightarrow m_{P_2O_5}=0,02.142=2,84\left(g\right)\)
Bạn tham khảo nhé!
Đúng 1
Bình luận (0)
\(KMnO_4--t^o->K_2MnO_4+MnO_2+O_2\)
158 32
31,6 \(x\)
Với \(H=50\%\) \(\Rightarrow x=\dfrac{31,6.32}{158}.50\%=3,2\left(g\right)\)
\(4P+5O_2--t^o->2P_2O_5\)
124 160
\(y\) 3,2
\(\Rightarrow y=\dfrac{124.3,2}{160}=2,48\left(g\right)\)
Đúng 0
Bình luận (0)
Nung 24,5gam KClO3 ( hiệu suất 50%) thu được oxi cho tác dụng hoàn toàn với 2,7 gam Al. Tìm khối lượng Al2O3 thu được?
\(m_{KClO_3\left(pư\right)}=24.5\cdot0.5=12.25\left(g\right)\)
\(n_{KClO_3}=\dfrac{12.25}{122.5}=0.1\left(mol\right)\)
\(n_{Al}=\dfrac{2.7}{27}=0.1\left(mol\right)\)
\(2KClO_3\underrightarrow{t^0}2KCl+3O_2\)
\(0.1...........................0.15\)
\(4Al+3O_2\underrightarrow{t^0}2Al_2O_3\)
\(4............3\)
\(0.1..........0.15\)
\(LTL:\dfrac{0.1}{4}< \dfrac{0.15}{3}\Rightarrow O_2dư\)
\(m_{Al_2O_3}=0.05\cdot102=5.1\left(g\right)\)
Đúng 0
Bình luận (0)
Nhiệt phân hoàn toàn 31,6 gam KMnO4 thu được chất rắn A gồm K2MnO4, MnO2 và khí O2. Lượng khí O2 thu được cho tác dụng với 11,2 gam sắt thu được chất rắn B. Tính khối lượng của chất rắn A và chất rắn B
Đọc tiếp
Nhiệt phân hoàn toàn 31,6 gam KMnO4 thu được chất rắn A gồm K2MnO4, MnO2 và khí O2. Lượng khí O2 thu được cho tác dụng với 11,2 gam sắt thu được chất rắn B. Tính khối lượng của chất rắn A và chất rắn B
Ta có: \(n_{KMnO_4}=\dfrac{31,6}{158}=0,2\left(mol\right)\)
PT: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
Theo PT: \(n_{K_2MnO_4}=n_{MnO_2}=n_{O_2}=\dfrac{1}{2}n_{KMnO_4}=0,1\left(mol\right)\)
\(\Rightarrow m_A=m_{K_2MnO_4}+m_{MnO_2}=0,1.197+0,1.87=28,4\left(g\right)\)
Ta có: \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
PT: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
Xét tỉ lệ: \(\dfrac{0,2}{3}>\dfrac{0,1}{2}\), ta được Fe dư.
Chất rắn B gồm: Fe3O4 và Fe dư.
⇒ mB = mFe3O4 + mFe (dư) = mFe + mO2 = 11,2 + 0,1.32 = 14,4 (g)
Đúng 2
Bình luận (0)
nung 15.8 gam kmno4 đến khi phản ứng xảy ra hoàn toàn
a,tính thể tích oxi thu được đktc
b.nếu đem toàn bộ lượng oxi trên tác dụng với 6.2 gam photpho thì chất nào dư khối lượng bao nhiêu'?
\(n_{KMnO_4}=\dfrac{15.8}{158}=0.1\left(mol\right)\)
\(2KMnO_4\underrightarrow{t^0}K_2MnO_4+MnO_2+O_2\)
\(n_{O_2}=\dfrac{0.1}{2}=0.05\left(mol\right)\)
\(V_{O_2}=0.05\cdot22.4=1.12\left(l\right)\)
\(b.\)
\(n_P=\dfrac{6.2}{31}=0.2\left(mol\right)\)
\(4P+5O_2\underrightarrow{t^0}2P_2O_5\)
\(4.........5\)
\(0.2........0.05\)
\(LTL:\dfrac{0.2}{4}>\dfrac{0.05}{5}\Rightarrow Pdư\)
\(m_{P\left(dư\right)}=\left(0.2-0.04\right)\cdot31=4.96\left(g\right)\)
Đúng 1
Bình luận (0)
PTHH:2KMnO4--- K2MnO4+MnO2 +O2
ADCT nKmno4=15,8/158=0,1 mol
a, theo pt có nO2/nKmno4= 1/2
nO2=0,05 mol
ADCT V=n*22,4
VO2=0,05*22,4 =1,12 l
b, PTHH: 5O2+4P---2P2O5
ADCTnP=6,2/31=0,2 mol
Theo pt
nO2/5=0,01 bé hơn nP/4=0,05
P dư
theo pt nP(pư)/nO2=4/5
nP(p/ư)=0,04 mol
nP(dư)=0,05-0,04 =0,01 mol
ADCT:m=n*M
mP(dư)=0,01*31=0,31g
Đúng 0
Bình luận (0)
giúp mình với :
Phân hủy hoàn toàn 31,6 gam KMnO4 ở nhiệt độ cao
a. tính Vo2 thu đc ở đktc
b. tính Klg oxit sắt từ ( Fe3O4) tạo thành khi cho toàn bộ lượng khí oxi thu được ở phản ứng trên tác dụng với 11,2 gam sắt. Biết phản ứng xảy ra hoàn toàn.
giúp mik câu b đi lm ơn
a)\(n_{KMnO_4}=\dfrac{31,6}{158}=0,2\left(m\right)\)
\(PTHH:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
tỉ lệ :2 1 1 1
số mol :0,2 0,1 0,1 0,1
\(V_{O_2}=0,1.22,4=2,24\left(l\right)\)
b)\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(m\right)\)
\(PTHH:3Fe+2O_2\underrightarrow{ }Fe_3O_4\)
theo phương trình ta có tỉ lệ\(\dfrac{0,2}{3}>\dfrac{0,1}{2}\)=>Fe dư
\(PTHH:3Fe+2O_2\xrightarrow[]{}Fe_3O_4\)
tỉ lệ :3 2 1
số mol :0,15 0,1 0,05
\(m_{Fe_3O_4}=0,05.232=11,6\left(g\right)\)
Đúng 3
Bình luận (2)
Trộn KMnO4, KClO3 với một lượng bột MnO2 trong bình kín thu được hỗn hợp rắn X. Lấy 52,55 gam X đem nung nóng, sau một thời gian thu được hỗn hợp rắn Y (trong đó có 0,2 mol KCl và KCl chiếm 36,315% khối lượng) và V lít O2. Biết rằng KClO3 nhiệt phân hoàn toàn. Sau đó, cho toàn bộ Y tác dụng hoàn toàn với HCl đặc, dư, đun nóng, sau phản ứng cô cạn dung dịch thu được 51,275 gam hỗn hợp muối khan. Hiệu suất quá trình nhiệt phân KMnO4 là A. 62,5% B. 91,5% C. 75,0% D. 80,0%
Đọc tiếp
Trộn KMnO4, KClO3 với một lượng bột MnO2 trong bình kín thu được hỗn hợp rắn X. Lấy 52,55 gam X đem nung nóng, sau một thời gian thu được hỗn hợp rắn Y (trong đó có 0,2 mol KCl và KCl chiếm 36,315% khối lượng) và V lít O2. Biết rằng KClO3 nhiệt phân hoàn toàn. Sau đó, cho toàn bộ Y tác dụng hoàn toàn với HCl đặc, dư, đun nóng, sau phản ứng cô cạn dung dịch thu được 51,275 gam hỗn hợp muối khan. Hiệu suất quá trình nhiệt phân KMnO4 là
A. 62,5%
B. 91,5%
C. 75,0%
D. 80,0%
Nhiệt phân hoàn toàn 31,6 gam KMnO4 thu được khí O2 toàn bộ lượng khí O2 tác dụng với lưu huỳnh thu được khí SO2. Toàn bộ khí SO2 cho qua 100 ml dung dịch NaOH a M thì thu được dung dịch X có chứa 11,72 gam muối. Giá trị a là A. 1 B. 1,4 C. 1,2 D. 1,6
Đọc tiếp
Nhiệt phân hoàn toàn 31,6 gam KMnO4 thu được khí O2 toàn bộ lượng khí O2 tác dụng với lưu huỳnh thu được khí SO2. Toàn bộ khí SO2 cho qua 100 ml dung dịch NaOH a M thì thu được dung dịch X có chứa 11,72 gam muối. Giá trị a là
A. 1
B. 1,4
C. 1,2
D. 1,6
Đáp án : D
2KMnO4 -> K2MnO4 + MnO2 + O2
S + O2 -> SO2
SO2 + 2NaOH -> Na2SO3 + H2O
SO2 + NaOH -> NaHSO3
Ta có : nSO2 = nO2 = ½ nKMnO4 = 0,1 mol
Xét muối thu được gồm x mol Na2SO3 và y mol NaHSO3
=> bảo toàn S : nSO2 = x + y = 0,1
Và mmuối = 126x + 104y = 11,72g
=> x = 0,06 ; y = 0,04 mol
=> nNaOH = 2nNa2SO3 + nNaHSO3 ( bảo toàn Na) = 0,16 mol
=> a = 1,6M
Đúng 0
Bình luận (0)
Khi phân hủy có xúc tác 122,5g Kaliclorat (KClO3) thể tích khí oxi (đktc) thu được là :
A. 48 lít
B. 24,5 lít
C. 67,2 lít
D. 33,6 lít
Nhiệt phân hoàn toàn 31,6 gam KMnO4, thu được V lít O2 (đktc), biết hiệu suất phản ứng 80% . Giá trị của V là
A. 2,24
B. 1,792
C. 10,08
D. 8,96
Xem thêm câu trả lời
Hỗn hợp X gồm 31,6 gam KMnO4 và 73,5 gam KClO3. Nung nóng X trong bình kín một thời gian thu được khí O2 và 93,9 gam hỗn hợp rắn Y gồm KMnO4, K2MnO4, MnO2, KClO3 và KCl. Cho Y tác dụng hoàn toàn với dung dịch axit clohidric 36,50%, đun nóng (khối lượng riêng là 1,18 g/ml). Thể tích dung dịch HCl cần dùng (vừa đủ) gần nhất với giá trị nào sau đây? A. 271 ml B. 300 ml C. 322 ml D. 383 ml
Đọc tiếp
Hỗn hợp X gồm 31,6 gam KMnO4 và 73,5 gam KClO3. Nung nóng X trong bình kín một thời gian thu được khí O2 và 93,9 gam hỗn hợp rắn Y gồm KMnO4, K2MnO4, MnO2, KClO3 và KCl. Cho Y tác dụng hoàn toàn với dung dịch axit clohidric 36,50%, đun nóng (khối lượng riêng là 1,18 g/ml). Thể tích dung dịch HCl cần dùng (vừa đủ) gần nhất với giá trị nào sau đây?
A. 271 ml
B. 300 ml
C. 322 ml
D. 383 ml