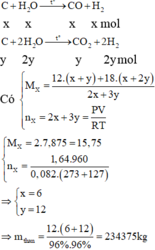đốt cháy 4g bột than (chứa C và tạp chất rắn trơ ko cháy ) thu đc 6,72 lít khí CO2 ở đktc.tính độ tinh khiết của than

Những câu hỏi liên quan
Câu 1.Đốt cháy hoàn toàn 2 gam một mẩu than có lẫn tạp chất, thu được 3,36 lít khí CO2 ở đktc. Thành phần % theo khối lượng của cacbon có trong mẩu than là bao nhiêu?
Câu 2.Cần dùng bao nhiêu gam Al tác dụng với dung dịch HCl, thì thu được 6,72 lít khí hiđro (đktc)?
Câu 1:
\(n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: C + O2 --to--> CO2
0,15<-----------0,15
=> \(\%C=\dfrac{0,15.12}{2}.100\%=90\%\)
Câu 2:
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,2<-------------------0,3
=> mAl = 0,2.27 = 5,4 (g)
Đúng 3
Bình luận (0)
Câu 1.
\(n_{CO_2}=\dfrac{3,36}{22,4}=0,15mol\)
\(C+O_2\underrightarrow{t^o}CO_2\)
0,15 0,15
\(m_C=0,15\cdot12=1,8g\)
\(\%C=\dfrac{1,8}{2}\cdot100\%=90\%\)
Câu 2.
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
0,2 0,3
\(m_{Al}=0,2\cdot27=5,4g\)
Đúng 1
Bình luận (0)
nung hoàn toàn 20,2g KNO3 a) tính khối lượng chất rắn cồn lại b) dùng toàn bộ lượng khí O2 thu được để đốt cháy hoàn toàn m g một loại than chứa 92% cacbon , 4% khối lượng lưa huỳnh còn lại là tạp chất trơ . tính giá trị của m . tính thể tích khí CO2 và SO2 sinh ra
nKNO3 = 0.2 (mol)
2KNO3 -to-> 2KNO2 + O2
0.2__________0.2____0.1
mKNO2 = 0.2*85=17(g)
C + O2 -to-> CO2
x___x
S + O2 -to-> SO2
y___y
x + y = 0.1 (1)
Mặt khác :
+) 32y/m * 100% = 4%
=> 32y = 0.04m (2)
+) 12x/m = 0.92
=> 12x = 0.92m (3)
(1) , (2) , (3) :
x = 0.1
y = 0.002
m = 1.3
VCO2 + VSO2 = ( 0.1 + 0.002) * 22.4 = 2.2848 (l)
Đúng 1
Bình luận (0)
đốt cháy hoàn toàn 10 kg than đá chứa 10% tạp chất khác ko cháy được , còn lại là cacbon . tính thể tích khí co2 tạo thàn ở đktc
\(n_C = \dfrac{10(100\%-10\%)}{12} = 0,75(kmol)\\ C + O_2 \xrightarrow{t^o} CO_2\\ n_{CO_2} = n_C = 0,75(kmol) = 750(mol)\\ V_{CO_2} = 750.22,4 = 16800(lít)\)
Đúng 2
Bình luận (0)
Cho hơi nước qua than nung đỏ, sau khi làm khô hết hơi nước thu được hỗn hợp khí X (gồm CO, H2 và CO2) có tỉ khối của X so với H2 bằng 7,875. Cần bao nhiêu kg than có chứa 4% tạp chất trơ để thu được 960 m3 hỗn hợp khí X trên đo ở 1,64 atm và
127
o
C
, biết rằng có 96% cacbon bị đốt cháy? A. 225,000 kg B. 156,250 kg C. 216,000 kg D. 234,375 kg
Đọc tiếp
Cho hơi nước qua than nung đỏ, sau khi làm khô hết hơi nước thu được hỗn hợp khí X (gồm CO, H2 và CO2) có tỉ khối của X so với H2 bằng 7,875. Cần bao nhiêu kg than có chứa 4% tạp chất trơ để thu được 960 m3 hỗn hợp khí X trên đo ở 1,64 atm và 127 o C , biết rằng có 96% cacbon bị đốt cháy?
A. 225,000 kg
B. 156,250 kg
C. 216,000 kg
D. 234,375 kg
Cho hơi nước qua than nung đỏ, sau khi làm khô hết hơi nước thu được hỗn hợp khí X (gồm CO, H2 và CO2) có tỉ khối của X so với H2 bằng 7,875. Cần bao nhiêu kg than có chứa 4% tạp chất trơ để thu được 960 m3 hỗn hợp khí X trên đo ở 1,64 atm và 127oC, biết rằng có 96% cacbon bị đốt cháy A. 225,000 kg B. 156,250 kg C. 216,000 kg D. 234,375 kg
Đọc tiếp
Cho hơi nước qua than nung đỏ, sau khi làm khô hết hơi nước thu được hỗn hợp khí X (gồm CO, H2 và CO2) có tỉ khối của X so với H2 bằng 7,875. Cần bao nhiêu kg than có chứa 4% tạp chất trơ để thu được 960 m3 hỗn hợp khí X trên đo ở 1,64 atm và 127oC, biết rằng có 96% cacbon bị đốt cháy
A. 225,000 kg
B. 156,250 kg
C. 216,000 kg
D. 234,375 kg
ĐÁP ÁN D
M = 15,75; nX = 48 kmol;
C + H2O -> CO + H2 C + 2H2O -> CO2 + 2H2
x--------------x------x y----------------y------2y kmol
Hỗn hợp X gồm x mol CO ; (x + 2y) mol H2 ; y mol CO2
Ta có : nX = 2x + 3y = 48; mX = 30x + 48y =756;
=> x = 6 ; y = 12;
=> m =18.12/(0,96.0,96) = 234,375 kg
Đúng 0
Bình luận (0)
Đốt cháy hết m gam một mẫu than (chứa 4% tạp chất trơ còn lại là cacbon) bởi V lít khí oxi thu được 2,24 lít hỗn hợp chất khí X ở điều kiện tiêu chuẩn sục khí X vào dung dịch nước vôi trong dư thấy tạo thành 8 gam kết tủa tính giả sử N và V biết thể tích các khí ở ở điều kiện tiêu chuẩn
Xem chi tiết
X gồm O2 dư và CO2
CO2+ Ca(OH)2 -> CaCO3+ H2O
nCaCO3= nCO2= 0,08 mol
nX= 0,1 mol
=> nO2 dư= 0,02 mol
C+ O2 ⟶ CO2
=> nC= nO2 phản ứng= nCO2= 0,08 mol
Tổng nO2= 0,08+0,02= 0,1 mol
=> V= 2,24l
mC= 0,08.12= 0,96g
Than chứa 96% C nên lượng than đem đốt là 0,96:96%= 1g
Pt thứ 2 có nhiệt độ nha bn:)
Đúng 1
Bình luận (0)
\(n_{CaCO_3}=n_{CO_2}=\dfrac{8}{100}=0.08\left(mol\right)\)
\(n_{CO}=n_X-n_{CO_2}=0.1-0.08=0.02\left(mol\right)\)
\(2C+O_2\underrightarrow{t^0}2CO\)
\(C+O_2\underrightarrow{t^0}CO_2\)
\(V_{O_2}=\left(\dfrac{0.02}{2}+0.08\right)\cdot22.4=2.016\left(l\right)\)
\(m_C=\left(0.01+0.08\right)\cdot\dfrac{12}{0.96}=1.125\left(g\right)\)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 24kg than đá có chứa 0,5% tạp chất lưu huỳnh và 1,5% tạp chất khác không cháy được. Tính thể tích khí CO2 và SO2 tạo thành (ở điều kiện tiêu chuẩn).
Đổi: 24kg = 24000g
24kg than đá có chứa 0,5% tạp chất lưu huỳnh và 1,5% tạp chất khác không cháy được

⇒ nS = 120 / 32 = 3,75 mol
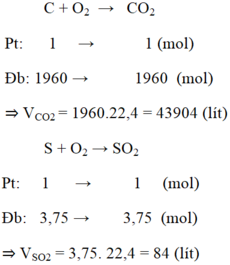
Đúng 1
Bình luận (0)
Thể tích khí oxi (ở đktc) cần dùng để đốt cháy hoàn toàn 5 kg than có chứa 4% tạp chất không cháy làA. 8,96 m3. B. 4,48 m3. C. 9,33 m3. D. 6,72 m3.
Đọc tiếp
Thể tích khí oxi (ở đktc) cần dùng để đốt cháy hoàn toàn 5 kg than có chứa 4% tạp chất không cháy là
A. 8,96 m3. B. 4,48 m3. C. 9,33 m3. D. 6,72 m3.
Khối lượng cacbon có trong 5kg than trên là :
\(m_C=\dfrac{5.\left(100-4\right)}{100}=4,8kg=4800g\)
\(\rightarrow n_C=4800:12=400mol\)
\(C+O_2\rightarrow CO_2\)
400 400 mol
\(\Rightarrow V_{O2}=400.22,4=8960\) lít = 8,96 \(m^3\)
\(\Rightarrow\) Chọn A
Đúng 2
Bình luận (0)
Bài 5 (SGK trang 84): Đốt cháy hoàn toàn 24kg than đá có chứa 0,5% tạp chất lưu huỳnh và 1,5% tạp chất khác không cháy được. Tính thể tích khí CO2 và SO2 ( ở điều kiện tiêu chuẩn ).
PT: \(C+O_2\underrightarrow{t^o}CO_2\) (1)
\(S+O_2\underrightarrow{t^o}SO_2\) (2)
Ta có: mS = 24.0,5% = 0,12 (kg) = 120 (g) ⇒ nS = 120/32 = 3,75 (mol)
Theo PT (2): \(n_{SO_2}=n_S=3,75\left(mol\right)\)
\(\Rightarrow V_{SO_2}=3,75.22,4=84\left(l\right)\)
Ta có: mC = 24 - 0,12 - 24.1,5% = 23,52 (kg) = 23520 (g)
\(\Rightarrow n_C=\dfrac{23520}{12}=1960\left(mol\right)\)
Theo PT (1): \(n_{CO_2}=n_C=1960\left(mol\right)\)
\(\Rightarrow V_{CO_2}=1960.22,4=43904\left(l\right)\)
Đúng 1
Bình luận (0)