Nêu thành phần thể tích của các chất trong không khí.

Những câu hỏi liên quan
Cho biết thành phần phần trăm thể tích các khí trong không khí ? Nêu vai trò của không
khí đối với sự sống ? Nêu các nguyên nhân gây ô nhiễm không khí ? Ô nhiễm không khí có tác
hại gì đối với đời sống ? Em có thể làm gì đề góp phần làm giảm ô nhiễm không khí ?
Hãy cho biết thành phần trăm theo thể tích các chất khí có trong không khí
Em tham khảo:
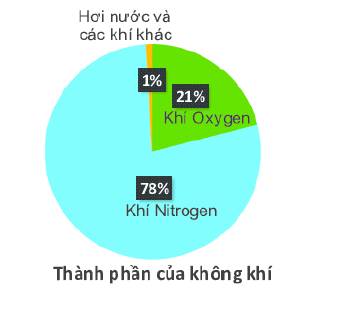
Trong không khí Nito chiếm 78%, Oxi chiếm 21%, còn 1% là các khí khác ( Hơi nước , khí hiếm, cacbon điôxit)
Đúng 0
Bình luận (0)
(Thành phần các chất trong không khí)
Không khí xung quanh ta gồm nhiều chất khí khác nhau. Trong điều kiện thông thường, khí oxygen chiếm khoảng 21% thể tích không khí. Hỏi có bao nhiêu mét khối oxygen trong một căn phòng có thể tích 70,2 \({m^3}\)?
Số mét khối oxygen trong một căn phòng có thể tích 70,2 \({m^3}\) là:
\(70,2.\dfrac{{21}}{{100}} = 14,742\left( {{m^3}} \right)\)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 15,6 gam hỗn hợp gồm Mg và Ag trong không khí thu được 18,8 g hỗn hợp chất rắn.
a) viết PTHH xảy ra
b) tính thể tích không khí cần dùng ở đktc biết rằng thể tích oxi chiếm 20% thể tích không khí
c) tính thành phần phần trăm các kim loại trong hỗn hợp ban đầu
Xem chi tiết
a. Ag không phản ứng nên ta có PTHH: \(2Mg+O_2\rightarrow^{t^o}2MgO\)
\(\rightarrow m_{O_2}=m_{hh}-m_{\mu\text{ối}}=18,8-15,6=3,2g\)
\(\rightarrow n_{O_2}=\frac{3,2}{32}=0,1mol\)
b. \(\rightarrow V_{O_2}=n.22,4=22,4.0,1=2,24l\)
\(\rightarrow V_{kk}=4,48.5=11,2l\)
c. Có \(n_{Mg}=2n_{O_2}=0,2l\)
\(\rightarrow m_{Mg}=0,2.24=4,8g\)
\(\rightarrow\%m_{Mg}=\frac{4,8.100}{15,6}\approx30,77\%\)
\(\rightarrow\%m_{Ag}=100\%-30,77\%=69,23\%\)
1. Phân biệt vật thể, chất.2. Tính chất vật lí, tính chất hóa học của chất,sự chuyển thể của chất.3. Tính chất của oxygen.4. Thành phần của không khí.5. Nguyên nhân gây ô nhiễm không khí .6. Đơn vị và dụng cụ đo chiều dài. Nêu các bước cần thực hiện khi đo chiều dài của một vật.7. Giới hạn đo (GHĐ) và độ chia nhỏ nhất (ĐCNN) của một dụng cụ đo gì?8. Đơn vị và dụng cụ đo khối lượng. Nêu các bước cần thực hiện khi đo khối lượng của một vật.9. Đơn vị và dụng cụ đo thời gian . Nêu các bước cần th...
Đọc tiếp
1. Phân biệt vật thể, chất.
2. Tính chất vật lí, tính chất hóa học của chất,sự chuyển thể của chất.
3. Tính chất của oxygen.
4. Thành phần của không khí.
5. Nguyên nhân gây ô nhiễm không khí .
6. Đơn vị và dụng cụ đo chiều dài. Nêu các bước cần thực hiện khi đo chiều dài của một vật.
7. Giới hạn đo (GHĐ) và độ chia nhỏ nhất (ĐCNN) của một dụng cụ đo gì?
8. Đơn vị và dụng cụ đo khối lượng. Nêu các bước cần thực hiện khi đo khối lượng của một vật.
9. Đơn vị và dụng cụ đo thời gian . Nêu các bước cần thực hiện khi đo thời gian của một hoạt động.
10. Nhiệt độ là gì? Nêu đơn vị và dụng cụ dùng để đo nhiệt độ.
Câu 1:“Vật chất” và “vật thể” là hai khái niệm khác nhau. Vật thể là một vật có đặc tính vật lý và chỉ định một dạng hình thể cụ thể ví dụ: Viên kim cương. Vật thể là những dạng vật chất cụ thể cảm tính.
Đúng 1
Bình luận (0)
Câu 2: Tính chất vật lý là tính chất có thể đo được mà không làm thay đổi thành phần hóa học của vật chất. Những tính chất này có thể được sử dụng để mô tả sự xuất hiện và kích thước của vật chất.
Câu 3: Oxygen ở thể khí, không màu, không mùi, không vị, ít tan trong nước và nặng hơn không khí. - Oxygen hóa lỏng ở -183oC, hóa rắn ở -218oC. Ở thể lỏng và rắn, oxygen có màu xanh nhạt.
Đúng 0
Bình luận (0)
Nung m gam hỗn hợp X gồm FeS và
FeS
2
trong một bình kín chứa không khí (gồm 20% thể tích
O
2
và 80% thể tích
N
2
) đến khi các phản ứng xảy ra hoàn toàn, thu được một chất rắn duy nhất và hỗn hợp khí Y có thành phần thể tích: 84,8%
N
2
, 14%
SO
2
, còn lại là ...
Đọc tiếp
Nung m gam hỗn hợp X gồm FeS và FeS 2 trong một bình kín chứa không khí (gồm 20% thể tích O 2 và 80% thể tích N 2 ) đến khi các phản ứng xảy ra hoàn toàn, thu được một chất rắn duy nhất và hỗn hợp khí Y có thành phần thể tích: 84,8% N 2 , 14% SO 2 , còn lại là O 2 . Thành phần phần trăm khối lượng của FeS trong hỗn hợp X là
A. 42,31%
B. 59,46%
C. 19,64%
D. 26,83%
Chọn C
N 2 : 0 , 848 m o l S O 2 : 0 , 14 m o l O 2 d u : 1 − 0 , 848 − 0 , 14 = 0 , 012 m o l → K h ô n g k h í N 2 : 0 , 848 m o l O 2 : 0 , 212 m o l
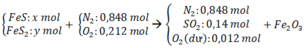
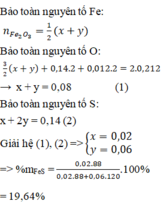
Đúng 2
Bình luận (0)
Đối cháy 24,8 gam phốt pho bằng 67,2 lít không khí ở điều kiện tiêu chuẩn (không khí có chứa 20% khí oxy và 80% khí nitơ về thể tích). a) Tính khối lượng sản phẩm tạo thành? b) Tính thành phần phần trăm về khối lượng các chất có trong hỗn hợp sau phản ứng? Biết rằng khí nitơ không cháy.
$\rm a)n_{kk} = \dfrac{67,2}{22,4} = 3 (mol)$
$\rm \Rightarrow n_{O_2} = 20\%.3 = 0,6 (mol)$
$\rm n_P = \dfrac{24,8}{31} = 0,8 (mol)$
PTHH: \(\rm 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5 \)
Ban đầu: 0,8 0,6
Pư: 0,48<--0,6
Sau pư: 0,32 0 0,24
$\rm \Rightarrow m_{\text{sản phẩm tạo thành}} = m_{P_2O_5(sinh.ra)} = 0,24.142 = 34,08 (g)$
$\m b) m_{hh} = m_{P(dư)} + m_{P_2O_5} = 0,32.31 + 34,08 = 44 (g)$
$\rm \Rightarrow \%m_P = \dfrac{0,32.31}{44} .100\% = 22,545\%$
$\rm \Rightarrow \%m_{P_2O_5} = 100\% - 22,545\% = 77,455\%$
Đúng 2
Bình luận (0)
\(n_P=\dfrac{24,8}{31}=0,8\left(mol\right)\)
Thể tích Oxi trong 67,2 lít không khí :
67,2 x 20% = 13,44(l)
\(n_{O_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH :
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
Trc p/ư: 0,8 0,6 (mol)
p/ư 0,48 0,6 0,24
Sau p/ư: 0,32 0 0,24
=> Sau p/ư P dư
Khối lượng sản phẩm tạo thành :
\(m_{P_2O_5}=0,24.142=34,08\left(g\right)\)
Khối lượng P trong hỗn hợp :
\(m_{P\left(P_2O_5\right)}=0,48.31=14,88\left(g\right)\)
Thành phần % của P :
\(14,88:34,08=43,66\%\)
Đúng 1
Bình luận (0)
Trình bày thí nghiệm xác định thành phần phần trăm về thể tích của oxygen trong không khí. Nêu hiện tượng xảy ra trong thí nghiệm. Giải thích và kết luận.
Giúp tôi nhanh với
Từ câu trên, thể tích oxi có trong bình đúng bằng thể tích của mực nước dâng lên chiếm 1/5 chiều cao bình
=> oxi trong không khí chiếm khoảng 20% khá tương tương với tỉ lệ oxi xuất hiện trong biểu đồ là 21%
xin like
Đúng 1
Bình luận (0)
: Đốt cháy 2,24 lit khí metan trong 28 lit không khí tạo ra khí cacbonic và hơi nước . Hỏi sau phản ứng có những chất nào và thành phần % thể tích là bao nhiêu? Các khí đo ở đktc. Biết trong không khí có 80% N2 và 20% O2.
\(n_{metan}=\dfrac{2,24}{22,4}=0,1mol\)
\(V_{kk}=28l\Rightarrow V_{O_2}=\dfrac{28}{5}=5,6l\Rightarrow n_{O_2}=0,25mol\)
\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
0,1 0,25 0 0
0,1 0,2 0,1 0,2
0 0,15 0,1 0,2
Sau phản ứng oxi còn dư và \(V_{CO_2}=0,1\cdot22,4=2,24l\)
\(V_{ddCO_2}=2,24+28-0,2\cdot22,4=25,76l\)
\(\%V=\dfrac{2,24}{25,76}\cdot100\%=8,7\%\)
Đúng 5
Bình luận (2)
























