
Những câu hỏi liên quan
Cho 1,37g hỗn hợp X gồm Fe và kim loại M hoá trị không đổi tác dụng với dung dịch HCl dư thấy giải phóng 1,232 lít khí H2 (đkc). Mặt khác hỗn hợp X trên tác dụng vừa đủ với lượng khí Cl2 điều chế được bằng cách cho 3,792 gam KMnO4 tác dụng với dung dịch HCl đặc dư. Tỉ lệ số mol của Fe và M trong hỗn hợp là 1: 3. Kim loại M là A. Mg B. Cu C. Al D. Zn
Đọc tiếp
Cho 1,37g hỗn hợp X gồm Fe và kim loại M hoá trị không đổi tác dụng với dung dịch HCl dư thấy giải phóng 1,232 lít khí H2 (đkc). Mặt khác hỗn hợp X trên tác dụng vừa đủ với lượng khí Cl2 điều chế được bằng cách cho 3,792 gam KMnO4 tác dụng với dung dịch HCl đặc dư. Tỉ lệ số mol của Fe và M trong hỗn hợp là 1: 3. Kim loại M là
A. Mg
B. Cu
C. Al
D. Zn
Đáp án : C
X + HCl : Fe -> Fe2+ có nH2 = 0,055 mol
X + Cl2 : Fe -> Fe3+
bảo toàn e : 5nKMnO4 = 2nCl2 => nCl2 = 0,06 mol
Do M có hóa trị không đổi => nFe = ne (2) – ne (1) = 2nCl2 – 2nH2 = 0,01 mol
Giả sử M có hóa trị n => n.nM + 2.0,01 = 2nH2 => n.nM = 0,09 mol
Có : mX = 1,37g = 0,01.56 + nM.M => nM.M = 0,81g
=> M = 9n
Nếu n = 3 => M = 27g (Al) Thỏa mãn
Đúng 0
Bình luận (0)
cho 13 g kim loại hoá trị 2 tác dụng vừa đủ với 0,4 mol HCl dư sinh ra 4,48 lít khí ở đktc tìm kim loại
\(n_{H_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(A+2HCl\rightarrow ACl_2+H_2\)
\(0.2..............................0.2\)
\(M_A=\dfrac{13}{0.2}=65\left(\dfrac{g}{mol}\right)\)
\(A:Zn\)
Đúng 2
Bình luận (0)
Cho 1,37 gam hỗn hợp X gồm Fe và kim loại M hoá trị không đổi tác dụng với dung dịch HCl dư thấy giải phóng 1,232 lít khí H2 (đktc). Mặt khác hỗn hợp X trên tác dụng vừa đủ với lượng khí Cl2 điều chế được bằng cách cho 3,792 gam KMnO4 tác dụng với dung dịch HCl đặc dư. Tỉ lệ số mol của Fe và M trong hỗn hợp là 1: 3. Kim loại M là A. Mg B. Cu. C. Al D. Zn.
Đọc tiếp
Cho 1,37 gam hỗn hợp X gồm Fe và kim loại M hoá trị không đổi tác dụng với dung dịch HCl dư thấy giải phóng 1,232 lít khí H2 (đktc). Mặt khác hỗn hợp X trên tác dụng vừa đủ với lượng khí Cl2 điều chế được bằng cách cho 3,792 gam KMnO4 tác dụng với dung dịch HCl đặc dư. Tỉ lệ số mol của Fe và M trong hỗn hợp là 1: 3. Kim loại M là
A. Mg
B. Cu.
C. Al
D. Zn.
Số OXH của Fe sau khi tác dụng với dung dịch HCl là +2 còn sau khi td với Cl2 là +3
TN1
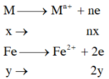
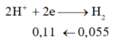
=> nx+2y=0,11 (1)
TN2: Xét cả quá trình
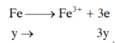
=> nx+3y=0,12 (2)
(1)-(2) được y=0,01
Thay y=0,01 vào (2) được nx=0,09(3)
Lại có: 56.0,01+ xM=1,37
=> Mx=0,81 (4)
(3)(4)=> M=9n
=> Kim loại là Al
Đáp án C
Đúng 0
Bình luận (0)
Câu 1 Cho 4,8 gam kim loại M tác dụng với 0,1 mol Cl2 thu được hỗn hợp chất rắn X. Cho X vào dung dịch HCl dư thu được 2,24 lít H2 (đktc) và dung dịch Y. Tính khối lượng muối trong Y và xác định tên kim loại M.Câu 2 Cho hỗn hợp m gam Fe và Cu gam Fe vào dung dịch H2SO4 loãng (dư), thu được 5,6 lít khí H2 (đktc). Cũng cho hỗn hợp trên vào dung dịch H2SO4 đặc, nóng (dư) thu đươc 11,2 lít SO2 (sản phẩm khử duy nhất, đktc). Tính m.
Đọc tiếp
Câu 1 Cho 4,8 gam kim loại M tác dụng với 0,1 mol Cl2 thu được hỗn hợp chất rắn X. Cho X vào dung dịch HCl dư thu được 2,24 lít H2 (đktc) và dung dịch Y. Tính khối lượng muối trong Y và xác định tên kim loại M.
Câu 2 Cho hỗn hợp m gam Fe và Cu gam Fe vào dung dịch H2SO4 loãng (dư), thu được 5,6 lít khí H2 (đktc). Cũng cho hỗn hợp trên vào dung dịch H2SO4 đặc, nóng (dư) thu đươc 11,2 lít SO2 (sản phẩm khử duy nhất, đktc). Tính m.
Mọi người giúp em 2 bài này với ạ, em đang cần gấpBài 1: Cho m gam kim loại Al tác dụng hết với 400ml dung dịch HCl(vừa đủ) thu được 13,44 lít khí H2 (đktc) và dung dịch X.a. Tính giá trị của m?b.Tính nồng độ mol/l của dung duchj HCl đã dùng?c. Tính nồng độ mol/l của dung dịch X?Bài 2: Cho 13 gam kim loại M tác dụng hét với dung dịch H2SO4 loãng, dư thu được 4,48 lít khí H2 (đktc). Xác định M?Em xin cảm ơn ạ !!!!
Đọc tiếp
Mọi người giúp em 2 bài này với ạ, em đang cần gấp
Bài 1: Cho m gam kim loại Al tác dụng hết với 400ml dung dịch HCl(vừa đủ) thu được 13,44 lít khí H2 (đktc) và dung dịch X.
a. Tính giá trị của m?
b.Tính nồng độ mol/l của dung duchj HCl đã dùng?
c. Tính nồng độ mol/l của dung dịch X?
Bài 2: Cho 13 gam kim loại M tác dụng hét với dung dịch H2SO4 loãng, dư thu được 4,48 lít khí H2 (đktc). Xác định M?
Em xin cảm ơn ạ !!!!
nH2=13,14:22,4=0,6 mol
PTHH: 2Al+6HCl=>2Al2Cl3+3H2
0,4<-1,2<----0,4<-----0,6
=> Al=0,4.27=10,8g
CMHCL=1,2:0,4=3M
CM Al2Cl3=0,4:0,4=1M
bài 2: nH2=0,2mol
PTHH: 2A+xH2SO4=> A2(SO4)x+xH2
0,4:x<---------------------------0,2
ta có PT: \(\frac{13}{A}=\frac{0,4}{x}\)<=> 13x=0,4A
=> A=32,5x
ta lập bảng xét
x=1=> A=32,5 loiaj
x=2=> A=65 nhận
x=3=> A=97,5 loại
=> A là kẽm (Zn)
Đúng 0
Bình luận (0)
3 kim loại X, Y, Z có tỉ lệ khối lượng mol lần lượt là 3:5:7, tỉ lệ số mol là 4:2:1. Cho 1,16g ba kim loại này tác dụng với HCl dư thì có có 0,784 lít ( đktc) khí H2 thoát ra. Xác định X, Y, Z biết khi tác dụng với HCl đều cho muối hóa trị 2. Giúp mik bài này bằng cách áp dụng t/c dãy tỉ số bằng nhau với, cảm ơn nhiều ạ:v
Gọi X, Y, Z là nguyên tử khối của X, Y, Z
x, y, z là số mol của X, Y, Z
Theo đề có: \(X:Y:Z=3:5:7\Rightarrow Y=\dfrac{5}{3}X;Z=\dfrac{7}{3}X\)
\(x:y:z=4:2:1\Rightarrow y=\dfrac{1}{2}x;z=\dfrac{1}{4}x\)
Mặt khác:
\(m_{hh}=Xx+Yy+Zz=1,16\\ \Leftrightarrow Xx+\dfrac{5}{3}X.\dfrac{1}{2}x+\dfrac{7}{3}X.\dfrac{1}{4}x=1,16\\ \Rightarrow Xx=0,48\)
Vì khi cho X, Y, Z tác dụng với HCl đều cho muối hóa trị 2 nên X, Y, Z là kim loại hóa trị 2.
Phản ứng:
\(X+2HCl\rightarrow XCl_2+H_2\)
x --------------------------> x
\(Y+2HCl\rightarrow YCl_2+H_2\)
y -------------------------> y
\(Z+2HCl\rightarrow ZCl_2+H_2\)
z -------------------------> z
\(n_{H_2}=x+y+z=\dfrac{0,784}{22,4}=0,035\left(mol\right)\)
\(\Leftrightarrow x+\dfrac{1}{2}x+\dfrac{1}{4}x=0,035\Rightarrow x=0,02\)
\(\Rightarrow X=\dfrac{0,48}{0,02}=24\left(Mg\right)\)
\(\Rightarrow\left\{{}\begin{matrix}Y=\dfrac{5}{3}X=\dfrac{5}{3}.24=40\left(Ca\right)\\Z=\dfrac{7}{3}X=\dfrac{7}{3}.24=56\left(Fe\right)\end{matrix}\right.\)
Đúng 3
Bình luận (0)
cho 13 g kim loại hoá trị 2 tác dụng vừa đủ với 0,4 mol HCl tìm kim loại đó
\(A+2HCl\rightarrow ACl_2+H_2\)
\(0.2.......0.4\)
\(M_A=\dfrac{13}{0.2}=65\left(\dfrac{g}{mol}\right)\)
\(A:Zn\)
Đúng 2
Bình luận (0)
PTHH: \(R+2HCl\rightarrow RCl_2+H_2\)
Ta có: \(n_R=\dfrac{1}{2}n_{HCl}=0,2\left(mol\right)\)
\(\Rightarrow M_R=\dfrac{13}{0,2}=65\) (Kẽm)
Đúng 1
Bình luận (0)
cho 9,4 gam hỗn hợp Na và kim loại R hoá trị ii tan trong nước dư thoát ra 3,36lít H2. Mặt khác cho 0,2 mol hỗn hợp kim loại trên tác dụng với HCl dư sinh ra 3,36lit H2. Xác định R
TN1: \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{Na}=a\left(mol\right)\\n_R=b\left(mol\right)\end{matrix}\right.\)
PTHH:
2Na + 2H2O ---> 2NaOH + H2
a--------------------------------->0,5a
R + 2H2O ---> R(OH)2 + H2
b------------------------------>b
=> 0,5a + b =0,15 (1)
TN2: \(\left\{{}\begin{matrix}n_{Na}=ak\left(mol\right)\\n_R=bk\left(mol\right)\end{matrix}\right.\)
=> ak + bk = 0,2 (2)
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH:
2Na + 2HCl ---> 2NaCl + H2
ak------------------------------>0,5ak
R + 2HCl ---> RCl2 + H2
bk------------------------>bk
=> 0,5ak + bk = 0,15 (3)
(1)(2)(3) => \(\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,1\left(mol\right)\\k=1\end{matrix}\right.\)
\(\rightarrow M_R=\dfrac{9,4-0,1.23}{0,1}=71\left(\dfrac{g}{mol}\right)\) Đề sai à bạn?
Đúng 2
Bình luận (1)
Cho 5,56g hỗn hợp A gồm Fe và kim loại M ( hóa trị không đổi) . Chia A thành 2 phần bằng nhau
Phần 1 : Hòa tan hết trong dd HCl được 1,568 lít khí H2(đktc)
Phần 2 : Tác dụng vừa đủ với 2,016 lít khí Cl2 ( đktc) . Xác định kim loại M? Giúp mình vớii
Gọi: \(\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_M=y\left(mol\right)\end{matrix}\right.\) (trong 1 phần) ⇒ 56x + MM.y = 5,56:2 (1)
Giả sử M có hóa trị n không đổi.
- Phần 2: \(n_{Cl_2}=\dfrac{2,016}{22,4}=0,09\left(mol\right)\)
PT: \(2Fe+3Cl_2\underrightarrow{t^o}2FeCl_3\)
\(2M+nCl_2\underrightarrow{t^o}2MCl_n\)
Theo PT: \(n_{Cl_2}=\dfrac{3}{2}n_{Fe}+\dfrac{n}{2}n_M=\dfrac{3}{2}x+\dfrac{n}{2}y=0,09\left(2\right)\)
- Phần 1: \(n_{H_2}=\dfrac{1,568}{22,4}=0,07\left(mol\right)\)
+ TH1: M có pư với HCl.
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(2M+2nHCl\rightarrow2MCl_n+nH_2\)
Theo PT: \(n_{H_2}=n_{Fe}+\dfrac{n}{2}n_M=x+\dfrac{n}{2}y=0,07\left(3\right)\)
Từ (2) và (3) \(\Rightarrow\left\{{}\begin{matrix}x=0,04\left(mol\right)\\ny=0,06\end{matrix}\right.\)
Thay vào (1), ta được: \(M_M.y=0,54\) \(\Rightarrow\dfrac{M_M.y}{n.y}=\dfrac{0,54}{0,06}\Rightarrow M_M=9n\)
Với n = 3 thì MM = 27 (g/mol) là thỏa mãn.
→ M là Al.
+ TH2: M không pư với HCl.
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(x=n_{Fe}=n_{H_2}=0,07\left(mol\right)\)
Thay vào (1) ta được \(M_M.y=-1,14\) (vô lý vì MM và y đều là số dương)
Vậy: M là Al.
Đúng 2
Bình luận (0)





















