Bài tập Lập hệ phương trình
Hoà tan hoàn toàn hh 9,3g Fe và Zn trong dd HCl vừa đủ thu 3,36 lít khí H2. Tính % khối lượng Zn trong hh đầu?
Bài tập Lập hệ phương trình
Hoà tan hoàn toàn hh 18,6g Fe và Zn trong 200ml dd HCl 3M vừa đủ. Tính khối lượng Zn trong hh đầu?
Đặt \(n_{Fe}=x(mol);n_{Zn}=y(mol)\Rightarrow 56x+65y=18,6(1)\)
\(n_{HCl}=3.0,2=0,6(mol)\\ PTHH:Fe+2HCl\to FeCl_2+H_2\\ Zn+2HCl\to ZnCl_2+H_2\\ \Rightarrow 2x+2y=0,6(2)\\ (1)(2)\Rightarrow x=0,1(mol);y=0,2(mol)\\ \Rightarrow m_{Zn}=0,2.65=13(g)\)
Bài tập Lập hệ phương trình
Hoà tan hoàn toàn hh 9,52g FeO và Zn trong 280ml dd HCl 1M vừa đủ. Tính khối lượng FeO trong hh đầu?
Đặt \(n_{FeO}=x(mol);n_{Zn}=y(mol)\Rightarrow 72x+65y=9,52(1)\)
\(n_{HCl}=0,28.1=0,28(mol)\\ PTHH:FeO+2HCl\to FeCl_2+H_2O\\ Zn+2HCl\to ZnCl_2+H_2\\ \Rightarrow 2x+2y=0,28(2)\\ (1)(2)\Rightarrow x=0,06(mol);y=0,08(mol)\\ \Rightarrow m_{FeO}=0,06.72=4,32(g)\)
Gọi số mol FeO, Zn là a,b
=> 72a + 65b = 9,52 (1)
nHCl = 0,28.1 = 0,28(mol)
PTHH: FeO + 2HCl --> FeCl2 + H2O
_______a--->2a
Zn + 2HCl --> ZnCl2 + H2
b----->2b
=> 2a + 2b = 0,28
=> a + b = 0,14 (2)
(1)(2) => \(\left\{{}\begin{matrix}a=0,06\\b=0,08\end{matrix}\right.\)
=> mFeO = 0,06.72 = 4,32(g)
Bài tập Lập hệ phương trình
Hoà tan hoàn toàn hh 8g Fe và Mg trong dd HCl vừa đủ thu 22,2g muối. Tính % khối lượng Fe trong hh đầu?
Đặt \(n_{Fe}=x(mol);n_{Mg}=y(mol)\Rightarrow 56x+24y=8(1)\)
\(PTHH:Fe+2HCl\to FeCl_2+H_2\\ Mg+2HCl\to MgCl_2+H_2\\ \Rightarrow 127x+95y=22,2(2)\\ (1)(2)\Rightarrow x=y=0,1(mol)\\ \Rightarrow \%_{Fe}=\dfrac{0,1.56}{8}.100\%=70\%\)
Hoà tan hoàn toàn hh 12,1g Fe và Zn trong 200ml dd HCl 2M vừa đủ. Tính % khối lượng Fe trong hh đầu?
Gọi số mol Fe, Zn là a,b
=> 56a + 65b = 12,1 (1)
PTHH: Fe + 2HCl --> FeCl2 + H2
______a---->2a
Zn + 2HCl --> ZnCl2 + H2
_b---->2b
=> 2a + 2b = 0,4 (2)
(1)(2) => \(\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\)
=> \(\%Fe=\dfrac{56.0,1}{12,1}.100\%=46,28\%\)
Đặt \(n_{Fe}=x(mol);n_{Zn}=y(mol)\Rightarrow 56x+65y=12,1(1)\)
\(n_{HCl}=2.0,2=0,4(mol)\\ PTHH:Fe+2HCl\to FeCl_2+H_2\\ Zn+2HCl\to ZnCl_2+H_2\\ \Rightarrow 2x+2y=0,4(2)\\ (1)(2)\Rightarrow x=y=0,1(mol)\\ \Rightarrow \%_{Fe}=\dfrac{0,1.56}{12,1}.100\%=46,28\%\)
Hòa tan hoàn toàn hh X gồm Fe và Zn bằng 1 lượng vừa đủ h2so4 10% thu được dd Y và 22,4l h2 ( đktc). nồng đọ của znso4 trong dd Y là 11,6022%. tính khối lượng mỗi kl trong X.
Số mol H2 = 22,4: 22,4 = 1 mol. Goi số mol Fe là x và số mol Zn là y
Fe + H2SO4 → FeSO4 + H2 (1)
Mol x→ x→ x→ x
Zn + H2SO4 → ZnSO4 + H2 (2)
Mol y→ y→ y→ y
=>Số mol H2SO4 = số mol H2 = (x+y) = 1 (*)
Khối lượng dung dịch H2SO4 = 98 . 100/10 = 980 gam
mdd = 56x +65y + 980 – 2 = (56x + 65y +978)
C%(ZnSO4) = 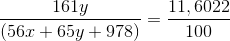
=>15345,857y – 649,7232x = 11346,9516 (**)
Giải hệ PT (*) và (**): x = 0,25; y = 0,75
=>mFe = 0,25.56 = 14g; mZn = 0,75.65 = 48,75g
Hòa tan hoàn toàn 24,2g hỗn hợp X gồm 2 kim loại là Zn và Fe trong 200 ml dung dịch HCl vừa đủ thu được V lít khí H2(đktc) và dung dịch Y. Cô cạn đ Y thu đc 52,6g muối khan.
a, Tính V lít H2
b, Lượng H2 thoát ra ở trên tác dụng vừa đủ với m gam hh Z gồm 50% CuO và 50% Fe2O3 về khối lượng. Tính m?
a. Gọi x, y lần lượt là số mol của Zn và Fe
PTHH: Zn + 2HCl ---> ZnCl2 + H2 (1)
Fe + 2HCl ---> FeCl2 + H2 (2)
Theo PT(1): \(n_{ZnCl_2}=n_{Zn}=x\left(mol\right)\)
Theo PT(2): \(n_{FeCl_2}=n_{Fe}=y\left(mol\right)\)
Theo đề, ta có:
136x + 127y = 52,6 (*)
65x + 56y = 24,2 (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}136x+127y=52,6\\65x+56y=24,2\end{matrix}\right.\)
=> x = 0,2, y = 0,2
Theo PT(1): \(n_{H_2}=n_{Zn}=0,2\left(mol\right)\)
Theo PT(2): \(n_{H_2}=n_{Fe}=0,2\left(mol\right)\)
=> \(n_{H_2}=0,2+0,2=0,4\left(mol\right)\)
=> \(V_{H_2}=0,4.22,4=8,96\left(lít\right)\)
Hòa tan hoàn toàn 24,2g hỗn hợp X gồm 2 kim loại là Zn và Fe trong 200 ml dung dịch HCl vừa đủ thu được V lít khí H2(đktc) và dung dịch Y. Cô cạn đ Y thu đc 52,6g muối khan.
a, Tính V lít H2
b, Lượng H2 thoát ra ở trên tác dụng vừa đủ với m gam hh Z gồm 50% CuO và 50% Fe2O3 về khối lượng. Tính m?
Hòa tan hh gồm fe và zn trong 50ml dd hcl 0,4M thu dc dd A và 1,792 lít khí H2(đktc) cô cạn đe A đc 10,52g muối khan a, Tính khối lượng hh ban đầu b, tính nồng độ mol các chất ddA ? Bt rằng thể tích dd thu đc sau phản ứng ko đáng kể
hòa tan hoàn toàn 13,9g hh gồm al và fe trong đd axit hcl 14,6% vừa đủ sau phản ứng thoát ra 7,84 l khí h2 ở đktc , thu đc dd X
a) vieeta pthh
b)tính khối lượng mỗi kim loại trong hh ban đầu
c) tính nồng độ phần trăm mỗi muối trong dd X
\(\text{Đặt }n_{Al}=x(mol);n_{Fe}=y(mol)\\ \Rightarrow 27x+56y=13,9(1)\\ n_{H_2}=\dfrac{7,84}{22,4}=0,35(mol)\\ a,PTHH:2Al+6HCl\to 2AlCl_3+3H_2(1)\\ Fe+2HCl\to FeCl_2+H_2(2)\\ b,\text{Từ 2 PT: }1,5x+y=0,35(2)\\ (1)(2)\Rightarrow x=0,1(mol);y=0,2(mol)\\ \Rightarrow m_{Al}=0,1.27=2,7(g)\\ m_{Fe}=0,2.56=11,2(g)\)
\(c,n_{HCl(1)}=3n_{Al}=0,3(mol);n_{AlCl_3}=0,1(mol);n_{H_2(1)}=0,15(mol)\\ \Rightarrow m_{dd_{HCl(1)}}=\dfrac{0,3.36,5}{14,6\%}=75(g)\\ \Rightarrow C\%_{AlCl_3}=\dfrac{0,1.133,5}{2,7+75-0,15.2}.100\%=17,25\%\)
\(n_{HCl(2)}=2n_{Fe}=0,4(mol);n_{FeCl_2}=n_{H_2(2)}=n_{Fe}=0,2(mol)\\ \Rightarrow m{dd_{HCl(2)}}=\dfrac{0,4.36,5}{14,6\%}=100(g)\\ \Rightarrow C\%_{FeCl_2}=\dfrac{0,2.127}{11,2+100-0,2.2}.100\%=22,92\%\)
a) 2Al + 6HCl --> 2AlCl3 + 3H2
Fe + 2HCl --> FeCl2 + H2
b) Gọi số mol Al, Fe lần lượt là a,b
=> 27a + 56b = 13,9
\(n_{H_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
2Al + 6HCl --> 2AlCl3 + 3H2
a----->3a--------->a------->1,5a______(mol)
Fe + 2HCl --> FeCl2 + H2
b------>2b-------->b----->b__________(mol)
=> 1,5a + b = 0,35
=> \(\left\{{}\begin{matrix}a=0,1=>m_{Al}=0,1.27=2,7\left(g\right)\\b=0,2=>m_{Fe}=0,2.56=11,2\left(g\right)\end{matrix}\right.\)
c) nHCl = 3a + 2b = 0,7 (mol)
=> mHCl = 0,7.36,5 = 25,55(g)
=> \(m_{ddHCl}=\dfrac{25,55.100}{14,6}=175\left(g\right)\)
\(m_{dd\left(saupu\right)}=13,9+175-2.0,35=188,2\left(g\right)\)
\(\left\{{}\begin{matrix}m_{AlCl_3}=0,1.133,5=13,35\left(g\right)\\m_{FeCl_2}=0,2.127=25,4\left(g\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}C\%\left(AlCl_3\right)=\dfrac{13,35}{188,2}.100\%=7,1\%\\C\%\left(FeCl_2\right)=\dfrac{25,4}{188,2}.100\%=13,5\%\end{matrix}\right.\)