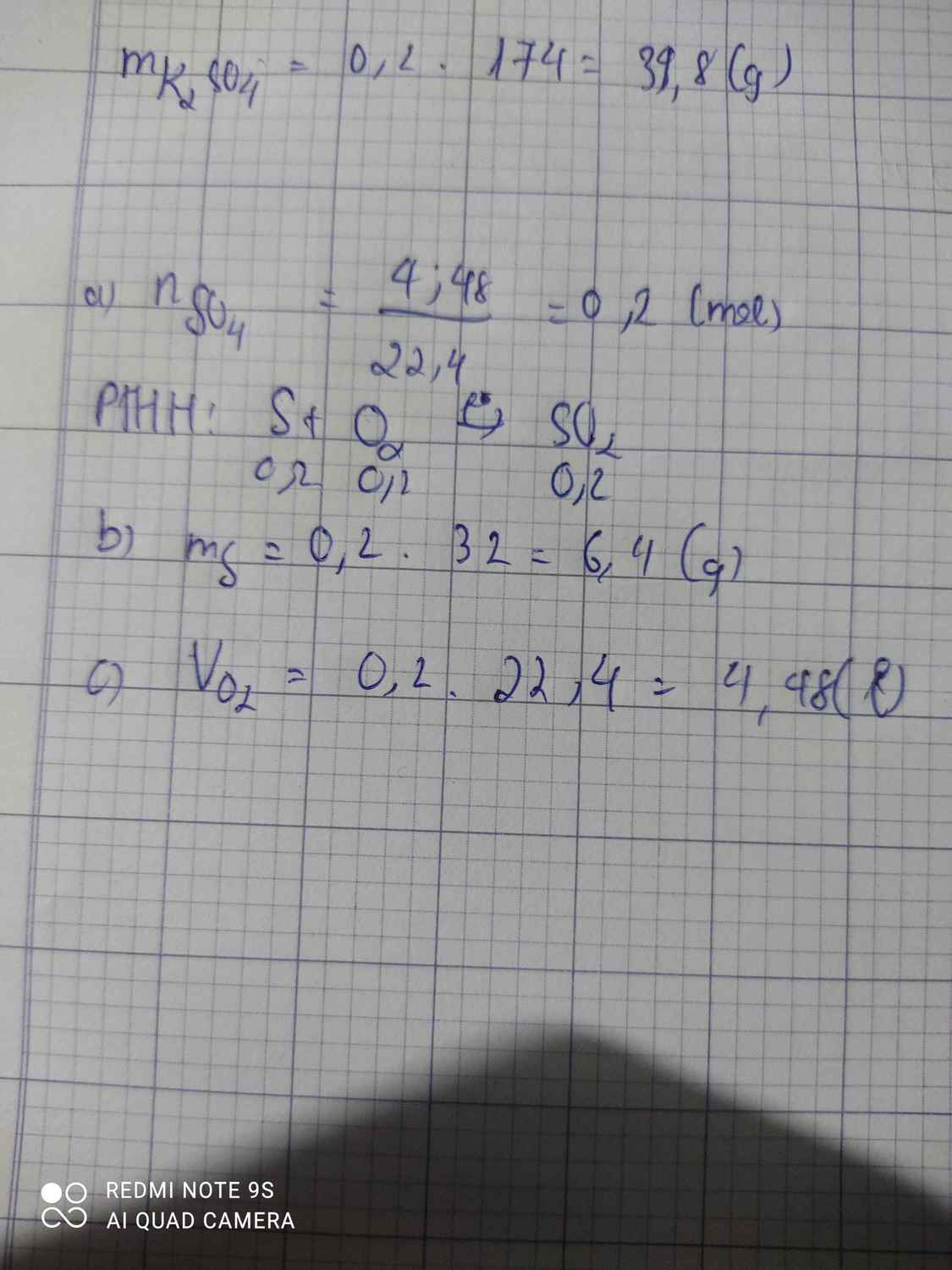Những câu hỏi liên quan
Câu 14: (1.5đ). Cho 3,2 gam lưu huỳnh cháy trong khí oxi sau phản ứng thu được khí sunfurơ (SO2 ) a. Lập phương trình phản ứng? b. Tính khối lượng oxi tham gia phản ứng và thể tích SO2 sinh ra ở (đktc). Cho biết : S =32 ; O2 =16
a) $S + O_2 \xrightarrow{t^o} SO_2$
b)
Theo PTHH :
$n_{O_2} = n_{SO_2} = n_S = \dfrac{3,2}{32} = 0,1(mol)$
$m_{O_2} = 0,1.32 = 3,2(gam)$
$V_{SO_2} = 0,1.22,4 = 2,24(lít)$
Đúng 2
Bình luận (0)
Ta có: n S = 3,2 / 32 = 0,1 ( mol )
PTHH: S + O2 \(\rightarrow\) SO2
0,1--0,1-----0,1
Theo pthh
n O2 = 0,1 ( mol ) => m O2 = 3,2 ( g )
n SO2 = 0,1 ( mol ) => V SO2 = 2,24 ( lít )
Đúng 2
Bình luận (0)
Bài 3: Đốt cháy hoàn toàn 6,4 g bột lưu huỳnh trong không khí thu được lưu huỳnh trong không khí thu được lưu huỳnh dioxit( SO2)
.a. Tính khối lượng của chất tạo thành.
b. Tính thể tích khí oxi tham gia phản ứng ở điều kiện tiêu chuẩn.
Ta có: \(n_S=\dfrac{6,4}{32}=0,2\left(mol\right)\)
a. PTHH: S + O2 ---to---> SO2
Theo PT: \(n_{SO_2}=n_S=0,2\left(mol\right)\)
=> \(m_{SO_2}=0,2.64=12,8\left(g\right)\)
b. Theo PT: \(n_{O_2}=n_S=0,2\left(mol\right)\)
=> \(m_{O_2}=0,2.32=6,4\left(g\right)\)
Đúng 2
Bình luận (1)
a)S+O2-------->SO2
b)n S=6,4/32=0,2(mol)
Theo pthh
n SO2 =n S=0,2(mol)
V SO2=0,2.22,4=4,48(mol)
Đúng 0
Bình luận (1)
Đốt cháy lưu huỳnh trong oxi sau phản ứng thu được 4,48l khí sunfurơ (đktc)
a) viết phương trình phản ứng
b) tính khối lượng lưu huỳnh tham gia phản ứng cháy
c) tính thể tích (đktc) khí oxi cần thiết để phản ứng xảy ra hoàn toàn
S+O2-to>SO2
0,2--0,2----0,2 mol
n SO2=\(\dfrac{4,48}{22,4}\)=0,2 mol
=>m S=0,2.32=6,4g
=>VO2=0,2.22,4=4,48l
Đúng 5
Bình luận (4)
a. \(n_{SO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH : S + O2 -to> SO2
0,2 0,2 0,2
b. \(m_S=0,2.32=6,4\left(g\right)\)
c. \(V_S=0,2.22,4=44,8\left(l\right)\)
Đúng 1
Bình luận (1)
Đốt cháy 3,2 gam lưu huỳnh cháy trong không khí thu được 6,4 gam lưu huỳnh đioxit SO2. Tính khối lượng oxi đã tham gia phản ứng? Biết lưu huỳnh cháy là tham gia phản ứng với khí oxi.
Định luật bảo toàn khối lượng :
\(m_S+m_{O2}=m_{SO2}\)
3,2 + \(m_{O2}\) = 6,4
⇒ \(m_{O2}=6,4-3,2=3,2\left(g\right)\)
Chúc bạn học tốt
Đúng 2
Bình luận (0)
\(BTKL: \\ m_S+m_{O_2}=m_{SO_2}\\ 3,2+m_{O_2}=6,4\\ m_{O_2}=6,4-3,2=3,1(g)\)
Đúng 0
Bình luận (1)
Lưu huỳnh (S) cháy trong không khí sinh ra chất khí mùi hắc, gây ho đó là lưu huỳnh đioxit (khí sunfurơ) có công thức hóa học là SO2. a) Viết phương trình hóa học của lưu huỳnh cháy trong không khí. b) Biết khối lượng lưu huỳnh tham gia phản ứng là 1,6g. Hãy tìm. -Thể tích khí sunfurơ sinh ra ở đktc. -Thể tích không khí cần dùng ở đktc. Biết oxi chiếm 1/5 thể tích không khí.
Đọc tiếp
Lưu huỳnh (S) cháy trong không khí sinh ra chất khí mùi hắc, gây ho đó là lưu huỳnh đioxit (khí sunfurơ) có công thức hóa học là SO2.
a) Viết phương trình hóa học của lưu huỳnh cháy trong không khí.
b) Biết khối lượng lưu huỳnh tham gia phản ứng là 1,6g. Hãy tìm.
-Thể tích khí sunfurơ sinh ra ở đktc.
-Thể tích không khí cần dùng ở đktc. Biết oxi chiếm 1/5 thể tích không khí.
a) Phương trình hóa học S + O2 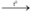 SO2
SO2
b) nS = 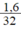 = 0,05 mol.
= 0,05 mol.
Theo phương trình trên, ta có:
nSO2 = nS = nO2 = 0,05 mol.
⇒ VSO2 = 0,05 .22,4 = 1,12 l.
⇒ VO2 = 22,4.0,05 = 1,12 l
Vì khí oxi chiếm 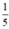 thể tích của không khí nên thể tích không khí cần là
thể tích của không khí nên thể tích không khí cần là
⇒ Vkk = 5VO2 = 5.1,12 = 5,6 l
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 64g lưu huỳnh trong bình chứa oxi thu được lưu huỳnh đioxit (SO2) a,Viết phương trình phản ứng xảy ra b,Tính thể tích khí oxi tham gia phương trình ở đktc c,Tính khối lượng Kali clorat (KClO3) cần dùng để phân hủy thì thu được một thể tích khí oxi bằng với thể tích khí oxi đã sử dụng ở phản ứng trên. Gỉa sử hiệu suất của phản ứng là 80%, thể tích đo được ở đktc
Đọc tiếp
Đốt cháy hoàn toàn 64g lưu huỳnh trong bình chứa oxi thu được lưu huỳnh đioxit (SO2) a,Viết phương trình phản ứng xảy ra b,Tính thể tích khí oxi tham gia phương trình ở đktc c,Tính khối lượng Kali clorat (KClO3) cần dùng để phân hủy thì thu được một thể tích khí oxi bằng với thể tích khí oxi đã sử dụng ở phản ứng trên. Gỉa sử hiệu suất của phản ứng là 80%, thể tích đo được ở đktc
a)`S+O_2->SO_2` nhiệt độ
`0,5-0,5`mol
`n_S=32/64=0,5`mol
`V_(O_2)=0,5.22,4=1,12l`l
c) `2KClO_3->2KCl+3O_2` nhiệt độ
`1/3-------0,5` mol
`H=80%`
`m_(KClO_3)=1/3.(122,5).80%=32,67`g
Đúng 1
Bình luận (0)
Bài 5: Đốt cháy 6,4 gam lưu huỳnh trong bình chứa khí oxi tạo thành Lưu huỳnh đioxit (SO2).
a. Viết phương trình hóa học
b. Tính khối lượng chất tạo thành
c. Tính thể tích khí oxi tham gia phản ứng ở đktc
a, \(n_S=\dfrac{6,4}{32}=0,2\left(mol\right)\)
PTHH: S + O2 ----to----> SO2
Mol: 0,2 0,2 0,2
b, \(m_{SO_2}=0,2.64=12,8\left(g\right)\)
c, \(V_{O_2}=0,2.22,4=4,48\left(l\right)\)
Đúng 3
Bình luận (0)
Cho 3,2g lưu huỳnh đốt cháy trong khí oxi. Sau phản ứng thu đc 1,12l khí SO2 ở đktc Tính thể tích khí oxi sau khi tham gia phản ứng