
Những câu hỏi liên quan
Cho 20 gam hỗn hợp gồm Mg Al và Cu tác dụng với HCL thu được 8,96 lít điều kiện chuẩn và 3 gam chất rắn .Tính khối lượng muối clorua thu được
Xem chi tiết
Ta có :
\(n_{H_2} =\dfrac{8,96}{22,4} = 0,4(mol)\)
Bảo toàn nguyên tố với H : \(n_{HCl} = 2n_{H_2} = 0,4.2 = 0,8(mol)\)
Bảo toàn khối lượng :
\(m_{muối} = m_{hỗn\ hợp} + m_{HCl} - m_{chất\ rắn} - m_{H_2} = 20 + 0,8.36,5 - 3 - 0,4.2 = 45,4(gam)\)
Đúng 3
Bình luận (0)
Cho 72,6 gam hỗn hợp A gồm 3 muối CaCO3, K2CO3 và Na2CO3 tác dụng hết với dung dịch HCl thu được 13,44 lít CO2 điều kiện tiêu chuẩn Tính khối lượng hỗn hợp muối clorua thu được
Hỗn hợp X gồm Al, Fe2O3, Fe3O4 và CuO trong đó oxi chiếm 25,39% khối lượng hỗn hợp. Cho m gam hỗn hợp X tác dụng với 8,96 lít CO (điều kiện tiêu chuẩn) sau một thời gian thu được chất rắn Y và hỗn hợp khí Z có tỉ khối so với hiđro là 19. Cho chất rắn Y tác dụng với dung dịch HNO3 loãng dư thu được dung dịch T và 7,168 lít NO (điều kiện tiêu chuẩn, sản phẩm khử duy nhất). Cô cạn dung dịch T thu được 3,456m gam muối khan. Giá trị của m gần với giá trị nào sau đây nhất? A. 42,5 B. 35,0 C. 38,5 D...
Đọc tiếp
Hỗn hợp X gồm Al, Fe2O3, Fe3O4 và CuO trong đó oxi chiếm 25,39% khối lượng hỗn hợp. Cho m gam hỗn hợp X tác dụng với 8,96 lít CO (điều kiện tiêu chuẩn) sau một thời gian thu được chất rắn Y và hỗn hợp khí Z có tỉ khối so với hiđro là 19. Cho chất rắn Y tác dụng với dung dịch HNO3 loãng dư thu được dung dịch T và 7,168 lít NO (điều kiện tiêu chuẩn, sản phẩm khử duy nhất). Cô cạn dung dịch T thu được 3,456m gam muối khan. Giá trị của m gần với giá trị nào sau đây nhất?
A. 42,5
B. 35,0
C. 38,5
D. 40,5D. 40,5
Đáp án C
· X gồm 0,2539m (g) O và 0,7461m (g) kim loại.
· Hỗn hợp khí Z gồm CO dư và CO2
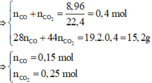
Þ Y gồm 0,7461m (g) kim loại và 0,2539m – 16.0,25 = 0,2539m – 4 (g) O
· Y + HNO3 → 0,32 mol NO + 3,456m g muối
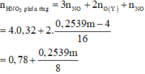
Þ Dung dịch T chứa
n NO 3 - = 0 , 78 + 0 , 2359 m 8 - 0 , 32 = 0 , 46 + 0 , 2359 m 8 ⇒ m muối = 0 , 7461 m + 62 . 0 , 46 + 0 , 2359 m 8 = 3 , 456 m ⇒ m = 38 , 43 g
Gần nhất với giá trị 38
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Al, Fe2O3, Fe3O4, CuO trong đó oxi chiếm 25,39% khối lượng hỗn hợp. Cho m gam hỗn hợp X tác dụng với 8,96 lít CO(điều kiện tiêu chuẩn) sau 1 thời gian thu được chất rắn Y và hỗn hợp khí Z có tỉ khối so với hiđro là 19. Cho chất rắn Y tác dụng với dung dịch HNO3 loãng dư thu được dung dịch T và 7,168 lít NO(điều kiện tiêu chuẩn, sản phẩm khử duy nhất). Cô cạn dung dịch T thu được 3,456m gam muối khan. Giá trị của m gần với giá trị nào sau đây nhất? A. 41,13 B. 35,19 C. 38,40 D....
Đọc tiếp
Hỗn hợp X gồm Al, Fe2O3, Fe3O4, CuO trong đó oxi chiếm 25,39% khối lượng hỗn hợp. Cho m gam hỗn hợp X tác dụng với 8,96 lít CO(điều kiện tiêu chuẩn) sau 1 thời gian thu được chất rắn Y và hỗn hợp khí Z có tỉ khối so với hiđro là 19. Cho chất rắn Y tác dụng với dung dịch HNO3 loãng dư thu được dung dịch T và 7,168 lít NO(điều kiện tiêu chuẩn, sản phẩm khử duy nhất). Cô cạn dung dịch T thu được 3,456m gam muối khan. Giá trị của m gần với giá trị nào sau đây nhất?
A. 41,13
B. 35,19
C. 38,40
D. 40,03
Hòa tan hoàn toàn 7,8 g hỗn hợp mg al trong dung dịch HCl dư thấy thoát ra 8,96 lít khí h2 điều kiện tiêu chuẩn với dung dịch x
a tính khối lượng và phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu
b tính phần trăm khối lượng muối clorua thu được khi cô cạn dung dịch x
Xem chi tiết
Giả sử: \(\left\{{}\begin{matrix}n_{Mg}=x\left(mol\right)\\n_{Al}=y\left(mol\right)\end{matrix}\right.\)
⇒ 24x + 27y = 7,8 (1)
Ta có: \(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
BT e, có: 2x + 3y = 0,8 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Mg}=0,1.24=2,4\left(g\right)\\m_{Al}=0,2.27=5,4\left(g\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{2,4}{7,8}.100\%\approx30,77\%\\\%m_{Al}\approx69,23\%\end{matrix}\right.\)
b, BTNT Mg và Al, có:
nMgCl2 = nMg = 0,1 (mol)
nAlCl3 = nAl = 0,2 (mol)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{MgCl_2}=\dfrac{0,1.95}{0,1.95+0,2.133,5}.100\%\approx26,24\%\\\%m_{AlCl_3}\approx73,76\%\end{matrix}\right.\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
Cho 10,8 g hỗn hợp A gồm Mg và Cu vào dung dịch H2 SO4 loãng dư sau phản ứng người ta thu được 8,96 lít khí H2 ở điều kiện tính chất và 3 gam chất rắn không tan a) Tính thành phần trăm của hỗn hợp A theo khối lượng b) cho hỗn hợp a vào dung dịch KOH dư.Tính thể tích khí H2 sinh ra ở điều kiện tính chất
hoà tan 16g hỗn hợp mg và cu vào dung dịch HCl(dư), sau phản ứng thu được 2,24 lít khí(ở điều kiện tiêu chuẩn) và chất rắn b. lấy b cho tác dụng với h2so4( đặc) đun nóng sinh ra khí co2: a, viết phương trình hoá học xảy ra. b, tính khối lượng mỗi kim loại trong hỗn hợp a Giúp mình với ạ, mình cảm ơn nhiềuuu
a, Mg + 2HCl \(\rightarrow\) MgCl2 + H2 Cu + 2HCl \(\rightarrow\) CuCl2 + H2
b, \(\left\{{}\begin{matrix}n_{Mg}=x\\n_{Cu}=y\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}24x+64y=16\\x+y=\dfrac{2,24}{22,4}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=-0,24\\y=0,34\end{matrix}\right.\)
Xem lại đầu bài nha
Đúng 0
Bình luận (0)
Cho 33,2 g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch HCl thu được V lít khí ở đktc và chất rắn không tan Y. Cho Y hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2 (đktc). Phần trăm khối lượng của Cu trong hỗn hợp X là A. 57,83%. B. 33,33%. C. 19,28%. D. 38,55%.
Đọc tiếp
Cho 33,2 g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch HCl thu được V lít khí ở đktc và chất rắn không tan Y. Cho Y hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2 (đktc). Phần trăm khối lượng của Cu trong hỗn hợp X là
A. 57,83%.
B. 33,33%.
C. 19,28%.
D. 38,55%.
cho hỗn hợp x gồm Mg và Cu có khối lượng 28 8g tác dụng với HCl sau pư thu được 8,96 lít khí H2 (đktc).Tính %m mỗi dung dịch
nH2 = \(\dfrac{8,96}{22,4}=0,4mol\)
Do chỉ có Mg tác dụng với HCl
Bảo toàn e
2nMg = 2nH2 = 0,8 mol
=> nMg = 0,4 mol
=> mMg = 9,6g
=> %mMg= \(\dfrac{9,6}{28,8}.100\%=33,33\%\)
%mCu = 100 - 33,33% = 66,67%
Đúng 1
Bình luận (0)
\(n_{H_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(n_{Mg}=0.4\left(mol\right)\)
\(\%Mg=\dfrac{0.4\cdot24}{28.8}\cdot100\%=33.33\%\)
\(\%Cu=100-33.33=66.67\%\)
Đúng 1
Bình luận (0)
















