Cho một thanh sắt và một viên kẽm vào cốc chứa 150ml dung dịch CuSO4. Sau một thời gian, lấy hai thanh kim loại ra khỏi cốc, thu được dung dịch M trong đó nồng độ mol của muối kẽm gấp 2,5 lần của muối sắt. Thêm dung dịch NaOH dư vào dung dịch M, lọc lấy kết tủa rồi nung ngoài không khí đến khối lượng không đổi, thu được 20g chất rắn N. Cho dòng khí H2 đi qua N đốt nóng tới khi phản ứng hoàn toàn, thu được 15,84g chất rắn P. Tính nồng độ mol/lit của dung dịch CuSO4 ban đầu và số gam đồng bám trên mỗi thanh kim loại

Những câu hỏi liên quan
Nhúng một thanh sắt và một thanh kẽm vào một cốc chứa 500ml dung dịch CuSO4, sau một thời gian lấy hai thanh kim loại ra khỏi cốc thì mỗi thanh có thêm đồng bám vào. khối lượng dung dịch bị giảm mất 0,27g. Trong dung dịch sau phản ứng nồng độ mol của ZnSO4 gấp 2,5 lần nồng độ mol của FeSO4.Thêm dung dịch natri hidroxit (lấy dư) lọc lấy hết kết tủa rồi nung ngoài khồn khí đến khối lượng không đổi thu được 14,5g chất rắn.Tính số gam Cu bám trên mỗi thanh kim loại và nồng độ mol của CuSO4 ban đầu
Đọc tiếp
Nhúng một thanh sắt và một thanh kẽm vào một cốc chứa 500ml dung dịch CuSO4, sau một thời gian lấy hai thanh kim loại ra khỏi cốc thì mỗi thanh có thêm đồng bám vào. khối lượng dung dịch bị giảm mất 0,27g. Trong dung dịch sau phản ứng nồng độ mol của ZnSO4 gấp 2,5 lần nồng độ mol của FeSO4.Thêm dung dịch natri hidroxit (lấy dư) lọc lấy hết kết tủa rồi nung ngoài khồn khí đến khối lượng không đổi thu được 14,5g chất rắn.Tính số gam Cu bám trên mỗi thanh kim loại và nồng độ mol của CuSO4 ban đầu
Nhúng một thanh kẽm và một thanh sắt vào cùng một dung dịch CuSO4. Sau một thời gian lấy 2 thanh kim loại ra thấy trong dung dịch còn lại có nồng độ mol ZnSO4 bằng 2,5 lần nồng độ FeSO4. Mặt khác khối lượng dung dịch giảm 2,2 gam. Khối lượng Cu bám lên kẽm và bám lên sắt lần lượt là: A. 64g; 25,6g B. 32g; 12,8g C. 64g; 12,8g D. 32g; 25,6g
Đọc tiếp
Nhúng một thanh kẽm và một thanh sắt vào cùng một dung dịch CuSO4. Sau một thời gian lấy 2 thanh kim loại ra thấy trong dung dịch còn lại có nồng độ mol ZnSO4 bằng 2,5 lần nồng độ FeSO4. Mặt khác khối lượng dung dịch giảm 2,2 gam. Khối lượng Cu bám lên kẽm và bám lên sắt lần lượt là:
A. 64g; 25,6g
B. 32g; 12,8g
C. 64g; 12,8g
D. 32g; 25,6g

Theo (1) có khối lượng Cu bám vào: mCu = 0,4.2,5.64 = 64 (gam)
Theo (2) có khối lượng Cu bám vào: mCu = 0,4.64 =25,6 (gam).
Đáp án A
Đúng 0
Bình luận (1)
Nhúng một thanh sắt và một thanh kẽm vào cùng một cốc chứa 500ml dd CuSO4. Sau 1 thời gian lấy 2 thanh kim loại ra khỏi cốc thì mỗi thanh có thêm kim loại đồng bám vào, khối lượng dd trong cốc bị giảm mất 0, 22g. Trong dd sau phản ứng, nồng độ mol của ZnSO4 gấp 2,5 lần nồng độ mol của FeSO4. Thêm dd NaOH dư vào cốc, lọc lấy kết tủa rồi nung ngoài không khí đến khối lượng ko đổi thu được 14,5 hỗn hợp chất rắn. Tính tổng số gam đồng bám trên thanh kim loại và nồng độ mol của dd CuSO4 ban đầu
Giúp...
Đọc tiếp
Nhúng một thanh sắt và một thanh kẽm vào cùng một cốc chứa 500ml dd CuSO4. Sau 1 thời gian lấy 2 thanh kim loại ra khỏi cốc thì mỗi thanh có thêm kim loại đồng bám vào, khối lượng dd trong cốc bị giảm mất 0, 22g. Trong dd sau phản ứng, nồng độ mol của ZnSO4 gấp 2,5 lần nồng độ mol của FeSO4. Thêm dd NaOH dư vào cốc, lọc lấy kết tủa rồi nung ngoài không khí đến khối lượng ko đổi thu được 14,5 hỗn hợp chất rắn. Tính tổng số gam đồng bám trên thanh kim loại và nồng độ mol của dd CuSO4 ban đầu
Giúp mình với
Copy thì có ý nghĩa gì nhỉ? Đâu phải sức lực mình đâu _._
Đúng 0
Bình luận (0)
n ZnSO4 = 2,5 n FeSO4 Zn+CuSO4−−>ZnSO4+Cu 2,5x------------------------------------2,5x Fe+CuSO4−−>FeSO4+Cu x---------------------------------------x m dung dịch giảm = m 2 kim loại tăng = 0,22 (g) Hay 160x + 64x - 162,5x - 56x = 5,5x = 0,22 (g) --> x = 0,04 (mol) m Cu trên Zn = 6,5 (g) m Cu trên Fe = 2,56 (g) Ở pứ tiếp theo cho vào NaOH dư : ZnSO4+2NaOH−−>Zn(OH)2+Na2SO4 FeSO4+2NaOH−−>Fe(OH)2+Na2SO4 0,04-----------------------------0,04 Zn(OH)2+2NaOH−−>Na2ZnO2+2H2O Trong kết tủa chắc chắn có Fe(OH)2 và có thể có thể có Cu(OH)2 TH1 : Tạo ra 1 kết tủa : Fe(OH)2 2Fe(OH)2+(1/2)O2−−>Fe2O3+2H2O 0,04 -------------------------------0,02 Rõ ràng m Fe2O3 = 3,2 (g) < m rắn theo đề bài ==> Loại TH2 : Tạo 2 kết tủa CuSO4+2NaOH−−>Cu(OH)2+Na2SO4 0,145-----------------------------0,145 2Fe(OH)2+(1/2)O2−−>Fe2O3+2H2O 0,04------------------------------------0,02 Cu(OH)2−−>CuO+H2O 0,145--------------0,145 --> m Fe2O3 = 3,2 (g) --> m CuO = 11,6 (g) --> n CuO = 0,145 (mol) n CuSO4 ban đầu = 0,145 + 0,04.2,5 + 0,04 = 0,285 (mol) --> C m CuSO4 = 0,285/0,5 = 0,57 M
Đúng 0
Bình luận (0)
gọi n\(_{FeCl2}=x\) và n\(_{_{ }ZnSO4}=2,5\left(mol\right)\)

Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Nhúng bản kẽm và bản sắt vào cùng một dung dịch đồng sunfat. Sau một thời gian, nhấc hai bản kim loại ra thì trong dung dịch thu được nồng độ mol của kẽm sunfat bằng 2,5 lần của sắt sunfat. Mặt khác khối lượng của dung dịch giảm 0,11 gam. Khối lượng đồng bám trên mỗi kim loại là: A. 1,28 gam và 3,2 gam B. 6,4 gam và 1,6 gam C. 1,54 gam và 2,6 gam D. 8,6 gam và 2,4 gam
Đọc tiếp
Nhúng bản kẽm và bản sắt vào cùng một dung dịch đồng sunfat. Sau một thời gian, nhấc hai bản kim loại ra thì trong dung dịch thu được nồng độ mol của kẽm sunfat bằng 2,5 lần của sắt sunfat. Mặt khác khối lượng của dung dịch giảm 0,11 gam. Khối lượng đồng bám trên mỗi kim loại là:
A. 1,28 gam và 3,2 gam
B. 6,4 gam và 1,6 gam
C. 1,54 gam và 2,6 gam
D. 8,6 gam và 2,4 gam
Có hai miếng kẽm cùng nặng 100 g , miếng thứ nhất được nhúng vào cốc đựng 100 ml dung dịch CuSO4 dư , miếng thứ hai được nhúng vào cốc đựng 500 ml dung dịch AgNO3 dư . Sau một thời gian lấy hai miếng kẽm ra khỏi dung dịch thấy miếng thứ nhất giảm 0,1% khối lượng , biết rằng nồng độ mol/l của muối kẽm trong hai dung dịch bằng nhau . Hỏi khối lượng miếng kẽm thứ hai thay đổi như thế nào ? Cho rằng các kim loại thoát ra đều bám hoàn toàn vào miếng kẽm
Đọc tiếp
Có hai miếng kẽm cùng nặng 100 g , miếng thứ nhất được nhúng vào cốc đựng 100 ml dung dịch CuSO4 dư , miếng thứ hai được nhúng vào cốc đựng 500 ml dung dịch AgNO3 dư . Sau một thời gian lấy hai miếng kẽm ra khỏi dung dịch thấy miếng thứ nhất giảm 0,1% khối lượng , biết rằng nồng độ mol/l của muối kẽm trong hai dung dịch bằng nhau . Hỏi khối lượng miếng kẽm thứ hai thay đổi như thế nào ? Cho rằng các kim loại thoát ra đều bám hoàn toàn vào miếng kẽm
1.Nhúng một thanh kim loại M hóa trị II vào 0,5 lít dd CuSO4 0,2M.Sau một thời gian pứ,khối lượng thanh M tăng 0,4g trong khi nồng độ CuSO4 còn lại 0,1M
a)Xác định M (Fe)
b)Lấy m(g) kim loại M vào 1 lít dd chứa AgNO3 và Cu(NO3)2 nồng độ mỗi muối là 0,1M.Sau pứ ta thu được rắn A có m15,28g và dd B.Tính m(g)
2.Nhúng một thanh sắt và 1 thanh kẽm vào cùng 1 cốc chứa 500ml dd CuSO4.Sau 1 thời gian lấy 2 thanh kl ra khỏi cốc thì mỗi thanh có thêm Cu bám vào,khối lượng dd trong cốc bị giảm mất 0,22g...
Đọc tiếp
1.Nhúng một thanh kim loại M hóa trị II vào 0,5 lít dd CuSO4 0,2M.Sau một thời gian pứ,khối lượng thanh M tăng 0,4g trong khi nồng độ CuSO4 còn lại 0,1M
a)Xác định M (Fe)
b)Lấy m(g) kim loại M vào 1 lít dd chứa AgNO3 và Cu(NO3)2 nồng độ mỗi muối là 0,1M.Sau pứ ta thu được rắn A có m=15,28g và dd B.Tính m(g)
2.Nhúng một thanh sắt và 1 thanh kẽm vào cùng 1 cốc chứa 500ml dd CuSO4.Sau 1 thời gian lấy 2 thanh kl ra khỏi cốc thì mỗi thanh có thêm Cu bám vào,khối lượng dd trong cốc bị giảm mất 0,22g.Trong dd sau pứ,nồng độ mol của ZnSO4 gấp 2,5 lần nồng độ mol FeSO4.Thêm dd NaOH dư vào cốc,lọc lấy kết tủa r nung ngoài kk đến m không đổi,thu được 14,5g chất rắn.Số gam Cu bám trên mối thanh kl và nồng độ mol của dd CuSO4 ban đầu là bao nhiêu ? (2,56g 6,4g 0,5625M)
1.
M + CuSO4 -> MSO4 + Cu (1)
nCuSO4 ban đầu=0,5.0,2=0,1(mol)
nCuSO4 sau PƯ=0,5.0,1=0,05(mol)
nCuSO4 bị PƯ=0,1-0,05=0,05(mol)
Theo PTHH 1 ta có:
nM=nCu=nCuSO4 bị PƯ=0,05(mol)
mCu sinh ra=64.0,05=3,2(g)
Ta có:
mCu-mM=0,4
=>mM=3,2-0,4=2,8(g)
MM=\(\dfrac{2,8}{0,05}=56\)
Vậy M là sắt,KHHH là Fe
Fe + 2AgNO3 -> Fe(NO3)2 + 2Ag (2)
Fe + Cu(NO3)2 -> Fe(NO3)2 + Cu (3)
nAgNO3=0,1(mol)
nCu(NO3)2=0,1(mol)
Theo PTHH 2 ta có:
nAg=nAgNO3=0,1(mol)
mAg=108.0,1=10,8(g)
Vì 10,8<15,28 nên phải có PƯ 3
mCu=15,28-10,8=4,48(g)
nCu=0,07(mol)
Vì 0,07<0,1 nên sau PƯ 3 xảy ra thì Cu(NO3)2 dư
Theo PTHH 2 và 3 ta có:
nFe(2)=\(\dfrac{1}{2}\)nAg=0,05(mol)
nFe(3)=nCu=0,07(mol)
=>mFe=(0,05+0,07).56=6,72(g)
Đúng 1
Bình luận (7)
Bài 2 sao mình tính mCu bám trên thanh sắt là 11,6 nhỉ
Đúng 0
Bình luận (1)
Bài 1 :
a)
Theo đề bài ta có : nCuSO4 = 0,5.0,2 = 0,1 (mol)
mà sau PƯ CuSO4 còn dư 0,1M => nCuSO4 (pư) = 0,05 (mol)
PTHH :
\(M+C\text{uS}O4->MSO4+Cu\)
0,05mol...0,05mol.....................0,05mol
Ta có :
\(\Delta m\left(t\text{ă}ng\right)=m_{kl\left(sau\right)}-m_{kl\left(tr\text{ư}\text{ớc}\right)}=mCu-mM\)
<=> 0,05.64 - 0,05.M = 0,4
=> M = 56 (g/mol) (nhận) ( Fe = 56 )
=> M là sắt ( Fe)
b)
Ta xét TH 1 : hỗn hợp muối đều phản ứng hết với kim loại M
PTHH :
\(Fe+2AgNO3->Fe\left(NO3\right)2+2Ag\)
\(Fe+Cu\left(NO3\right)2->Fe\left(NO3\right)2+Cu\)
mcr = mCu + mAg = 0,1.64 + 0,1.108 = 17,2(g) > 15,2(g) => TH này không thỏa mãn
Ta xét TH2 : kim loại M chỉ phản ứng hết với dd muối AgNO3
PTHh :
\(Fe+2AgNO3->Fe\left(NO3\right)2+2Ag\)
0,05mol...0,1mol..................................0,1mol
=> mcr = 0,1.108 = 10,8 (g) < 15,28(g) => TH này không thỏa mãn
Ta xét TH 3 : Kim loại M pư với 2 dd muối nhưng sau pư Cu(NO3)2 còn dư
Gọi x là số mol của Cu(NO3)2 dư
PTHH :
\(Fe+2AgNO3->Fe\left(NO3\right)2+2Ag\)
0,05mol...................................................0,1mol
Fe + CuSO4 \(->\) FeSO4 + Cu
xmol.....................................xmol
Ta có :
mCu + mAg = 15,28
<=> 64x + 0,1.108 = 15,28
<=> 64x = 4,48 => x = 0,07(mol)
=> mFe(pư) = (0,05+0,07).56 = 6,72(g)
Vậy....
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Có hai miếng kẽm , miếng thứ nhất nặng 50 gam được cho vào cốc đựng 150 ml dung dịch CuSO4 dư , miếng thứ hai nặng 70 gam được cho vào cốc đựng 450 ml dung dịch AgNO3 dư . Sau một thời gian lấy hai miếng kẽm ra khỏi dung dịch thấy miếng thứ nhất giảm 0,3% khối lượng , biết rằng nồng độ mol/l của muối kẽm trong hai dung dịch bằng nhau . Hỏi khối lượng miếng kẽm thứ hai tăng lên hay giảm xuống bao nhiêu gam ? Cho rằng các kim loại thoát ra đều bám hoàn toàn vào miếng kẽm
Đọc tiếp
Có hai miếng kẽm , miếng thứ nhất nặng 50 gam được cho vào cốc đựng 150 ml dung dịch CuSO4 dư , miếng thứ hai nặng 70 gam được cho vào cốc đựng 450 ml dung dịch AgNO3 dư . Sau một thời gian lấy hai miếng kẽm ra khỏi dung dịch thấy miếng thứ nhất giảm 0,3% khối lượng , biết rằng nồng độ mol/l của muối kẽm trong hai dung dịch bằng nhau . Hỏi khối lượng miếng kẽm thứ hai tăng lên hay giảm xuống bao nhiêu gam ? Cho rằng các kim loại thoát ra đều bám hoàn toàn vào miếng kẽm
Gọi a là số gam Zn tham gia phản ứng ở phương trình :
Zn + CuSO4 \(\rightarrow\) ZnSO4 + Cu ( 1 )
Theo phương trình , ta có : \(n_{Zn}=\dfrac{a}{56}=n_{ZnSO_4}=n_{Cu}\)
Số gam Zn còn dư : 50 - 65 \(\cdot\dfrac{a}{65}+64\cdot\dfrac{a}{65}=50-0,3=49,7\left(g\right)\)
Giải ra , ta được a = 19,5 ( gam ) \(\Rightarrow n_{Zn}=n_{ZnSO_4}=n_{Cu}=0,3\left(mol\right)\)
Gọi b là số gam Zn sau phản ứng ở phương trình :
Zn + 2AgNO3 \(\rightarrow\) Zn(NO3)2 + 2Ag ( 2 )
Vì thể tích dung dịch AgNO3 gấp 3 lần thể tích của dung dịch CuSO4 . Do vậy số mol của AgNO3 sẽ gấp 3 lần số mol của CuSO4 và bằng 0,3 . 3 = 0,9 ( mol ) . Ta có :
b = 70 - 65 . 0,9 + 2 . 0,9 . 108 = 205,9 ( gam )
Vậy khối lượng miếng Zn thứ hai tăng : 205,9 - 70 = 135,9 ( gam )
Đúng 0
Bình luận (0)
Cho 12,8g kim loại A phản ứng hoàn toàn với khí clo thu được muối B. Hòa tan B vào nước thu được 400ml dung dịch C. Nhúng thanh Fe nặng 11,2g vào dung dịch C, sau một thời gian thấy kim loại A bám vào thanh Fe và khối lượng thanh sắt lúc này là 12g, nồng độ FeCl2 0,25M. Tính nồng độ mol của muối B trong dung dịch C A. 1M B. 0,75M C. 0,25M D. 0,5M
Đọc tiếp
Cho 12,8g kim loại A phản ứng hoàn toàn với khí clo thu được muối B. Hòa tan B vào nước thu được 400ml dung dịch C. Nhúng thanh Fe nặng 11,2g vào dung dịch C, sau một thời gian thấy kim loại A bám vào thanh Fe và khối lượng thanh sắt lúc này là 12g, nồng độ FeCl2 0,25M. Tính nồng độ mol của muối B trong dung dịch C
A. 1M
B. 0,75M
C. 0,25M
D. 0,5M
Đáp án D
A → An+
nFe + 2An+ → nFe2+ + 2A
2,2A/n - 5,6 = 12 -11,2 = 0,8→ A = 32n→A = 64 (Cu)
CM = 12,8/(64.0,4) = 0,5M
Đúng 0
Bình luận (0)
Cho 12,8 gam kim loại A hóa trị II phản ứng hoàn toàn với khí Cl2 thu muối B. Hòa tan B vào nước thu được 400ml dung dịch C. Nhúng thanh sắt nặng 11,2 gam vào dung dịch C, sau một thời gian thấy kim loại A bám vào thanh sắt và khối lượng thanh sắt là 12,0 gam, nồng độ FeCl2 trong dung dịch là 0,25M. Xác định kim loại A và nồng độ mol của kim loại B trong dung dịch C.
Đọc tiếp
Cho 12,8 gam kim loại A hóa trị II phản ứng hoàn toàn với khí Cl2 thu muối B. Hòa tan B vào nước thu được 400ml dung dịch C. Nhúng thanh sắt nặng 11,2 gam vào dung dịch C, sau một thời gian thấy kim loại A bám vào thanh sắt và khối lượng thanh sắt là 12,0 gam, nồng độ FeCl2 trong dung dịch là 0,25M. Xác định kim loại A và nồng độ mol của kim loại B trong dung dịch C.
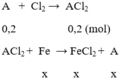
số mol FeCl2 là n = 0,25 . 0,4 = 0,1 (mol)
gọi x là số mol Fe phản ứng
khối lượng kim loại tăng là Δm = mA - mFe = Ax – 56x = 0,8
x = 0,1 → A.0,1 – 56.0,1 = 0,8 → A = 64. A là Cu
số mol Cu là nCu = 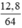 = 0,2 (mol)
= 0,2 (mol)
số mol CuCl2 → n(CuCl2) = nCu = 0,2 (mol)
nồng độ mol/l CuCl2 là C(M(CuCl2)) = 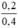 = 0,5M
= 0,5M
Đúng 0
Bình luận (0)

















