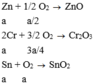Những câu hỏi liên quan
Cho 13,2g hh Mg và Fe tác dụng với lượng dư dd HCl,sau phản ứng thu được dd X và 7,84 lít khí H2( đktc)
a) Viết phương trình phản ứng xảy ra và tính phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu
b) Cô cạn dung dịch X thu được m gam muối khan.Tính m
mn giúp em với
Xem chi tiết
nH2= 0,35(mol)
a) PTHH: Mg + 2 HCl -> MgCl2 + H2
x_________2x_______x______x(mol)
PTHH: Fe + 2 HCl -> FeCl2 + H2
y________2y________y_____y(mol)
Ta có hpt: \(\left\{{}\begin{matrix}24x+56y=13,2\\x+y=0,35\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,15\end{matrix}\right.\)
b) m=m(muối khan)= mMgCl2 + mFeCl2= 95.x+127y=95.0,2+127.0,15= 38,05(g)
Đúng 1
Bình luận (0)
a)
Gọi
\(n_{Fe} = a(mol) ; n_{Mg} = b(mol)\\ \Rightarrow 56a + 24b = 13,2(1)\)
\(Mg + 2HCl \to MgCl_2 + H_2\\ Fe + 2HCl \to FeCl_2 + H_2\)
Theo PTHH : \(n_{H_2} = a + b = 0,35(mol)\)(2)
Từ (1)(2) suy ra a = 0,15 ;b = 0,2
Vậy :
\(\%m_{Fe} = \dfrac{0,15.56}{13,2}.100\% = 63,64\%\\ \Rightarrow m_{Mg} = 100\% - 63,64\% = 36,36\%\)
b)
Ta có :\(n_{HCl} = 2n_{H_2} = 0,7(mol)\)
Bảo toàn khối lượng :
\(m_{muối} = m_{kim\ loại} + m_{HCl} - m_{H_2} = 13,2 + 0,7.36,5 - 0,35.2=38,05(gam)\)
Đúng 1
Bình luận (0)
Cho 13,2g hh Mg và Fe tác dụng với lượng dư dd HCl,sau phản ứng thu được dd X và 8,6765
lít khí H2( đktc) a) Viết phương trình phản ứng xảy ra và tính phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu b) Cô cạn dung dịch X thu được m gam muối khan.Tính mSửa đề: đktc → đkc
a, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Ta có: 24nMg + 56nFe = 13,2 (1)
\(n_{H_2}=\dfrac{8,6765}{24,79}=0,35\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Mg}+n_{Fe}=0,35\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Mg}=0,2\left(mol\right)\\n_{Fe}=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,2.24}{13,2}.100\%\approx36,36\%\\\%m_{Fe}\approx63,64\%\end{matrix}\right.\)
b, Theo PT: \(\left\{{}\begin{matrix}n_{MgCl_2}=n_{Mg}=0,2\left(mol\right)\\n_{FeCl_2}=n_{Fe}=0,15\left(mol\right)\end{matrix}\right.\)
⇒ m muối khan = 0,2.95 + 0,15.127 = 38,05 (g)
Đúng 2
Bình luận (0)
hòa tan m (g) hh gồn Fe và kim loại M có hóa trị ko đổi trong dd HCl dư thì thu đc 1,008 lít khí (đktc) và dd chứa 4,575 g muối khan.
a) Tính m
b) hòa tan m g hh ở trên trong dd chứa hh HNO3 đặc và H2SO4 ở nhiệt độ thích hợp thì thu đc 1,8816 lít hh gồm 2 khí(đktc) có tỉ khối hơi so với H2 là 25,25. Xác định M
hòa tan hoàn toàn khối lượng Fe và Cu(tỉ lệ 1:1) bằng axit HNO3 thu được V lít hỗn hợp khí X gồm NO và NO2 và dung dịch Y (chỉ chứa 2 muốivà axit ) tỉ khối của X đối với H2 bằng 19. tính V
các bạn giải theo cách bảo toàn electron nha
Đúng 0
Bình luận (0)
a) Ta có: nH2 = 1,008/22.4 = 0,045 \(\rightarrow\) nHCl = 0,045 x 2= 0,09mol
mA = mmuối - mCl = 4,575 - 0,09 x 35,5 = 1,38g
Đặt x, y lần lượt là số mol của Fe, M và n là hóa trị của M trong hợp chất. Từ 2 phương trình ta có:
56x + My = 1,38 (1)
2x + ny = 0,09 (2)
b) Ở câu b này mình cho rằng đó là H2SO4 đặc chứ ko phải loãng vì nếu loãng thì ta ko thu được hh khí có tỉ khối hơi như vậy.
Các phương trình phản ứng:
Fe + 6HNO3 \(\rightarrow\) Fe(NO3)3 +3NO2 + 3H2O
M + 2nHNO3\(\rightarrow\) M(NO3)n + nNO2 + nH20
2Fe + 6H2SO4 \(\rightarrow\) Fe2(SO4)3 + 3SO2 + 6H2O
2M + 2nH2SO4 \(\rightarrow\) M2(SO4)n + nSO2 + 2nH2O
Ta có: dkhí/ H2 =25,25 \(\rightarrow\) Mkhí = 50,5
Số mol 2 khí=1,8816:22,4=0,084mol
lập hệ giải ra: nNO2 = 0,063, nSO2 = 0,021
Ta có các phương trình e như sau:
Fe \(\rightarrow\) Fe3+ + 3e
x---------------3x
M \(\rightarrow\) Mn+ + ne
y--------------ny
N5+ + 1e \(\rightarrow\) N4+
0,063 \(\leftarrow\) 0,063
S6+ + 2e\(\rightarrow\) S4+
0,042 \(\leftarrow\) 0,021
Tổng e nhận = tổng e nhường nên :
3x + ny = 0,063 + 0,042 = 0,105
kết hợp với (2) suy ra được x = 0,015
ny = 0,06 \(\rightarrow\) y = 0,06/n
Thay vào (1) \(\rightarrow\) M = 9n
Biện luận thì tìm được M là Al.
Đúng 0
Bình luận (1)
hoà tan 13,4 g hh X gồm Al,Fe,Mg vằng 1 lg vừa đủ dd HCL sau phản ưng thu đc 11,2 l khí h2 và đ chứa m gam muối tìm m
\(n_{H_2}=\dfrac{11.2}{22.4}=0.5\left(mol\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(n_{HCl}=2n_{H_2}=0.5\cdot2=1\left(mol\right)\)
\(BTKL:\)
\(m_X+m_{HCl}=m_M+m_{H_2}\)
\(\Rightarrow m_M=13.4+1\cdot36.5-0.5\cdot2=48.94\left(g\right)\)
Đúng 1
Bình luận (1)
\(2Al + 6HCl \to 2AlCl_3 + 3H_2\\ Fe +2HCl \to FeCl_2 + H_2\\ Mg + 2HCl \to MgCl_2 + H_2\\ n_{Cl} = n_{HCl} = 2n_{H_2} = 2.\dfrac{11,2}{22,4} = 1(mol)\\ m_{muối} = m_{kim\ loại} + m_{Cl} = 13,4 + 1.35,5 = 48,9(gam)\)
Đúng 1
Bình luận (0)
Câu 10: Cho m(g) hh Na2CO3 và Na2SO4 tác dụng hết với dd H2SO4 2M dư thu được 2,24 lít hh khí (ở đktc) có tỷ khối so với H2 bằng 27. Giá trị của m làB. 11,6 gam A. 1,16 g C. 6,11g D. 61,1 gam.Câu 11: Hỗn hợp X gồm có 3 kim loại Al, Mg, Fe. Lấy 6,7 g hhX tác dụng hết với dd H2SO4 thu được 5,6 lít H2 đktc và dd A. Cô cạn dd A thu được m (g) muối khan . Giá trị của m là :C. 30,7g B. 7,2 gam A. 6,2g D. 31,7 gam.Câu 12 : Thêm 100ml dd H,SO, vào 200ml dd NaOH 0,1M ta thu được dd X . Cho X tác dụng vừ...
Đọc tiếp
Câu 10: Cho m(g) hh Na2CO3 và Na2SO4 tác dụng hết với dd H2SO4 2M dư thu được 2,24 lít hh khí (ở đktc) có tỷ khối so với H2 bằng 27. Giá trị của m là
B. 11,6 gam A. 1,16 g C. 6,11g D. 61,1 gam.
Câu 11: Hỗn hợp X gồm có 3 kim loại Al, Mg, Fe. Lấy 6,7 g hhX tác dụng hết với dd H2SO4 thu được 5,6 lít H2 đktc và dd A. Cô cạn dd A thu được m (g) muối khan . Giá trị của m là :
C. 30,7g B. 7,2 gam A. 6,2g D. 31,7 gam.
Câu 12 : Thêm 100ml dd H,SO, vào 200ml dd NaOH 0,1M ta thu được dd X . Cho X tác dụng vừa đủ với 0,25g BaCl2 . Nồng độ của dd H2SO4 ban đầu là.
A. 1,6M B. 0,8M C. 2,6M D. 1,8M
15. Cho một lượng sắt dư vào 500ml dd H2SO4 thu được 33,6 lít H2(đktc).
a.Tính khối lượng bột sắt đã tham gia phản ứng
b.Làm bay hơi dd thu được sau pư thu được m gam muối.xác định m
c. xác định nồng độ mol của dd H2SO4 đã dùng
16. hòa tan hoàn toàn 4 gam hh Mg và Fe trong dd Hcl dư,thu được 2,24 lít khí H2(đktc).Tính khối lượng mỗi mối thu được
17. Cho 22,2g hh Fe,Al tan hoàn toàn trong HCl dư thu được 13,44 lít khí H2(đktc).tính phần trăm khối lượng mỗi kim loại trong hh ban đầu
18. Hòa tan 10...
Đọc tiếp
15. Cho một lượng sắt dư vào 500ml dd H2SO4 thu được 33,6 lít H2(đktc).
a.Tính khối lượng bột sắt đã tham gia phản ứng
b.Làm bay hơi dd thu được sau pư thu được m gam muối.xác định m
c. xác định nồng độ mol của dd H2SO4 đã dùng
16. hòa tan hoàn toàn 4 gam hh Mg và Fe trong dd Hcl dư,thu được 2,24 lít khí H2(đktc).Tính khối lượng mỗi mối thu được
17. Cho 22,2g hh Fe,Al tan hoàn toàn trong HCl dư thu được 13,44 lít khí H2(đktc).tính phần trăm khối lượng mỗi kim loại trong hh ban đầu
18. Hòa tan 10,54g hh Cu,Mg,Fe bằng mọt lượng dư dd HCl thu được 4,48 lít khí(đktc),2,54g chất rắn B ko tan và dd E.Cô cạn E thu được m gam muối khan.tính giá trị của m
20. Cho 115,556g dd BaCl2 45% vào 81,667g dd H2SO4 30%.tính khối lượng kết tủa thu đc.
15
a)\(Fe+H2SO4-->FeSO4+H2\)
\(n_{H2}=\frac{33,6}{22,4}=1,5\left(mol\right)\)
\(n_{Fe}=n_{H2}=1,5\left(mol\right)\)
\(m_{Fe}=1,5.56=84\left(g\right)\)
b)\(n_{FeSO4}=n_{H2}=1,5\left(mol\right)\)
\(m=m_{FeSO4}=1,5.152=228\left(g\right)\)
c)\(n_{H2SO4}=n_{H2}=1,5\left(mol\right)\)
\(C_{M\left(H2SO4\right)}=\frac{1,5}{0,5}=3\left(M\right)\)
16.
n\(_{H2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
Gọi \(n_{Mg}=x,n_{Fe}=y\)
\(Mg+2HCl--.MgCl2+H2\)
x-------------------------x----------x(mol)
\(Fe=2HCl-->FeCl2+H2\)
y----------------------------y------y(mol)
Theo bài ta có hpt
\(\left\{{}\begin{matrix}24x+56y=4\\x+y=0,1\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,05\\y=0,05\end{matrix}\right.\)
\(m_{MgCl2}=0,05.95=4,75\left(g\right)\)
\(m_{FeCl2}=0,05.127=6,35\left(g\right)\)
17.
\(n_{H2}=\frac{13,44}{22,4}=0,6\left(mol\right)\)
\(Fe+2HCl--.FeCl2+H2\)
x----------------------------------x(mol)
\(2Al+6HCl--.2AlCl3+3H2\)
y----------------------------------------1,5y(mol)
theo bài ta có hpt
\(\left\{{}\begin{matrix}56x+27y=22,2\\x+1,5y=0,6\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,3\\y=0,2\end{matrix}\right.\)
\(\%m_{Fe}=\frac{0,3.56}{22,2}.100\%=75,68\%\%\)
\(\%m_{Al}=100-75,68=24,32\%\)
18.
\(Mg+2HCl--.MgCl2+H2\)
\(Fe+2HCl--.FeCl2+H2\)
Chất rắn k tan là Cu = 2,54(g)
=>\(m_{Mg+Fe}=10,54-02,54=10\left(g\right)\)
\(n_{H2}=\frac{4,48}{22,4}=0,2\left(mol\right)\Rightarrow m_{H2}=0,4\left(g\right)\)
\(n_{HCl}=n_{H2}=0,4\left(mol\right)\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)
\(m=m_{Fe+Mg}+m_{HCl}-m_{H2}=10+14,6-0,4=24,2\left(g\right)\)
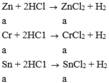
Cho m gam hh bột X gồm ba kim loại Zn, Cr, Sn có số mol bằng nhau t/d hết với lượng dư dd HCl loãng, nóng thu được dd Y và khí H2. Cô cạn dd Y thu được 8,98 gam muối khan. Nếu cho m gam hh X t/d hoàn toàn với O2 (dư) để tạo hh 3 oxit thì thể tích khí O2 (đktc) pư là A. 2, 016 lít. B. 1,008 lít. C. 0,672 lít. D. 1,344 lít.
Đọc tiếp
Cho m gam hh bột X gồm ba kim loại Zn, Cr, Sn có số mol bằng nhau t/d hết với lượng dư dd HCl loãng, nóng thu được dd Y và khí H2. Cô cạn dd Y thu được 8,98 gam muối khan. Nếu cho m gam hh X t/d hoàn toàn với O2 (dư) để tạo hh 3 oxit thì thể tích khí O2 (đktc) pư là
A. 2, 016 lít.
B. 1,008 lít.
C. 0,672 lít.
D. 1,344 lít.
Bài 1 hòa tan hoàn toàn 8,68 g hh Fe , Mg .Zn cần dùng hết 160ml đ HCl 2M
a Tính thể tích của H2 sinh ra
b Cô cạn dd sau pứ thì thu đc bao nhiêu g muối than
bài 2 Cho 7,8 g hh kim loại Al và Mg tác dụng với HCl thu đ 8,96 lít H2 ở đktc . Hỏi khi cô cạn dd thu đc bao nhiêu g muối than
Bài 3 Hòa tan hoàn toàn 11,8 g hh X gồm Fe, Mg và Al 1 lượng vừa đủ đ HCl loãng thu đ 11,2 lít H2 đktc và dd chứa m gam muối Tính m
Đọc tiếp
Bài 1 hòa tan hoàn toàn 8,68 g hh Fe , Mg .Zn cần dùng hết 160ml đ HCl 2M
a Tính thể tích của H2 sinh ra
b Cô cạn dd sau pứ thì thu đc bao nhiêu g muối than
bài 2 Cho 7,8 g hh kim loại Al và Mg tác dụng với HCl thu đ 8,96 lít H2 ở đktc . Hỏi khi cô cạn dd thu đc bao nhiêu g muối than
Bài 3 Hòa tan hoàn toàn 11,8 g hh X gồm Fe, Mg và Al = 1 lượng vừa đủ đ HCl loãng thu đ 11,2 lít H2 đktc và dd chứa m gam muối Tính m
Bài 2:
2Al+6HCl-->2AlCl3+3H2
Mg+2HCl-->MgCl2+H2
Theo PT trên cứ 2mol HCl tạo ra 1 mol H2
=>nHCl=nH2.2=0.4.2=0.8mol
=>mHCl=36.5.0.8=29.2g
mH2=0.4.2=0.8g
Áp dụng ĐL bảo toàn KL ta có:
mhhKL+mHCl=m muối+mH2
=> muối=7.8+29.2-0.8=36.2g
Vậy KL muối khan thu đc là 36.2 g.
Đúng 0
Bình luận (0)
Bài 2:
\(n_{H_2}=0,4mol\)
\(n_{HCl}=2n_{H_2}=0,8mol\)(2 phân tử HCl tạo 1 phân tử H2)
\(n_{Cl}=n_{HCl}=0,8mol\)
mmuối=mKim loại+mCl=7,8+0,8.35,5=36,2g
Đúng 0
Bình luận (0)
Bài 1:
\(n_{HCl}=0,32mol\)
2 phân tử HCl tạo 1 phân tử H2 nên:
\(n_{H_2}=\dfrac{1}{2}n_{HCl}=0,16mol\)
\(V_{H_2}=0,16.22,4=3,584l\)
nCl=nHCl=0,32mol
mmuối=mkim loại+mCl=8,68+0,32.35,5=20,04g
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Cho 18,6g hhX (Mg, Fe, Al) tác dụng vừa đủ với 7,841l O2 (đktc). Mặt khác cứ 0,275 mol hh trên tác dụng với dd HCl dư thu đc 7,28l H2( đktc). Tính % khối lượng mỗi kim loại trong hh X