Dẫn từ từ đến dư khí C O 2 vào dung dịch chứa 0,2 mol B a O H 2 . Sự phụ thuộc của số mol kết tủa (a mol) vào số mol khí C O 2 tham gia phản ứng (b mol) được biểu diễn như đồ thị sau:
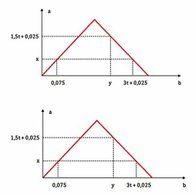
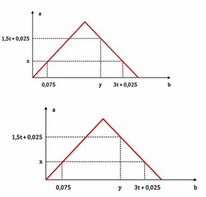
Tỉ lệ y : x là
A. 2,0
B. 2,5
C. 3,0
D. 3,5
Dẫn từ từ 1,12 lít khí CO2 (đktc) vào một dung dịch chứa 0,2 mol Ca(OH)2.a) Xác định khối lượng muối thu được sau phản ứng .b)Chất nào đã dư và dư bao nhiêu gam?(Cho biết Ca=40, C=12,O=16,H=1)
\(n_{CO_2}=0,05mol\)
\(\dfrac{n_{CO_2}}{n_{Ca\left(OH\right)_2}}=\dfrac{0,05}{0,2}=0,25< 1\)
Ca(OH)2 dư tạo muối CaCO3
CO2+Ca(OH)2\(\rightarrow\)CaCO3+H2O
\(n_{Ca\left(OH\right)_2}=n_{CaCO_3}=n_{CO_2}=0,05mol\)
\(m_{CaCO_3}=0,05.100=5g\)
\(n_{Ca\left(OH\right)_2}\left(dư\right)=0,2-0,05=0,15mol\)
\(m_{Ca\left(OH\right)_2}=0,15.74=3,7g\)
Dung dịch A chứa a mol Ca(OH)2. Hòa tan hết m gam NaOH vào dung dịch A, thu được dung dịch B. Sau đó dẫn CO2 từ từ đến dư vào dung dịch B, ta thấy lượng kết tủa biến đổi theo đồ thị như hình vẽ bên. Xác định giá trị của a và m.
nêu hiện tượng và viết phương trình phản ứng:
a)nung quặng FeS trong không khí. Thu khí thoát ra, dẫn từ từ nước vào dung dịch nước crom. cho dung dịch Ba(OH)2 vào dung dịch thu được.
b)nhỏ vài giọt dung dịch H2SO4 đặc vào cốc thủy tinh có chứa 1 ít đường ăn.
c)cho hỗn hợp bột Na2O và Al2O3(tỉ lệ 1:1) vào cốc thủy tinh chứa H2O dư.
Bài tập 1:Viết phương trình phản ứng xảy ra khi:
a. Dẫn từ từ khí SO2 vào dung dịch KOH cho đến dư
b. Dẫn từ từ khí CO2 vào dung dịch Ca(OH)2 cho đến dư
c. Dẫn từ từ khí CO2 vào dung dịch Ba(OH)2 cho đến dư
d. Dẫn từ từ khí SO2 vào dung dịch Ca(OH)2 cho đến dư
e. Dẫn từ từ khí N2O5 vào dung dịch Ca(OH)2 cho đến dư
f. Dẫn từ từ P2O5 vào dung dịch Ca(OH)2 cho đến dư
g. Dẫn từ từ P2O5 vào dung dịch NaOH cho đến dư
h. Dẫn từ từ P2O5 vào dung dịch Ba(OH)2 cho đến dư
j. Dẫn từ từ P2O5 vào nước
Bài tập 2: Viết phương trình phản ứng xảy ra khi:
a. Sắt (III) oxit tác dụng với dung dịch H2SO4, HCl, HNO3, H3PO4
b. Magie oxit tác dụng với dung dịch H2SO4, HCl, HNO3, H3PO4
c. Natri oxit tác dụng với dung dịch H2SO4, HCl, HNO3, H3PO4
d. Crom (II) oxit tác dụng với dung dịch H2SO4loãng, HCl, H3PO4
f. Sắt từ oxit tác dụng với dung dịch H2SO4loãng, HCl, H3PO4
g.Nhôm oxit tác dụng với dung dịch H2SO4, HCl, HNO3, H3PO4
h. Kẽm oxit tác dụng với dung dịch H2SO4, HCl, HNO3, H3PO4
j. Đồng (II) oxit tác dụng với dung dịch H2SO4, HCl, HNO3, H3PO4
câu 1:
a. KOH + SO2 → KHSO3
b. CO2 + Ca(OH)2 → Ca(HCO3)2
c. CO2 + Ba(OH)2 → Ba(HCO3)2
d. SO2 + Ca(OH)2 → Ca(HSO3)2
e. Ca(OH)2 + N2O5 → Ca(NO3)2 + H2O
f. P2O5 + Ca(OH)2 + H2O → Ca(H2PO4)2
g. P2O5+ 2NaOH + H2O ------> 2NaH2PO4
h. 3Ba(OH)2 + 2P2O5 = Ba(H2PO4)2 + 2BaHPO4
j. 3H2O + P2O5 → 2H3PO4
Dẫn từ từ khí CO2 đến dư vào dung dịch chứa x mol Ca(OH)2 và 2x mol NaOH. Sự phụ thuộc của khối lượng kết tủa thu được vào số mol CO2 phản ứng được biểu diễn theo đồ thị sau
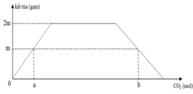
Tỉ lệ b : a là
A. 5 : 1
B. 7 : 2
C. 7 : 1
D. 6 : 1
Dung dịch X chứa 0,4 mol HCl, dung dịch Y chứa 0,2 mol NaHCO 3 và 0,3 mol Na 2 CO 3 . Nếu cho từ từ dung dịch X vào dung dịch Y thì thoát ra a mol khí . Nếu cho từ từ dung dịch Y vào dung dịch X thì thoát ra b mol khí. Giá trị của a và b lần lượt là
A. 0,10 và 0,50
B. 0,30 và 0,20
C. 0,20 và 0,30
D. 0,10 và 0,25
có dung dịch A chứa 0,2 mol NaCO3, 0,3 mol NaHCO3. dung dịch b chứa 0,5 mol HCl, tính thể tích khí bay ra ở 3 thí nghiệm sau:
TN1:Đổ rất từ từ B vào A cho đến hết
TN2: Dổ rất từ từ A vào B cho đến hết
TN3: trộn nhanh 2 dd A,B với nhau
Thêm từ từ đến hết dung dịch chứa 0,2 mol KHCO3 và 0,1 mol K2CO3 vào dung dịch chứa 0,3 mol HCl. Thể tích khí CO2 (ở đktc) thu được là
A. 3,36 lít
B. 5,04 lít
C. 4,48 lít
D. 6,72 lít
Chọn đáp án B
Nhỏ từ từ đến lúc vừa hết 0,3 mol HCl thì thấy đã dùng 2x mol KHCO3 và x mol K2CO3
Phản ứng: KHCO3 + HCl → KCl + CO2 + H2O || K2CO3 + 2HCl → 2KCl + CO2 + H2O
⇒ 2x + 2 × x = ∑nHCl phản ứng = 0,3 mol ⇒ x = 0,075 mol
⇒ ∑nCO2 = 3x = 0,225 mol ⇒ VCO2 = 0,225 × 22,4 = 5,04 lít. Chọn B
Thêm từ từ đến hết dung dịch chứa 0,2 mol KHCO3 và 0,1 mol K2CO3 vào dung dịch chứa 0,3 mol HCl. Thể tích khí CO2 (ở đktc) thu được là
A. 3,36 lít
B. 5,04 lít
C. 4,48 lít
D. 6,72 lít
Nhỏ từ từ đến lúc vừa hết 0,3 mol HCl thì thấy đã dùng 2x mol KHCO3 và x mol K2CO3
Phản ứng: KHCO3 + HCl → KCl + CO2 + H2O || K2CO3 + 2HCl → 2KCl + CO2 + H2O
⇒ 2x + 2 × x = ∑nHCl phản ứng = 0,3 mol ⇒ x = 0,075 mol
⇒ ∑nCO2 = 3x = 0,225 mol ⇒ VCO2 = 0,225 × 22,4 = 5,04 lít
Đáp án B