(Giải thích giùm em bài này vs ạ!!!)
Hiệu ứng nhiệt của phản ứng thu nhiệt có đặc điểm là:
A. \(\Delta_fH_{298}^0>0\)
B. \(\Delta_fH^0_{298}< 0\)
C. \(\Delta_fH^0_{298}>100\)
D. \(\Delta_fH^0_{298}=1000\)
(Giải thích giùm em bài này vs ạ!!!)
Hiệu ứng nhiệt của phản ứng thu nhiệt có đặc điểm là:
A. \(\Delta_fH_{298}^0>0\)
B. \(\Delta_fH^0_{298}< 0\)
C. \(\Delta_fH^0_{298}>100\)
D. \(\Delta_fH^0_{298}=1000\)
có bao nhiêu phát biểu đúng?
1. điều kiện chuẩn là điều kiện ứng với 1 bar ( đối với chất lỏng )
2. độ biến thiên enthalpy của một quá trình không thay đổi theo nhiệt độ
3. tính chất của enthalpy đặc trưng cho 1 hệ riêng biệt
4. ý nghĩa của enthalpy là xác định hiệu ứng nhiệt trong quá trình đẳng áp, đẳng nhiệt
A.2 B.4 C.1 D.3
Mạnh mẽ hơn Nesbitt?
Với a, b, c là các số thực sao cho: \(a+b+c>0,\text{ }ab+bc+ca>0,\text{ }\left(a+b\right)\left(b+c\right)\left(c+a\right)>0\) thì:
\(\frac{a}{b+c}+\frac{b}{c+a}+\frac{c}{a+b}-\frac{3}{2}\ge\left(\Sigma ab\right)\left(\Sigma\frac{1}{\left(a+b\right)^2}\right)-\frac{9}{4}\)
Chứng minh: \(4\left(a+b+c\right)\left(a+b\right)^2\left(b+c\right)^2\left(c+a\right)^2\cdot\left(\text{VT}-\text{VP}\right)\)
\(=\left(a+b\right)\left(b+c\right)\left(c+a\right)\left[\Sigma\left(ab+bc-2ca\right)^2+\left(ab+bc+ca\right)\Sigma\left(a-b\right)^2\right]\)
\(+\left(a+b+c\right)\left(a-b\right)^2\left(b-c\right)^2\left(c-a\right)^2\ge0\)
Bất đẳng thức trên đúng với mọi số thực a, b, c. Ai có thể chứng minh?
Câu28
Áp dụng Ct tính độ hấp phụ \(T=-\frac{_C}{RT}.\frac{d\sigma}{dC}\)
vs \(\frac{d\sigma}{dC}=-16,7.10^{-3}.21,5.\frac{1}{1+21,5C}\)
Đến đây em rất lúng túng để thay số do em ko rõ cách đổi đơn vị C [g/l] và \(\sigma\left(\frac{N}{m}\right)\)như thế nào cho phù hợp.
Thầy nói lại em biết với ạ.Em cám ơn thầy
Bài này thầy đã chữa trên lớp, ko giải thích lại.
Câu 30: Xét quá trình đốt cháy khí propane C3H8(g):
C3H8(g) + 5O2(g) 3CO2(g) + 4H2O(g)
a) Tính biến thiên enthalpy chuẩn của phản ứng dựa vào bảng nhiệt tạo thành của hợp chất và dựa vào dựa vào bảng năng lượng liên kết.
Biết nhiệt tạo thành của C3H8(g); CO2(g) và H2O(g) lần lượt là : 105,00; 393,50 và 241,82 kJ/mol.
Biết EC-H = 418 kJ/mol; EC-C = 346 kJ/mol; EO=O = 494 kJ/mol; EC=O = 732 kJ/mol và EO-H = 459 kJ/mol.
b) So sánh hai giá trị đó và nếu có sự khác biệt, hãy giải thích tại sao lại có sự khác biệt đó ?
Cho biết phản ứng tạo thành 2 mol HCl(g) ở điều kiện chuẩn sau đây tỏa ra 184,6 kJ:
H2(g) + Cl2(g) → 2HCl(g) (*)
Những phát biểu sau dưới đây là đúng?
A. Nhiệt tạo thành của HCl là -184,6 kJ.mol-1.
B. Biến thiên enthalpy phản ứng (*) là -184,6 kJ.
C. Nhiệt tạo thành của HCl là -92,3 kJ.mol-1.
D. Biến thiên enthalpy phản ứng (*) là -92,3 kJ.
A. Sai vì đó là nhiệt tạo thành của 2 mol HCl
B. Đúng vì (*) là phản ứng tỏa nhiệt nên enthalpy mang giá trị âm
C. Đúng vì nhiệt tạo thành tỉ lệ với số mol chất tạo thành, đây là phản ứng tỏa nhiệt nên mang giá trị âm
D. Sai vì phản ứng (*) ứng với 2 mol
=> Đáp án B, C đúng
c) Tính biến thiên enthanpy của phản ứng tạo thành ammonia (sử dụng năng lượng liên kết).
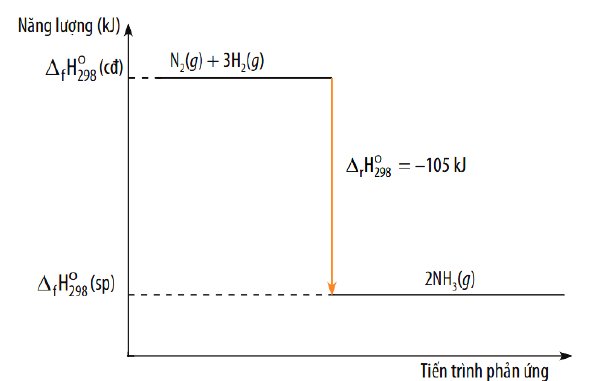
Cho biết phản ứng thu nhiệt hay toả nhiệt và vẽ sơ đồ biểu diễn biến thiên enthalpy của phản
ứng 3H2 (g) + N2 (g) → 2NH3 (g)
Liên kết Eb (kJ/ mol)
H – N 386
H – H 436
N ≡ N 945
\(\Delta_rH^{^{ }o}_{298}=3\cdot436+945-2\left(3\cdot386\right)=-63kJ\cdot mol^{-1}\)
Sơ đồ:
Giúp gấp vs ạ:
Chứng minh rằng với \(\text{|}x\text{|}\) rất bé so với \(a>0\left(\text{| }x\text{| }\le a\right)\) ta có:
\(\sqrt{a^2+x}\approx a+\dfrac{x}{2a}\left(x>0\right)\)
Áp dụng công thức trên, hãy tính gần đúng số sau:
\(\sqrt{146}\)
Tham khảo: Bài 4.8 trang 211 Sách bài tập Đại số và giải tích 11: Chứng minh rằng với |x| rất bé so với
Tham khảo cách giải:
Đặt \(x\left(y\right)=\sqrt{a^2+x}\) ta có:
\(y'\left(x\right)=\dfrac{\left(a^2+x\right)'}{2\sqrt{a^2+x}}=\dfrac{1}{2\sqrt{a^2+x}}\)
Từ đó:
\(\Delta y=y\left(x\right)-y\left(0\right)\approx y'\left(0\right)x\)
\(\Rightarrow\sqrt{a^2+x}-\sqrt{a^2+0}\approx\dfrac{1}{2\sqrt{a^2+0}}x\)
\(\Rightarrow\sqrt{a^2+x}-a\approx\dfrac{x}{2a}\)
\(\Rightarrow\sqrt{a^2+x}\approx a+\dfrac{x}{2a}\)
Áp dụng :
\(\sqrt{146}=\sqrt{12^2+2}\)
\(\approx12+\dfrac{2}{2.12}\approx12,0833\)
Quá trình lên men rượu vang xảy ra phản ứng hóa học sau
C6H12O6(s) ----> 2C2H5OH(1)+2CO2(g)
a. Tính biến thiên enthalpy chuẩn của phản ứng theo nhiệt tạo thành chuẩn của các chất (biết nhiệt tạo thành chuẩn của C6H12O6(s) C2H5OH(l); CO2(g) có giá trị lần lượt là –1274kJ/mol: 277,69 kJ/mol 393,51kJ/mol
b, Tính lượng nhiệt tòa ra hay thu vào khi lên men 3 kg nhỏ (chứa khoảng 7% đường glucose) ở điều kiện chuẩn
a) Xác định biến thiên enthalpy của phản ứng sau ở điều kiện chuẩn:
4FeS2 (s) + 11O2 (g) → 2Fe2O3 (s) + 8SO2 (g)
Biết nhiệt tạo thành ΔrH0298 của các chất FeS2(s), Fe2O3(s) và SO2(g) lần lượt là -177,9 kJ/mol,
-825,5 kJ/mol và -296,8 kJ/mol.
\(\Delta_rH^o_{298}=2\left(-825,5\right)+8\left(-296,8\right)-4\left(-177,9\right)\\ \Delta_rH^o_{298}=-3313,8\left(kJ\right)\)