Hỗn hợp khí SO 2 và O 2 có tỉ khối hơi đối với metan ( CH 4 ) bằng 3. Tính thể tích khí O 2 ần thêm vào 20 lít hỗn hợp trên để thu được hỗn hợp khí có tỉ khối hơi bằng 2,5.

Những câu hỏi liên quan
Bài 1. a) Tính tỉ khối hơi của khí SO2 so với khí O2 N2, SO3, CO, N2O, NO2.b) Tính tỉ khối hơi của hỗn hợp khí A gồm SO2 và O2 có tỉ lệ mol 1:1 đối với khí O2.Bài 2. a) Tính tỉ khối hơi của hỗn hợp khí X gồm hai khí N2 và CO đối với khí metan CH4. Hỗn hợp X nặng hay nhẹ hơn không khí?b) Tính tỉ khối hơi của hỗn hợp Y đồng khối lượng gồm khí C2H4 (etilen), N2 và khí CO so với khí H2.c) Hỗn hợp khí X gồm: NO, NxO, CH4. Trong đó NO chiếm 30% về thể tích, NxO chiếm 30% còn lại là CH4. Trong hỗn hợp...
Đọc tiếp
Bài 1. a) Tính tỉ khối hơi của khí SO2 so với khí O2 N2, SO3, CO, N2O, NO2.
b) Tính tỉ khối hơi của hỗn hợp khí A gồm SO2 và O2 có tỉ lệ mol 1:1 đối với khí O2.
Bài 2. a) Tính tỉ khối hơi của hỗn hợp khí X gồm hai khí N2 và CO đối với khí metan CH4. Hỗn hợp X nặng hay nhẹ hơn không khí?
b) Tính tỉ khối hơi của hỗn hợp Y đồng khối lượng gồm khí C2H4 (etilen), N2 và khí CO so với khí H2.
c) Hỗn hợp khí X gồm: NO, NxO, CH4. Trong đó NO chiếm 30% về thể tích, NxO chiếm 30% còn lại là CH4. Trong hỗn hợp CH4 chiếm 22,377% về khối lượng. Xác định công thức hoá học của NxO. Tính tỷ khối của X so với không khí
Bài 2:
a) Vì khối lượng mol của N2 và CO đều bằng 28 và lớn hơn khối lượng mol của khí metan CH4 (28>16)
=> \(d_{\dfrac{hhX}{CH_4}}=\dfrac{28}{16}=1,75\)
Hỗn hợp X nhẹ hơn không khí (28<29)
b)
\(M_{C_2H_4}=M_{N_2}=M_{CO}=28\left(\dfrac{g}{mol}\right)\\ \rightarrow M_{hhY}=28\left(\dfrac{g}{mol}\right)\\ d_{\dfrac{Y}{H_2}}=\dfrac{28}{2}=14\)
c) \(\%V_{NO}=100\%-\left(30\%+30\%\right)=40\%\\ \rightarrow\%n_{CH_4}=40\%\\ Vì:\%m_{CH_4}=22,377\%\\ Nên:\dfrac{30\%.16}{40\%.30+30\%.16+30\%.\left(x.14+16\right)}=22,377\%\\ \Leftrightarrow x=-0,03\)
Sao lại âm ta, để xíu anh xem lại như nào nhé.
Đúng 2
Bình luận (4)
Bài 1:
\(a.\\ d_{\dfrac{SO_2}{O_2}}=\dfrac{64}{32}=2\\ d_{\dfrac{SO_2}{N_2}}=\dfrac{64}{28}=\dfrac{16}{7}\\ d_{\dfrac{SO_2}{SO_3}}=\dfrac{64}{80}=0,8\\ d_{\dfrac{SO_2}{CO}}=\dfrac{64}{28}=\dfrac{16}{7}\\ d_{\dfrac{SO_2}{N_2O}}=\dfrac{64}{44}=\dfrac{16}{11}\\ d_{\dfrac{SO_2}{NO_2}}=\dfrac{64}{46}=\dfrac{32}{23}\\ b.M_{hhA}=\dfrac{1.64+1.32}{1+1}=48\left(\dfrac{g}{mol}\right)\\ d_{\dfrac{hhA}{O_2}}=\dfrac{48}{32}=1,5\)
Đúng 4
Bình luận (2)
Tỉ khối của hỗn hợp khí A gồm khí metan (CH4) và Oxi đối với khí Hidro là 14,4. Bật tia lửa điện để đốt cháy hoàn toàn khí metan thì thu được hỗn hợp khí B và hơi nước. Tính tỉ khối của B so với A.
Gọi số mol CH4, O2 là a, b (mol)
Có: \(\overline{M}_A=\dfrac{16a+32b}{a+b}=14,4.2=28,8\left(g/mol\right)\)
=> 12,8a = 3,2b
=> a : b = 1 : 4
Giả sử A gồm 1 mol CH4 và 4 mol O2
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
Xét tỉ lệ: \(\dfrac{1}{1}< \dfrac{4}{2}\) => CH4 hết, O2 dư
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
1---->2----------->1
=> \(B\left\{{}\begin{matrix}CO_2:1\left(mol\right)\\O_{2\left(dư\right)}=4-2=2\left(mol\right)\end{matrix}\right.\)
=> \(\overline{M}_B=\dfrac{1.44+2.32}{1+2}=36\left(g/mol\right)\)
=> \(d_{B/A}=\dfrac{36}{28,8}=1,25\)
Đúng 1
Bình luận (0)
hỗn hợp B gồm 2 khí N2O và O2 có tỉ khối đối với khí metan CH4 là 2,5 . tính phần trăm thể tích của mỗi khí trong hỗn hợp B. ( đề hsg hóa)
`d_[B//CH_4]=[\overline{M_B}]/16=2,5`
`=>\overline{M_B}=40`
`=>[n_[N_2 O]]/[n_[O_2]]=|[40-32]/[40-44]|=2`
Vì phần trăm của thể tích mỗi khí trog hỗn hợp `B` bằng phần trăm của số mol mỗi khí trong hỗn hợp `B`
`=>%V_[N_2 O]=2/[2+1] .100~~66,67%`
`=>%V_[O_2]~~100-66,67~~33,33%`
Đúng 9
Bình luận (0)
Hỗn hợp khí và hơi gồm metan, anđehit axetic và axit acrylic có tỉ khối so với H2 là 31,8. Đốt cháy hoàn toàn 0,05 mol hỗn hợp rồi hấp thụ toàn bộ sản phẩm cháy vào bình đựng dung dịch Ca(OH)2 (dư) thì khối lượng bình tăng thêm m gam. Giá trị của m là A. 7,34 B. 9,54 C. 5,54 D. 7,74
Đọc tiếp
Hỗn hợp khí và hơi gồm metan, anđehit axetic và axit acrylic có tỉ khối so với H2 là 31,8. Đốt cháy hoàn toàn 0,05 mol hỗn hợp rồi hấp thụ toàn bộ sản phẩm cháy vào bình đựng dung dịch Ca(OH)2 (dư) thì khối lượng bình tăng thêm m gam. Giá trị của m là
A. 7,34
B. 9,54
C. 5,54
D. 7,74
Đáp án D
CH4; C2H4O; C3H4O2
Đặt công thức chung là: Cn+1H4On => 28n+16 = 63,6 => n = 1,7
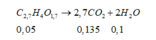
m b i n h tan g = m C O 2 + m H 2 O = 0 , 135 . 44 + 0 , 1 . 18 = 7 , 74 g a m
Đúng 0
Bình luận (0)
11,2 lít hỗn hợp X gồm hiđro và metan CH4 (đktc) có tỉ khối so với oxi là 0,325.
a/ Xác định % thể tích các khí trong X?
b/ Đốt cháy hoàn toàn hỗn hợp với 32 gam khí oxi. Phản ứng xong, làm lạnh để hơi nước ngưng tụ hết được hỗn hợp khí Y.
- Viết phương trình hoá học xảy ra.
- Tính thể tích các khí trong Y.
a) Gọi số mol H2, CH4 là a, b
=> \(a+b=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(M_X=\dfrac{2a+16b}{a+b}=0,325.32=10,4\)
=> a = 0,2 ; b = 0,3
=> \(\left\{{}\begin{matrix}\%V_{H_2}=\dfrac{0,2}{0,5}.100\%=40\%\\\%V_{CH_4}=\dfrac{0,3}{0,5}.100\%=60\%\end{matrix}\right.\)
b) \(n_{O_2}=\dfrac{32}{32}=1\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,3--->0,6------->0,3
2H2 + O2 --to--> 2H2O
0,2-->0,1
=> \(\left\{{}\begin{matrix}V_{CO_2}=0,3.22,4=6,72\left(l\right)\\V_{O_2\left(dư\right)}=\left(1-0,6-0,1\right).22,4=6,72\left(l\right)\end{matrix}\right.\)
Đúng 4
Bình luận (0)
1. Hỗn hợp khí X gồm O2 và CO2 có tỉ khối hơi so với hidro là 18. Tính số mol mỗi có trong 4,48 lít hỗn hợp khí X (đktc)
2. Tính số mol mỗi khí có trong 5,6 lít (đktc) hỗn hợp khí A gồm O2 và NO2 có tỉ khối so với hidro là 17,4
Đặt \(n_{O_2}=x;n_{CO_2}=y\)
\(n_X=\dfrac{4,48}{22,4}=0,2\left(mol\right)\Leftrightarrow x+y=0,2\)
Ta có: \(16x+44y=\left(x+y\right).18.2\)
\(\Leftrightarrow2y=5x\)
\(\Leftrightarrow\dfrac{y}{5}=\dfrac{x}{2}\)
Mà x+y=0,2
\(\Rightarrow\dfrac{y}{5}=\dfrac{x}{2}=\dfrac{x+y}{5+2}=\dfrac{0,2}{7}=0,0286\)
\(\Rightarrow y=5.0,0286=0,143\left(mol\right);x=0,2-0,143=0,057\left(mol\right)\)
Đúng 1
Bình luận (0)
dẫn 5,6 lít hỗn hợp X metan và axetilen vào lượng dư dung dịch trong NH3,thu được 24g kết và có V ml khí thoát đktc .tính V
2. Ankan A có tỉ khối hơi so với 2, xác định ctpt . viết ctct gọi tên A và viết pthh phản ứng với cl .tỉ lệ 1.1 ánh sáng
Tính tỉ khối hơi của hỗn hợp khí A gồm SO2 và O2 có tỉ lệ mol là 1/2 đối với khí O2.
Biết 11,2 lít (ở đktc) hỗn hợp X gồm hiđro và metan (CH4) có tỉ khối so với oxi là 0,325. Đốt hỗn hợp với 28,8 gam khí oxi. Phản ứng xong, làm lạnh để hơi nước ngưng tụ hết được hỗn hợp khí Y.
a. Viết phương trình hoá học xảy ra. Xác định % thể tích các khí trong X.
b. Xác định % thể tích và % khối lượng của các khí trong Y.

















