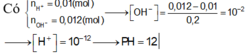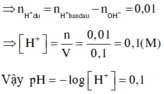Trộn 100ml dung dịch có pH=1 gồm HCl và H2SO4 với 100ml dung dịch KOH nồng độ x mol/lít, ghu được 200ml dung dịch có pH=13. Giá trị của x là (biết trong mọi dung dịch [H+] [OH-] = 10-14, bỏ qua sự điện li của nước)

Những câu hỏi liên quan
Trộn 100ml dung dịch có pH =1 gồm HCl và HNO3 với 100ml dung dịch NaOH nồng độ a mol/l thu được 200ml dung dịch có pH=12 giá trị của a là
Dung dịch axit ban đầu có [H+] = 0,1 M
⇒ nH+= 0,1.0,1 = 0,01 mol
Dung dịch sau phản ứng có pH = 12
⇒ dư bazơ và có pOH =14 – 12 = 2
⇒ [OH-] = 0,01M
⇒ nOH− dư = 0,002 mol
Phản ứng trung hòa:
nH+phản ứng = nOH−phản ứng = 0,01 mol
⇒ nNaOH ban đầu = nOH−phản ứng + nOH− dư
= 0,01 + 0,002 = 0,012 mol
⇒ a = 0,12M
Đúng 2
Bình luận (0)
1. Tính pH của 100ml dung dịch X có hòa tan 2,24 lít khí HCl (đktc)2. Tính nồng độ mol/l của các dung dịch:a) Dung dịch H2SO4 có pH 4.b) Dung dịch KOH có pH 11.3. Pha loãng 200ml dung dịch Ba(OH)2 với 1,3 lít nước thu được dung dịch có pH 12. Tính nồng độ mol/l của dung dịch Ba(OH)2 ban đầu, biết rằng Ba(OH)2 phân ly hoàn toàn. 4. Pha loãng 10ml HCl với nước thành 250ml. Dung dịch thu được có pH 3. Hãy tính nồng độ mol/l của HCl trước khi pha loãng và pH...
Đọc tiếp
1. Tính pH của 100ml dung dịch X có hòa tan 2,24 lít khí HCl (đktc)
2. Tính nồng độ mol/l của các dung dịch:
a) Dung dịch H2SO4 có pH = 4.
b) Dung dịch KOH có pH = 11.
3. Pha loãng 200ml dung dịch Ba(OH)2 với 1,3 lít nước thu được dung dịch có pH = 12. Tính nồng độ mol/l của dung dịch Ba(OH)2 ban đầu, biết rằng Ba(OH)2 phân ly hoàn toàn.
4. Pha loãng 10ml HCl với nước thành 250ml. Dung dịch thu được có pH = 3. Hãy tính nồng độ mol/l của HCl trước khi pha loãng và pH của dung dịch đó.
5. Trộn 100ml dung dịch HCl 0,25M với 300ml dung dịch HNO3 0,05M. pH của dung dịch thu được là:
6. Trộn lẫn 3 dung dịch NaOH 0,02M; KOH 0,03M và Ba(OH)2 0,01M theo tỉ lệ thể tích tương ứng là 1:1:2 thu được dung dịch có pH là bao nhiêu?
7. Phải thêm bao nhiêu ml dung dịch HCl pH = 2 vào 90 ml nước để được dung dịch có pH = 3?
Phải thêm bao nhiêu ml nước vào 10 ml dung dịch NaOH 0,1M để thu dung dịch có pH = 12?
2. Tính nồng độ mol/l của các dung dịch:
a) Dung dịch H2SO4 có pH = 4.
\(pH=4\Rightarrow\left[H^+\right]=10^{-4}M\)
=> \(CM_{H_2SO_4}=\dfrac{\left[H^+\right]}{2}=\dfrac{10^{-4}}{2}=5.10^{-5M}\)
b) Dung dịch KOH có pH = 11.
\(pH=11\Rightarrow pOH=14-11=3\)
=> \(\left[OH^-\right]=10^{-3}=CM_{KOH}\)
Đúng 2
Bình luận (0)
3. Pha loãng 200ml dung dịch Ba(OH)2 với 1,3 lít nước thu được dung dịch có pH = 12. Tính nồng độ mol/l của dung dịch Ba(OH)2 ban đầu, biết rằng Ba(OH)2 phân ly hoàn toàn.
Đặt CM Ba(OH)2 = xM
=> \(n_{Ba\left(OH\right)_2}=0,2x\left(mol\right)\)
\(V_{sau}=V_{Ba\left(OH\right)_2}+V_{H_2O}=0,2+1,3=1,5\left(l\right)\)
pH=12 => pOH=2 => \(\left[OH^-\right]=10^{-2}M\)
\(Ba\left(OH\right)_2\rightarrow Ba^{2+}+2OH^-\)
0,2x----------------------------->0,4x
=> \(\left[OH^-\right]=\dfrac{0,4x}{1,5}=10^{-2}\)
=> x=0,0375M
Vậy nồng độ mol/l của dung dịch Ba(OH)2 ban đầu là 0,0375M
Đúng 2
Bình luận (0)
1. Tính pH của 100ml dung dịch X có hòa tan 2,24 lít khí HCl (đktc)
\(n_{HCl}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
=> \(n_{H^+}=0,1\left(mol\right)\)
=> \(\left[H^+\right]=\dfrac{0,1}{0,1}=1M\Rightarrow pH=0\)
Xem lại đề câu này nha bạn
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Cho 100ml dung dịch X chứa KOH 0,13M và
Ba
(
OH
)
2
0,1M tác dụng với 200ml dung dịch
H
2
SO
4
x mol/lít. Sau khi phản ứng kết thúc thu được dung dịch có pH 2. Giá trị của x là A. 0,03 B. 0,09 C. 0,06 D. 0,045
Đọc tiếp
Cho 100ml dung dịch X chứa KOH 0,13M và Ba ( OH ) 2 0,1M tác dụng với 200ml dung dịch H 2 SO 4 x mol/lít. Sau khi phản ứng kết thúc thu được dung dịch có pH = 2. Giá trị của x là
A. 0,03
B. 0,09
C. 0,06
D. 0,045
Chọn B
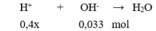
Dung dịch sau phản ứng có pH = 2 < 7 nên dung dịch sau phản ứng có H + dư
→ 0,4x – 0,033 = 10 - 2 .0,3 → x = 0,09
Đúng 0
Bình luận (0)
Tính số mol, nồng độ mol ion H+ và OH- và pH của dung dịch axit b) HNO3 0,04M c) dung dịch HCl 0.001M d) dung dịch H2SO4 0,003M e) dung dịch HNO3 có pH=2 f) dung dịch H2SO4 có pH=4 g) 200ml dung dịch H2SO4 0,01M + 100ml dung dịch HCl 0,05M Giúp em với ạ
Trộn 100ml dung dịch có pH=1 gồm HCl và HNO3 với 100ml dung dịch NaOH nồng độ a (mol/l) thu được 200ml dung dịch có pH=12 . Giá trị của a là ?
Ta có: \(pH=1\Rightarrow\left[H^+\right]=0,1\Rightarrow n_{H^+}=0,1.0,1=0,01\left(mol\right)\)
Sau pư, pH = 12 ⇒ OH- dư.
\(\Rightarrow\left[OH^-\right]_{\left(dư\right)}=\frac{10^{-14}}{10^{-12}}=0,01\Rightarrow n_{OH^-\left(dư\right)}=0,01.0,2=0,002\left(mol\right)\)
PT ion: \(H^++OH_{\left(pư\right)}^-\rightarrow H_2O\)
_______0,01 → 0,01 (mol)
\(\Rightarrow\Sigma n_{OH^-}=0,01+0,002=0,012\left(mol\right)\)
\(\Rightarrow\left[OH^-\right]=\frac{0,012}{0,1}=0,12M=a\)
Bạn tham khảo nhé!
Cho 100ml dung dịch HCl 0,1M vào 100ml dung dịch Ba(OH)2 0,06M thu được 200ml dung dịch X. Giá trị pH của dung dịch X là:Cho 100ml dung dịch HCl 0,1M vào 100ml dung dịch Ba(OH)2 0,06M thu được 200ml dung dịch X. Giá trị pH của dung dịch X là: A. 13 B. 2 C. 12 D. 7
Đọc tiếp
Cho 100ml dung dịch HCl 0,1M vào 100ml dung dịch Ba(OH)2 0,06M thu được 200ml dung dịch X. Giá trị pH của dung dịch X là:Cho 100ml dung dịch HCl 0,1M vào 100ml dung dịch Ba(OH)2 0,06M thu được 200ml dung dịch X. Giá trị pH của dung dịch X là:
A. 13
B. 2
C. 12
D. 7
Dung dịch X có chứa 0,07 mol Na+; 0,02 mol và x mol OH-. Dung dịch Y có chứa ; và y mol H+. Tổng số mol và là 0,04 mol. Trộn X với Y thu được 100ml dung dịch Z. Bỏ qua sự điện li của nước, pH của dung dịch thu được là: A. l B.2 C. 12. D.13
Đọc tiếp
Dung dịch X có chứa 0,07 mol Na+; 0,02 mol và x mol OH-. Dung dịch Y có chứa ; và y mol H+. Tổng số mol và là 0,04 mol. Trộn X với Y thu được 100ml dung dịch Z. Bỏ qua sự điện li của nước, pH của dung dịch thu được là:
A. l
B.2
C. 12.
D.13
Trộn 100ml dung dịch Ba(OH)2 0,5M và 100ml dung dịch KOH 0,5M thu dung dịch X. Cho X tác dụng với 100ml dung dịch H2SO4 1M. Khối lượng kết tủa và giá trị pH của dung dịch thu được sau phản ứng:
$n_{Ba^{2+}} = 0,1.0,5 = 0,05 < n_{SO_4^{2-}} = 0,1$ nên $SO_4^{2-}$ dư
$n_{BaSO_4} = n_{Ba^{2+}} = 0,05(mol)$
$m_{BaSO_4} = 0,05.233 = 11,65(gam)$
$n_{OH^-} = 0,1.0,5.2 + 0,1.0,5 = 0,15(mol)$
$n_{H^+} = 0,1.2 = 0,2(mol)$
$H^+ + OH^- \to H_2O$
$n_{H^+\ dư} = 0,2 - 0,15 = 0,05(mol)$
$V_{dd} = 0,1 + 0,1 + 0,1 = 0,3(lít)$
$[H^+] = \dfrac{0,05}{0,3} = \dfrac{1}{6}M$
$pH = -log( \dfrac{1}{6} ) = 0,778$
Đúng 1
Bình luận (1)
\(n_{Ba^{2+}}=0.1\cdot0.5=0.05\left(mol\right)\)
\(n_{OH^-}=0.1\cdot0.5\cdot2+0.1\cdot0.5=0.15\left(mol\right)\)
\(n_{H^+}=2\cdot0.1\cdot1=0.2\left(mol\right)\)
\(n_{SO_4^{2-}}=0.1\left(mol\right)\)
\(Ba^{2+}+SO_4^{2-}\rightarrow BaSO_4\)
\(0.05.........0.05.............0.05\)
\(SO_4^{2-}dư\)
\(m_{\downarrow}=0.05\cdot233=11.65\left(g\right)\)
\(H^++OH^-\rightarrow H_2O\)
\(0.15.......0.15\)
\(n_{H^+\left(dư\right)}=0.2-0.15=0.05\left(mol\right)\)
\(\left[H^+\right]=\dfrac{0.05}{0.1+0.1+0.1}=\dfrac{1}{6}\)
\(pH=-log\left(\dfrac{1}{6}\right)=0.77\)
Đúng 0
Bình luận (0)