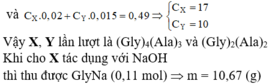Đót cháy hoàn toàn m gam sắt cần dùng 8,96 lít khí oxi (đktc) thu được m1 gam oxit . Tính m , m1

Những câu hỏi liên quan
Đót cháy m1 gam lưu huỳnh cần m2 gam khí Oxi, thu được 8,96 lít khí SO2(đktc). Tính m1 và m2
S+O2->SO2
nSO2=0.4(mol)
Theo pthh nS=nO2=nSO2->nS=nO2=nSO2=0.4(mol)
m1=0.4*32=12.8(g)
m2=0.4*32=12.8(g)
Đúng 0
Bình luận (0)
đốt cháy hoàn toàn 6,5 gam kẽm cần dùng hết V lít khí oxi ở đktc và thu đc m1 gam kẽm oxit. Tính gt của V và m1?(Zn=65,O=16)
\(n_{Zn}=\dfrac{6.5}{65}=0.1\left(mol\right)\)
\(2Zn+O_2\underrightarrow{^{^{t^0}}}2ZnO\)
\(0.1.......0.05.......0.1\)
\(V_{O_2}=0.05\cdot22.4=1.12\left(l\right)\)
\(m_{ZnO}=0.1\cdot81=8.1\left(g\right)\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn m1 gam khí etilen(C2H4) cần 7,84 lít khí oxi (đktc) thu được m2 lít khí CO2(đktc) và m3 gam H2O. Tính m1+m2+m3
Đốt cháy hoàn toàn m1 gam khí ãetilen(C2H2) cần V lít khí oxi(đktc) thu được 11,2 lít khí Co2(đktc) và m2 gam H2O. Tính m1+m2 và V
C2H2 + \(\frac{5}{2}\)O2 => (to) 2CO2 + H2O
0.25 0.625 0.5 0.25 (mol)
nCO2 = V/22.4 = 11.2/22.4 = 0.5 (mol);
m1 = n.M = 0.25 x 26 = 6.5 (g);
m2 = n.M = 0.25 x 18 = 4.5 (g);
m1 + m2 = 6.5 + 4.5 = 11 (g);
V = VO2 = n.22.4 = 0.625x22.4=14(l)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn m gam kim loại sắt cần dùng 4,48lit khí oxi(ở đktc) a.tính m b.khối lượng oxit sắt thu được là bao nhiêu gam? c.để có lượng oxit trên thì cần phải lấy bao nhiêu lít không khí? Biết oxit chiếm 20% thể tích không khí.
a) \(n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: 3Fe + 2O2 --to--> Fe3O4
0,3<---0,2-------->0,1
=> m = 0,3.56 = 16,8 (g)
b) mFe3O4 = 0,1.232 = 23,2 (g)
c) Vkk = 4,48 : 20% = 22,4 (l)
Đúng 3
Bình luận (0)
nO2 = 4,48/22,4 = 0,2 (mol)
PTHH: 3Fe + 2O2 -> (t°) Fe3O4
Mol: 0,3 <--- 0,2 ---> 0,1
mFe = 0,3 . 56 = 16,8 (g)
mFe3O4 = 0,1 . 232 = 23,2 (g)
Vkk = 4,48 . 5 = 22,4 (l)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn a gam sắt trong 8,96 lít khí oxi (đktc) thu được oxit sắt từ. Giá trị của a là (O = 16; Fe = 56)
\(n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: 3Fe + 2O2 --to--> Fe3O4
0,6<--0,4
=> mFe = 0,6.56 = 33,6(g)
Đúng 4
Bình luận (0)
\(n_{O_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
\(3Fe+2O_2\underrightarrow{^{^{t^0}}}Fe_3O_4\)
\(0.6......0.4\)
\(m_{Fe}=0.6\cdot56=33.6\left(g\right)\)
Đúng 4
Bình luận (0)
\(n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
\(PTHH:3Fe+2O_2->Fe_3O_4\)
0,13 0,2 0,4
\(m_{Fe}=0,13.56=7,28\left(g\right)\)
Đúng 0
Bình luận (1)
Đốt cháy hoàn toàn m1 gam este Z đơn chức , mạch hở có 1 nối 3 C C , cần dùng 8,96 lít O2 sau pư thu đc 8,96 lít CO2 và m2 gam H2O. Giá trị m1+m2 ?
Gọi CTPT của Z là $C_nH_{2n-4}O_2$
$n_{O_2} = 0,4(mol) ; n_{CO_2} = 0,4(mol)$
Bảo toàn electron :$n_Z.(4n + 2n - 4 - 2.2) = 4n_{O_2}$
Bảo toàn C : $n_Z.n = n_{CO_2}$
Suy ra:
$\dfrac{0,4.4}{6n-8} = \dfrac{0,4}{n} \Rightarrow n = 4$
Suy ra: Z là $C_4H_4O_2$
$n_Z = \dfrac{0,4}{4} = 0,1(mol)$
Bảo toàn H : $n_{H_2O} = 2n_Z = 0,2(mol)$
Suy ra : $m_1 + m_2 = 0,1.84 + 0,2.18 = 12(gam)$
Đúng 2
Bình luận (0)
Hỗn hợp P gồm hai peptit mạch hở: X (CnHmN7O8) và Y (CxHyN4O5). Đốt cháy hoàn toàn 13,29 gam hỗn hợp P cần dùng vừa đủ 13,104 lít khí O2 (đktc) thu được khí CO2, H2O và 2,24 lít khí N2. Thủy phân hoàn toàn 13,29 gam P trong dung dịch NaOH dư thu được m1 gam muối của glyxin và m2 gam muối của alanin. Giá trị của m1 là A. 10,67 B. 10,44 C. 8,73 D. 12,61
Đọc tiếp
Hỗn hợp P gồm hai peptit mạch hở: X (CnHmN7O8) và Y (CxHyN4O5). Đốt cháy hoàn toàn 13,29 gam hỗn hợp P cần dùng vừa đủ 13,104 lít khí O2 (đktc) thu được khí CO2, H2O và 2,24 lít khí N2. Thủy phân hoàn toàn 13,29 gam P trong dung dịch NaOH dư thu được m1 gam muối của glyxin và m2 gam muối của alanin. Giá trị của m1 là
A. 10,67
B. 10,44
C. 8,73
D. 12,61
Hỗn hợp P gồm hai peptit mạch hở: X (CnHmN7O8) và Y (CxHyN4O5). Đốt cháy hoàn toàn 13,29 gam hỗn hợp P cần dùng vừa đủ 13,104 lít khí O2 (đktc) thu được khí CO2, H2O và 2,24 lít khí N2. Thủy phân hoàn toàn 13,29 gam P trong dung dịch NaOH dư thu được m1 gam muối của glyxin và m2 gam muối của alanin. Giá trị của m1 là A. 10,67 B. 10,44 C. 8,73 D. 12,61
Đọc tiếp
Hỗn hợp P gồm hai peptit mạch hở: X (CnHmN7O8) và Y (CxHyN4O5). Đốt cháy hoàn toàn 13,29 gam hỗn hợp P cần dùng vừa đủ 13,104 lít khí O2 (đktc) thu được khí CO2, H2O và 2,24 lít khí N2. Thủy phân hoàn toàn 13,29 gam P trong dung dịch NaOH dư thu được m1 gam muối của glyxin và m2 gam muối của alanin. Giá trị của m1 là
A. 10,67
B. 10,44
C. 8,73
D. 12,61