Tính thể tích O2 cần đung (đơn vị m3 , ở đktc) để đốt cháy 12 kg một loại tha. Có chứa 90% khối lượng cácbon, 8% khối lượng lưu huỳnh còn lại là tạp chất ko cháy

Những câu hỏi liên quan
nung hoàn toàn 20,2g KNO3 a) tính khối lượng chất rắn cồn lại b) dùng toàn bộ lượng khí O2 thu được để đốt cháy hoàn toàn m g một loại than chứa 92% cacbon , 4% khối lượng lưa huỳnh còn lại là tạp chất trơ . tính giá trị của m . tính thể tích khí CO2 và SO2 sinh ra
nKNO3 = 0.2 (mol)
2KNO3 -to-> 2KNO2 + O2
0.2__________0.2____0.1
mKNO2 = 0.2*85=17(g)
C + O2 -to-> CO2
x___x
S + O2 -to-> SO2
y___y
x + y = 0.1 (1)
Mặt khác :
+) 32y/m * 100% = 4%
=> 32y = 0.04m (2)
+) 12x/m = 0.92
=> 12x = 0.92m (3)
(1) , (2) , (3) :
x = 0.1
y = 0.002
m = 1.3
VCO2 + VSO2 = ( 0.1 + 0.002) * 22.4 = 2.2848 (l)
Đúng 1
Bình luận (0)
Tính thể tích không khí (đktc) cần dùng để đốt cháy hoàn toàn 1 kg than tổ ong chứa 60% cacbon, 0,8% lưu huỳnh và phần còn lại là tạp chất không cháy. Biết oxi chiếm 1/5 thể tích không khí.
PTHH:
C + O2 ---to----> CO2
50.....50.......................................(mol)
S + O2 ----to---> SO2
0,25...0,25 ............................................(mol)
→ (cần dùng) = (50 + 0,25) . 22,4 = 1125,6 (l)
=>Vkk=1125.6.5=5628l
Đúng 0
Bình luận (0)
a) Tính khối lượng chất tan và khối lượng nước có trong 50g dung dịch MgCl² 4% b) Đốt cháy 6,4g lưu huỳnh trong không khí . Tính thể tích không khí ở (đktc) cần dùng đốt cháy lượng lưu huỳnh trên . Biết oxi chiếm 20% thể tích không khí .
a)
\(m_{MgCl_2}=\dfrac{50.4}{100}=2\left(g\right)\Rightarrow m_{H_2O}=50-2=48\left(g\right)\)
b)
\(n_S=\dfrac{6,4}{32}=0,2\left(mol\right)\)
PTHH: S + O2 --to--> SO2
0,2->0,2
=> VO2 = 0,2.22,4 = 4,48 (l)
=> Vkk = 4,48 : 20% = 22,4 (l)
Đúng 2
Bình luận (0)
a.\(m_{MgCl_2}=\dfrac{50.4}{100}=2g\)
\(m_{H_2O}=50-2=48g\)
b.\(n_S=\dfrac{6,4}{32}=0,2mol\)
\(S+O_2\rightarrow\left(t^o\right)SO_2\)
0,2 0,2 ( mol )
\(V_{kk}=V_{O_2}.5=\left(0,2.22,4\right).5=22,4l\)
Đúng 1
Bình luận (0)
Để đốt cháy một lượng lưu huỳnh, người ta đã dùng hết 5,6 lít khi oxi (ở ĐKTC). (S + O2 --->SO2)
a/ Hãy tính khối lượng lưu huỳnh đã bị đốt cháy
b/ Hãy tính thể tích khí lưu huỳnh đioxxit tạo thành sau phản ứng?
b: \(S+O_2\rightarrow SO_2\)
\(n_{O_2}=\dfrac{V_{O_2}}{22.4}=\dfrac{5.6}{22.4}=0.25\left(mol\right)\)
\(\Leftrightarrow n_{SO_2}=0.25\left(mol\right)\)
\(V=0.25\cdot n=0.25\cdot64=16\left(lít\right)\)
Đúng 0
Bình luận (0)
\(a.PTHH:S+O_2\underrightarrow{t^o}SO_2\\ n_{O_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Từ PTHH trên ta có:
Đốt hết 1 mol S thì cần 1 mol \(O_2\)
=> Đốt hết 0,25 mol S thì cần 0,25 mol \(O_2\)
\(\Rightarrow m_S=32.0,25=8\left(g\right)\)
b. Từ PTHH trên ta có
Đốt 1 mol \(O_2\) thì sinh ra 1 mol \(SO_2\)
=> Đốt 0,25 mol \(O_2\) thì sinh ra 0,25 mol \(SO_2\)
\(\Rightarrow V_{SO_2}=22,4.0,25=5,6\left(mol\right)\)
Đúng 0
Bình luận (0)
Đốt 16 gam lưu huỳnh trong không khí (biết rằng lưu huỳnh cháy là xảy ra phản ứng với oxi) thì thu được lưu huỳnh đioxita. Tính khối lượng lưu huỳnh đioxit thu đượcb. Tính thể tích không ở đktc cần dùng để đốt cháy hết lượng phốt pho trênc. Nếu đốt cháy lượng lưu huỳnh trên trong bình chứa 24 gam khí Oxi. Hỏi chất nào còn dư sau phản ứng và số mol chất còn dư là bao nhiêu?
Đọc tiếp
Đốt 16 gam lưu huỳnh trong không khí (biết rằng lưu huỳnh cháy là xảy ra phản ứng với oxi) thì thu được lưu huỳnh đioxit
a. Tính khối lượng lưu huỳnh đioxit thu được
b. Tính thể tích không ở đktc cần dùng để đốt cháy hết lượng phốt pho trên
c. Nếu đốt cháy lượng lưu huỳnh trên trong bình chứa 24 gam khí Oxi. Hỏi chất nào còn dư sau phản ứng và số mol chất còn dư là bao nhiêu?
a) \(n_S=\dfrac{16}{32}=0,5\left(mol\right)\)
PTHH: S + O2 --to--> SO2
0,5->0,5------>0,5
=> mSO2 = 0,5.64 = 32 (g)
b) VO2 = 0,5.22,4 = 11,2 (l)
=> Vkk = 11,2.5 = 56 (l)
c)
\(n_{O_2}=\dfrac{24}{32}=0,75\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,5}{1}< \dfrac{0,75}{1}\)
=> S hết, O2 dư
PTHH: S + O2 --to--> SO2
0,5->0,5------>0,5
=> nO2(dư) = 0,75 - 0,5 = 0,25 (mol)
Đúng 2
Bình luận (0)
Đốt cháy 36 Kg than đá có chứa 0,5 gam tạp chất lưu huỳnh và 1,5% tạp chất không cháy được. Tính thể tích các khí được sinh ra ở (đktc).
0,5g = 0,0005 kg
\(m_C=36-0,0005-\left(36.1,5\%\right)=35,4595kg=35459,5g\)
\(n_C=\dfrac{35459,5}{12}=2954,95mol\)
\(n_S=\dfrac{0,5}{32}=0,015625mol\)
\(C+O_2\rightarrow\left(t^o\right)CO_2\)
2954,5 2954,5 ( mol )
\(S+O_2\rightarrow\left(t^o\right)SO_2\)
\(0,015625\) \(0,015625\) ( mol )
\(V_{CO_2}=2954,5.22,4=66180,8l\)
\(V_{SO_2}=\)\(0,015625.22,4=0,35l\)
Đúng 2
Bình luận (0)
Câu 11. Cho 11,2 g CaO tác dụng với dung dịch có chứa 39,2 g H2SO4. Tính khối lượng các chất còn lại trong phản ứng hóa học trên (không tính khối lượng nước)Câu 12. Đốt cháy 6,4 g lưu huỳnh bằng 11,2 lít khí O2 (đktc) thu được sản phẩm là SO2. Tính thể tích của các khí thu được sau phản ứng hóa học trên ở đktcCâu 13. Đốt cháy 4,8 g cacbon bằng 6,72 lít khí oxi thu được sản phẩm sau phản ứng là CO2. Tìm khối lượng chất còn dư và thể tích khí CO2 thu đượcCâu 14. Cho 20,8 g BaCl2 tác dụng với dung...
Đọc tiếp
Câu 11. Cho 11,2 g CaO tác dụng với dung dịch có chứa 39,2 g H2SO4. Tính khối lượng các chất còn lại trong phản ứng hóa học trên (không tính khối lượng nước)
Câu 12. Đốt cháy 6,4 g lưu huỳnh bằng 11,2 lít khí O2 (đktc) thu được sản phẩm là SO2. Tính thể tích của các khí thu được sau phản ứng hóa học trên ở đktc
Câu 13. Đốt cháy 4,8 g cacbon bằng 6,72 lít khí oxi thu được sản phẩm sau phản ứng là CO2. Tìm khối lượng chất còn dư và thể tích khí CO2 thu được
Câu 14. Cho 20,8 g BaCl2 tác dụng với dung dịch chứa 9,8 g H2SO4. Tính khối lượng các chất thu được sau phản ứng.
Câu 15. Cho 20 g CuO tác dụng với dung dịch chứa 18,25 g HCl. Tính khối lượng các chất thu được sau phản ứng.
Câu 11:
\(n_{CaO}=\dfrac{11,2}{56}=0,2\left(mol\right);n_{H_2SO_4}=\dfrac{39,2}{98}=0,4\left(mol\right)\)
PTHH: \(CaO+H_2SO_4\rightarrow CaSO_4+H_2O\)
Ban đầu: 0,2 0,4 0,2
Sau pư: 0 0,2 0,2
`=>`\(\left\{{}\begin{matrix}m_{H_2SO_4}=0,2.98=19,6\left(g\right)\\m_{CaSO_4}=0,2.136=27,2\left(g\right)\end{matrix}\right.\)
Câu 12:
\(n_S=\dfrac{6,4}{32}=0,2\left(mol\right);n_{O_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: \(S+O_2\xrightarrow[]{t^o}SO_2\)
Ban đầu: 0,2 0,5
Sau pư: 0 0,3 0,2
`=>`\(\left\{{}\begin{matrix}V_{O_2}=0,3.22,4=6,72\left(l\right)\\V_{SO_2}=0,2.22,4=4,48\left(l\right)\end{matrix}\right.\)
Câu 13:
\(n_C=\dfrac{4,8}{12}=0,4\left(mol\right);n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: \(C+O_2\xrightarrow[]{t^o}CO_2\)
Ban đầu: 0,4 0,3
Sau pư: 0,1 0 0,3
`=>`\(\left\{{}\begin{matrix}m_{C\left(d\text{ư}\right)}=0,1.12=1,2\left(g\right)\\V_{CO_2}=0,3.22,4=6,72\left(l\right)\end{matrix}\right.\)
Câu 14:
\(n_{BaCl_2}=\dfrac{20,8}{208}=0,1\left(mol\right);n_{H_2SO_4}=\dfrac{9,8}{98}=0,1\left(mol\right)\)
PTHH: \(BaCl_2+H_2SO_4\rightarrow BaSO_4+2HCl\)
Ban đầu: 0,1 0,1
Sau pư: 0 0 0,1 0,2
`=>`\(\left\{{}\begin{matrix}m_{BaSO_4}=0,1.233=23,3\left(g\right)\\m_{HCl}=0,2.36,5=7,3\left(g\right)\end{matrix}\right.\)
Câu 15:
\(n_{CuO}=\dfrac{20}{80}=0,25\left(mol\right);n_{HCl}=\dfrac{18,25}{36,5}=0,5\left(mol\right)\)
PTHH: \(CuO+2HCl\rightarrow CuCl_2+H_2O\)
Ban đầu: 0,25 0,5
Sau pư: 0 0 0,25
`=>`\(m_{CuCl_2}=0,25.135=33,75\left(g\right)\)
Đúng 2
Bình luận (0)
đốt cháy 1kg than trong khí o2, biết than có 10% tạp chất không cháy tính:
- thể tích oxi(đktc) cần thiết để đốt cháy 1kg than trên
-khối lượng co2(đktc) sinh ra trong phản ứng trên
Cnguyên chất = (100%-10%).1000 = 900 (g)
\(n_C=\dfrac{900}{12}=75\left(mol\right)\)
PTHH: C + O2 ---to→ CO2
Mol: 75 75
\(V_{O_2}=75.22,4=1680\left(l\right)\)
\(m_{CO_2}=75.44=3300\left(g\right)\)
Đúng 2
Bình luận (0)
Một nhà máy phát điện vận hành bằng các đốt cháy nhiên liệu phức hợp có công thức trung bình là C11H7S. Giả sử nguồn không khí cung cấp chỉ chứa N2 và O2 có tỷ lệ mol 3,76:1,00 và N2 không cho phản ứng. Ngoài nước tạo thành, lượng cacbon trong nhiên liệu được chuyển hóa hoàn toàn thành CO2 và lưu huỳnh chuyển hóa thành SO2. (a) Viết phương trình phản ứng cháy của C11H7S. (b) Để phản ứng cháy xảy ra hoàn toàn, thực tế cần dùng dư 20% lượng oxy so với tỷ lượng lý thuyết. Tính khối lượng (kg) và t...
Đọc tiếp
Một nhà máy phát điện vận hành bằng các đốt cháy nhiên liệu phức hợp có công thức trung bình là C11H7S. Giả sử nguồn không khí cung cấp chỉ chứa N2 và O2 có tỷ lệ mol 3,76:1,00 và N2 không cho phản ứng. Ngoài nước tạo thành, lượng cacbon trong nhiên liệu được chuyển hóa hoàn toàn thành CO2 và lưu huỳnh chuyển hóa thành SO2.
(a) Viết phương trình phản ứng cháy của C11H7S.
(b) Để phản ứng cháy xảy ra hoàn toàn, thực tế cần dùng dư 20% lượng oxy so với tỷ lượng lý thuyết. Tính khối lượng (kg) và thể tích (ở đktc, m3) không khí cần sử dụng để đốt cháy hoàn toàn 1 tấn C11H7S.
(c) Tính tổng khối lượng CO2 và SO2 tạo thành trong điều kiện của câu (b) trên

Do lấy dư 20% oxi so với lượng cần đốt cháy nên lượng oxi đã lấy là:


Tổng khối lượng CO2 và SO2 :
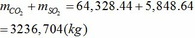
Chú ý:
Lượng O2 lấy dư 20% so với với lượng cần thiết => tính mol O2 chính xác
Đúng 0
Bình luận (0)






















