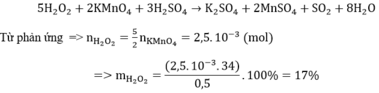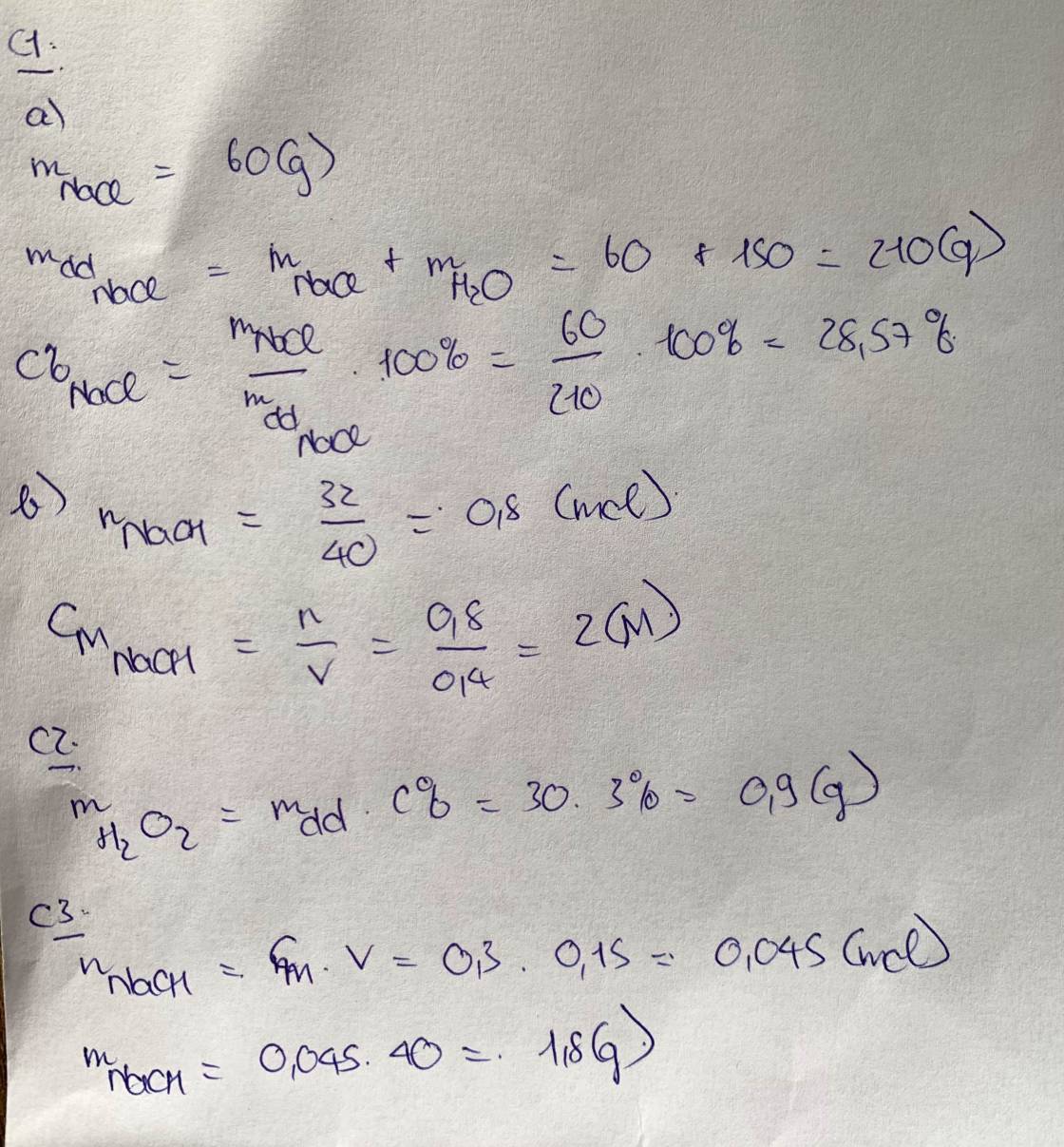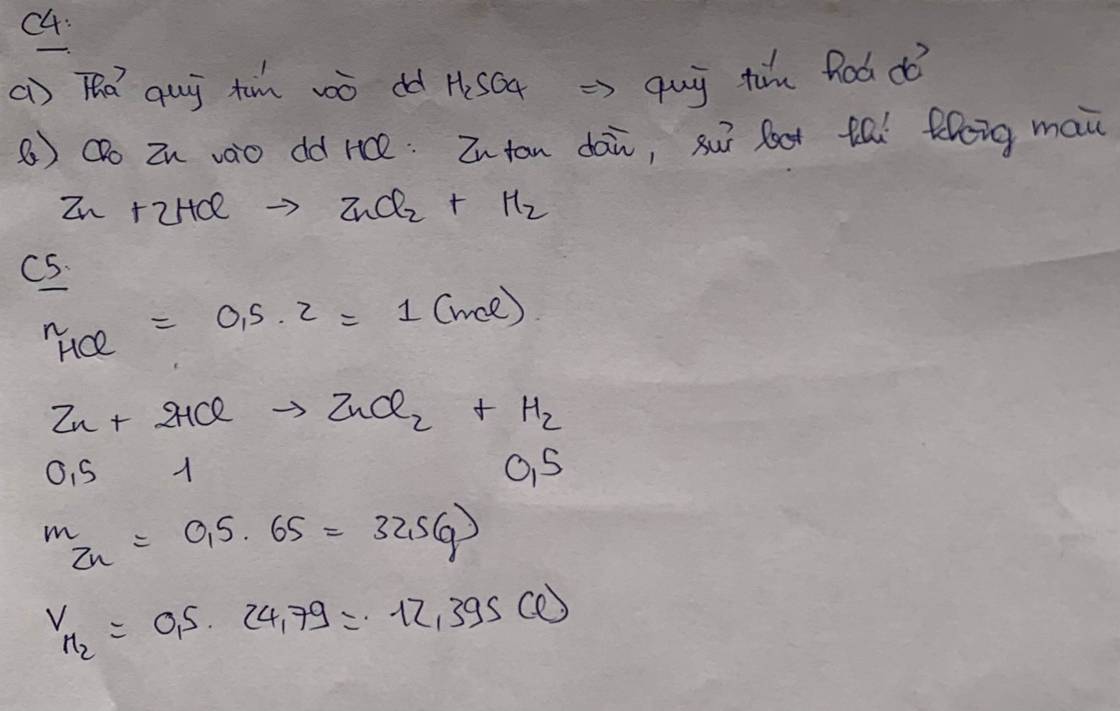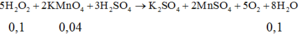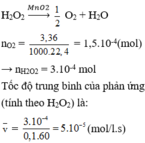30 ml dung dịch H2O2(oxy già hay là hydrogen peroxit) có nồng độ 3%,,tính khối lượng H2O2 có trong đó.

Những câu hỏi liên quan
Để xác định nồng độ dung dịch H2O2 , người ta hòa tan 0,5 gam nước oxi già vào nước, thêm H2SO4 tạo môi trường axit. Chuẩn độ dung dịch thu được cần vừa đủ 10 ml dung dịch KMnO4 0,1M . Xác định hàm lượng H2O2 trong nước oxi già. A. 9% B. 17% C. 12% D. 21%
Đọc tiếp
Để xác định nồng độ dung dịch H2O2 , người ta hòa tan 0,5 gam nước oxi già vào nước, thêm H2SO4 tạo môi trường axit. Chuẩn độ dung dịch thu được cần vừa đủ 10 ml dung dịch KMnO4 0,1M . Xác định hàm lượng H2O2 trong nước oxi già.
A. 9%
B. 17%
C. 12%
D. 21%
Dung dịch hydro peroxit (H2O2) có nồng độ 3% w / w trong nước thường được sử dụng làm chất sát trùng vết thương. Trong một nhà máy sản xuất dung dịch H2O2 để phân phối cho các hiệu thuốc, người ta đổ đầy chai nhựa nặng 20 g bằng dung dịch 3% sao cho cả chai nặng 220 g. Khối lượng H2O2 (tính bằng g) trong mỗi bình là bao nhiêu?
Mn ơi giải bài này hộ mình ạ!!!!!!!! Thank kiu mn ạ!
Dung dịch hydro peroxit (H2O2) có nồng độ 3% w / w trong nước thường được sử dụng làm chất sát trùng vết thương. Trong một nhà máy sản xuất dung dịch H2O2 để phân phối cho các hiệu thuốc, người ta đổ đầy chai nhựa nặng 20 g bằng dung dịch 3% sao cho cả chai nặng 220 g. Khối lượng H2O2 (tính bằng g) trong mỗi bình là bao nhiêu?
Ảnh hưởng của chất xúc tác đến tốc độ phản ứngChuẩn bị: nước oxy già (y tế) H2O2 3%, manganese dioxide (MnO2, dạng bột); ống nghiệm.Tiến hành:- Cho khoảng 3 mL dung dịch H2O2 3% vào hai ống nghiệm (1) và ống nghiệm (2).- Cho một ít bột manganese dioxide vào ống nghiệm (2).Quan sát hiện tượng xảy ra và trả lời câu hỏi: Phản ứng ở ống nghiệm nào xảy ra nhanh hơn?
Đọc tiếp
Ảnh hưởng của chất xúc tác đến tốc độ phản ứng
Chuẩn bị: nước oxy già (y tế) H2O2 3%, manganese dioxide (MnO2, dạng bột); ống nghiệm.
Tiến hành:
- Cho khoảng 3 mL dung dịch H2O2 3% vào hai ống nghiệm (1) và ống nghiệm (2).
- Cho một ít bột manganese dioxide vào ống nghiệm (2).
Quan sát hiện tượng xảy ra và trả lời câu hỏi:
Phản ứng ở ống nghiệm nào xảy ra nhanh hơn?
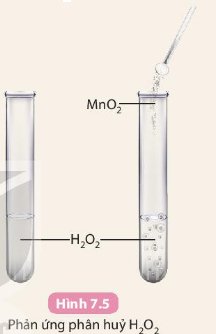
Phản ứng ở ống nghiệm (2) xảy ra nhanh hơn do khí thoát ra nhanh và mạnh hơn.
Đúng 1
Bình luận (0)
Phản ứng ở ống nghiệm (2) xảy ra nhanh hơn
Đúng 0
Bình luận (0)
Câu 1 a. Hòa tan 60 gam NaCl vào 150 gam nước. Tính nồng độ phần trăm của dung dịch thu được.b.Tính nồng độ mol của dung dịch khi hòa tan 32 gam NaOH trong 400ml nước. (coi thể tích dung dịch không đổi).Câu 2 Hãy tính khối lượng H2O2 có trong 30 g dung dịch nồng 3% .Câu 3 Tính khối lượng của NaOH có trong 300 ml dung dịch có nồng độ 0,15 M.Cho Na 23; O 16; H1.Câu 4Hãy nêu , giải thích được hiện tượng xảy ra trong thí nghiệm và viết phương trình hoá học .Từ đó rút ra nhận xét về tính chất...
Đọc tiếp
Câu 1
a. Hòa tan 60 gam NaCl vào 150 gam nước. Tính nồng độ phần trăm của dung dịch thu được.
b.Tính nồng độ mol của dung dịch khi hòa tan 32 gam NaOH trong 400ml nước. (coi thể tích dung dịch không đổi).
Câu 2 Hãy tính khối lượng H2O2 có trong 30 g dung dịch nồng 3% .
Câu 3 Tính khối lượng của NaOH có trong 300 ml dung dịch có nồng độ 0,15 M.
Cho Na= 23; O= 16; H=1.
Câu 4
Hãy nêu , giải thích được hiện tượng xảy ra trong thí nghiệm và viết phương trình hoá học .Từ đó rút ra nhận xét về tính chất của acid khi thực hiện các thí nghiệm sau:
a.Thả miếng giấy quì tím vào lọ đựng dung dịch sulfuric acid (H2SO4)
b.Cho viên kẽm (zinc) vào trong ống nghiệm có chứa dung dịch hydrochloric acid.
Câu 5
Cho kẽm (Zinc) dư tác dụng với 500 ml dung dịch hydrochloric acid 2 M, thu được V (lít) khí hydrogen (250C và 1 bar).
Tính khối lượng kẽm đã phản ứng và thể tích khí hydrogen thu được.
Nước oxy già có tính oxi hóa mạnh, do khả năng oxi hóa của hydrogen peroxide (H2O2).a) Từ công thức cấu tạo H – O – O – H, hãy xác định số oxi hóa của mỗi nguyên tử.b) Nguyên tử nguyên tố nào gây nên tính oxi hóa của H2O2. Viết các quá trình oxi hóa, quá trình khử minh họa.
Đọc tiếp
Nước oxy già có tính oxi hóa mạnh, do khả năng oxi hóa của hydrogen peroxide (H2O2).
a) Từ công thức cấu tạo H – O – O – H, hãy xác định số oxi hóa của mỗi nguyên tử.
b) Nguyên tử nguyên tố nào gây nên tính oxi hóa của H2O2. Viết các quá trình oxi hóa, quá trình khử minh họa.
a) H – O – O – H
Số oxi hóa của H là +1
Gọi x là số oxi hóa của O, theo quy tắc 1 và 2 có:
1.(+1) + 1.x + 1.x + 1.(+1) = 0 → x = -1.
Vậy số oxi hóa của H là +1, của O là -1 (trường hợp đặc biệt).
b) Nguyên tố O gây nên tính oxi hóa của H2O2.
2Fe2+ + H2O2 + 2H+ → 2Fe3+ + 2H2O(quá trình oxi hóa)
2Fe3+ + H2O2 + 2OH- → 2Fe2+ + 2H2O + O2 (quá trình khử)
Đúng 0
Bình luận (0)
Khi cho một lượng vừa đủ dung dịch loãng của KMnO4 và H2SO4 vào một lượng H2O2, thu được 2,24 lít O2 (đktc). Khối lượng của H2O2 có trong dung dịch đã lấy và khối lượng của KMnO4 đã phản ứng lần lượt là A. 6,32g và 2,04 g B. 2,04 g và 3,16 g. C. 3,4 g và 3,16 g D. 3,4 g và 6,32 g.
Đọc tiếp
Khi cho một lượng vừa đủ dung dịch loãng của KMnO4 và H2SO4 vào một lượng H2O2, thu được 2,24 lít O2 (đktc). Khối lượng của H2O2 có trong dung dịch đã lấy và khối lượng của KMnO4 đã phản ứng lần lượt là
A. 6,32g và 2,04 g
B. 2,04 g và 3,16 g.
C. 3,4 g và 3,16 g
D. 3,4 g và 6,32 g.
Khi cho một lượng vừa đủ dung dịch loãng của KMnO4 và H2SO4 vào một lượng H2O2, thu được 2,24 lít O2 (đktc). Khối lượng của H2O2 có trong dung dịch đã lấy và khối lượng của KMnO4 đã phản ứng lần lượt là A. 6,32g và 2,04 g B. 2,04 g và 3,16 g. C. 3,4 g và 3,16 g D. 3,4 g và 6,32 g
Đọc tiếp
Khi cho một lượng vừa đủ dung dịch loãng của KMnO4 và H2SO4 vào một lượng H2O2, thu được 2,24 lít O2 (đktc). Khối lượng của H2O2 có trong dung dịch đã lấy và khối lượng của KMnO4 đã phản ứng lần lượt là
A. 6,32g và 2,04 g
B. 2,04 g và 3,16 g.
C. 3,4 g và 3,16 g
D. 3,4 g và 6,32 g
Cho chất xúc tác
M
n
O
2
vào 100 ml dung dịch
H
2
O
2
, sau 60 giây thu được 3,36 ml khí
O
2
(đktc). Tốc độ trung bình của phản ứng (tính theo
H
2
O
2
) trong 60 giây trên là A.
2
,
5
.
10...
Đọc tiếp
Cho chất xúc tác M n O 2 vào 100 ml dung dịch H 2 O 2 , sau 60 giây thu được 3,36 ml khí O 2 (đktc). Tốc độ trung bình của phản ứng (tính theo H 2 O 2 ) trong 60 giây trên là
A. 2 , 5 . 10 - 4 m o l / ( l . s )
B. 5 , 0 . 10 - 4 m o l / ( l . s )
C. 1 , 0 . 10 - 3 m o l / ( l . s )
D. 5 , 0 . 10 - 5 m o l / ( l . s )