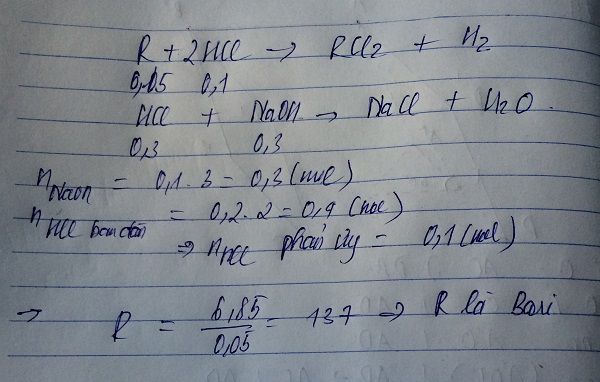Hòa tan hoàn toàn 6,85 g một kim loại kiềm thổ M bằng 100 ml dung dịch HCL 1M vừa đủ . Xác định tên kim loại trên

Những câu hỏi liên quan
Hòa tan hoàn toàn 6,85 g một kim loại kiềm thổ R bằng 50 ml dung dịch HCl 2 M. Xác định tên kim loại trên.
Hòa tan hoàn toàn 0,8 g một kim loại hoá trị II hoà tan hoàn toàn trong 100 ml H 2 S O 4 0,5 M. Lượng axit còn dư phản ứng vừa đủ với 33,4 ml dung dịch NaOH 1,00 M. Xác định tên kim loại.
Số mol H 2 S O 4 trong 100ml dung dịch 0,5M là :
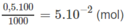
Số mol NaOH trong 33,4 ml nồng độ 1M :
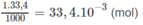
H 2 S O 4 + 2NaOH → N a 2 S O 4 + 2 H 2 O
Lượng H 2 S O 4 đã phản ứng với NaOH :

Số mol H 2 S O 4 đã phản ứng với kim loại là :
5. 10 - 2 - 1.67. 10 - 2 = 3,33. 10 - 2 mol
Dung dịch H 2 S O 4 0,5M là dung dịch loãng nên :
X + H 2 S O 4 → X S O 4 + H 2 ↑
Số mol X và số mol H 2 S O 4 phản ứng bằng nhau, nên :
3,33. 10 - 2 mol X có khối lượng 0,8 g
1 mol X có khối lượng: 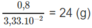
⇒ Mkim loại = 24 g/mol.
Vậy kim loại hoá trị II là magie.
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 42,6 gam hỗn hợp X gồm một kim loại kiềm và một kim loại kiềm thổ có tỉ lệ mol tương ứng là 5 : 4 vào 500 ml dung dịch HCl 1M thu được dung dịch Y và 17,472 lít khí (đktc).a) Xác định thành phần % về khối lượng mỗi kim loại trong X.b) Dẫn từ từ khí CO2 vào dung dịch Y, tính thể tích khí CO2 (đktc) cần dùng để thu được lượng kết tủa lớn nhất.
Đọc tiếp
Hòa tan hoàn toàn 42,6 gam hỗn hợp X gồm một kim loại kiềm và một kim loại kiềm thổ có tỉ lệ mol tương ứng là 5 : 4 vào 500 ml dung dịch HCl 1M thu được dung dịch Y và 17,472 lít khí (đktc).
a) Xác định thành phần % về khối lượng mỗi kim loại trong X.
b) Dẫn từ từ khí CO2 vào dung dịch Y, tính thể tích khí CO2 (đktc) cần dùng để thu được lượng kết tủa lớn nhất.
Hỗn hợp X gồm một kim loại kiềm (A) và một kim loại kiềm thổ (B) có tỉ lệ mol tương ứng là 5:4. Hòa tan hoàn toàn 42,6 gam bằng 500 ml dung dịch HCl 1M thu được dung dịch Y và 17,472 lít khí (ở đktc).a/ Xác định thành phần % về khối lượng mỗi kim loại trong X.b/ Dẫn từ từ khí CO2 vào dung dịch Y, tính thể tích khí CO2 (ở đktc) cần dùng để thu được lượng kết tủa lớn nhất
Đọc tiếp
Hỗn hợp X gồm một kim loại kiềm (A) và một kim loại kiềm thổ (B) có tỉ lệ mol tương ứng là 5:4. Hòa tan hoàn toàn 42,6 gam bằng 500 ml dung dịch HCl 1M thu được dung dịch Y và 17,472 lít khí (ở đktc).
a/ Xác định thành phần % về khối lượng mỗi kim loại trong X.
b/ Dẫn từ từ khí CO2 vào dung dịch Y, tính thể tích khí CO2 (ở đktc) cần dùng để thu được lượng kết tủa lớn nhất
a, Ta có: \(n_{H_2}=\dfrac{17,472}{22,4}=0,78\left(mol\right)\)
\(n_{HCl}=0,5.1=0,5\left(mol\right)\)
\(\Rightarrow2n_{H_2}>n_{HCl}\) → HCl hết, KL dư pư với H2O.
Gọi: \(\left\{{}\begin{matrix}n_A=5x\left(mol\right)\\n_B=4x\left(mol\right)\end{matrix}\right.\)
BT e, có: nA + 2nB = 2nH2 ⇒ 5x + 4x.2 = 0,78.2 ⇒ x = 0,12
\(\Rightarrow\left\{{}\begin{matrix}n_A=0,6\left(mol\right)\\n_B=0,48\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow0,6M_A+0,48M_B=42,6\Rightarrow5M_A+4M_B=355\)
Với MA = 39 (g/mol) và MB = 40 (g/mol) thì thỏa mãn.
→ A là K, B là Ca.
\(\Rightarrow\left\{{}\begin{matrix}\%m_K=\dfrac{0,6.39}{42,6}.100\%\approx54,93\%\\\%m_{Ca}\approx45,07\%\end{matrix}\right.\)
b, Dung dịch Y gồm: \(\left\{{}\begin{matrix}K^+\\Ca^{2+}\\Cl^-\\OH^-\end{matrix}\right.\)
BTNT Ca, có: nCa2+ = nCa = 0,48 (mol)
BTNT H, có: nOH- = 2nH2 - nHCl = 1,06 (mol)
TH1:
\(CO_2+2OH^-\rightarrow CO_3^{2-}+H_2O\)
\(Ca^{2+}+CO_3^{2-}\rightarrow CaCO_3\)
Có: nCO2 = nCO32- = nCa2+ = 0,48 (mol)
TH2:
\(CO_2+2OH^-\rightarrow CO_3^{2-}+H_2O\)
0,53____1,06______0,53 (mol)
\(CO_2+CO_3^{2-}+H_2O\rightarrow2HCO_3^-\)
0,05____0,05 (mol)
\(Ca^{2+}+CO_3^{2-}\rightarrow CaCO_3\)
0,48____0,48 (mol)
⇒ nCO2 = 0,05 + 0,53 = 0,58 (mol)
⇒ 0,48 ≤ nCO2 ≤ 0,58 thì thu được lượng kết tủa lớn nhất.
⇒ 10,752 (l) ≤ VCO2 ≤ 12,992 (l)
Đúng 3
Bình luận (0)
https://hoc24.vn/cau-hoi/hoa-tan-hoan-toan-426-gam-hon-hop-x-gom-mot-kim-loai-kiem-va-mot-kim-loai-kiem-tho-co-ti-le-mol-tuong-ung-la-54-vao-500-ml-dung-dich-hcl-1m-thu-duoc.4485788491246
Đúng 0
Bình luận (0)
hòa tan hoàn toàn một kim loại kiềm thổ R vào 200ml dung dịch HCl 2M.Để trung hòa lượng axit dư cần 100ml dung dịch NaOH 3M xác định tên kim loại đó.....trân thành cẳm ơn
Đề thiếu m
NaOH + HCl = NaCl + H2O
0,3 - - - - 0,3
=>số mol HCl pư là 0,1 mol
=>số mol OH- = số mol H+ = số mol HCl = 0,1 mol
=>số mol kiềm thổ là 0,05 mol
=>R = 6,85 / 0,05 = 137 => Ba
Đúng 0
Bình luận (0)
Hỗn hợp X gồm M2CO3, MHCO3, MCl (M là kim loại kiềm). Hòa tan hoàn toàn 30,15 gam hỗn hợp X trong V ml dung dịch HCl 10,52% (D 1,05g/ml) thu được dung dịch Y và 5,6 lít CO2 (đktc). Chia Y thành 2 phần bằng nhau. – Phần 1: tác dụng vừa đủ với 100 ml dung dịch KOH 1M thu được m gam muối. – Phần 2: tác dụng hoàn toàn với dung dịch AgNO3 dư thu được 50,225 gam kết tủa. a. Xác định tên kim loại M. b. Tính thành phần phần trăm theo khối lượng của từng chất trong hỗn hợp X. c. Tính V và m.
Đọc tiếp
Hỗn hợp X gồm M2CO3, MHCO3, MCl (M là kim loại kiềm). Hòa tan hoàn toàn 30,15 gam hỗn hợp X trong V ml dung dịch HCl 10,52% (D = 1,05g/ml) thu được dung dịch Y và 5,6 lít CO2 (đktc). Chia Y thành 2 phần bằng nhau.
– Phần 1: tác dụng vừa đủ với 100 ml dung dịch KOH 1M thu được m gam muối.
– Phần 2: tác dụng hoàn toàn với dung dịch AgNO3 dư thu được 50,225 gam kết tủa.
a. Xác định tên kim loại M.
b. Tính thành phần phần trăm theo khối lượng của từng chất trong hỗn hợp X.
c. Tính V và m.
hòa tan hoàn toàn một kim loại kiềm thổ R vào 200ml dung dịch HCl 2M.Để trung hòa lượng axit dư cần 100ml dung dịch NaOH 3M xác định tên kim loại đó.....trân thành cẳm ơn
<a href="http://tchiase.info/office-2016-tai-office-2016-professional-plus-full-crack/">tải office 2016</a>
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn m gam oxit kim loại chưa rõ hoá trị tác dụng vừa đủ với 800 ml dung dịch HCl 1M thu được 38gam muối . Xác định Oxit?
Để xác định oxit kim loại chưa rõ hoá trị trong bài toán này, ta cần sử dụng phương pháp tính toán dựa trên phản ứng hóa học.
Ta biết rằng muối được tạo thành từ phản ứng giữa oxit kim loại với axit clohidric (HCl). Với số mol muối thu được là n = 38g / (khối lượng mol muối), ta cần tìm khối lượng mol muối để tính toán số mol oxit kim loại ban đầu.
Theo phương trình phản ứng, ta biết rằng số mol muối bằng số mol oxit kim loại ban đầu. Vậy số mol oxit kim loại ban đầu cũng là n.
Số mol oxit kim loại ban đầu có thể tính bằng công thức: n = (số mol axit) x (tỷ lệ mol axit và muối) = (nồng độ axit) x (thể tích axit) x (tỷ lệ mol axit và muối)
Trong trường hợp này, ta có nồng độ axit HCl là 1M và thể tích axit HCl là 800ml. Tỷ lệ mol axit và muối là 1:1 theo phương trình phản ứng.
Vậy số mol oxit kim loại ban đầu là: n = 1M x 800ml x 1 = 800 mol
Tiếp theo, ta cần tìm khối lượng mol oxit kim loại ban đầu bằng cách sử dụng tỷ lệ khối lượng mol và số mol của chất.
Khối lượng mol oxit kim loại ban đầu có thể tính bằng công thức: m = n x khối lượng mol oxit
Vậy khối lượng mol oxit kim loại ban đầu là: m = 800 mol x (khối lượng mol oxit)
Cuối cùng, ta cần tìm tên của oxit kim loại chưa rõ hoá trị. Để làm điều này, cần biết khối lượng mol oxit và so sánh với các khối lượng mol của các oxit kim loại có thể có.
Tóm lại, để xác định oxit kim loại chưa rõ hoá trị, ta cần tính số mol oxit kim loại ban đầu, sau đó tính khối lượng mol oxit kim loại ban đầu. Cuối cùng, so sánh khối lượng mol oxit kim loại ban đầu với các khối lượng mol oxit kim loại có thể có để xác định tên của oxit kim loại.
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 8g oxit bazơ của kim loại hóa trị III cần vừa đủ 200 ml dung dịch HCl 1,5 M xác định công thức oxit gọi tên
Gọi hóa trị của kim loại M là x
PTHH: M2Ox + 2xHCl ===> 2MClx + xH2
Số mol HCl: nHCl = 1,5 x 0,2 = 0,3 (mol)
Theo PTHH, nM2Ox = 0,3/2x=0,15/x(mol)
⇒ MM2Ox = 8÷0,15/x=160x/3(g/mol)
⇔2MM+16x=160x/3
⇔2MM=160x/3−16x=112x/3
⇔MM=56x/3(g/mol)
Vì M là kim loại nên x nhận các giá trị 1, 2,3
+) x = 1 ⇒ MM = 563(loại)
+) x = 2 ⇒ MM = 1123(loại)
+) x = 3 ⇒ MM = 56 (nhận)
⇒ M là Fe
⇒ Công thức oxit: Fe2O3
Đúng 0
Bình luận (0)