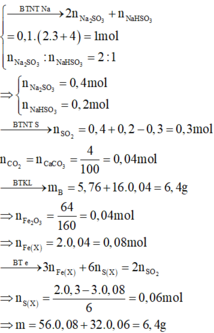Cho Fe và oxit sắt nặng 2,6g vào bình chứa CO nung nóng khí thoát ra thu vào dung dịch Ca(OH)2 xuất hiện 10 gam kết tủa trắng. Tính khối lượng Fe sau phản ứng.

Những câu hỏi liên quan
Thổi 8,96 lít CO (đktc) qua 16 gam một oxit sắt nung nóng. Dẫn toàn bộ khí sau phản ứng qua dung dịch Ca(OH)2 dư, thấy tạo ra 30 gam kết tủa trắng CaCO3, các phản ứng xảy ra hoàn toàn.
1) Tính khối lượng Fe thu được.
2) Xác định công thức oxit sắt.
a) nCaCO3 = 0.3 (mol)
CO + O => CO2
=> nO = 0.3 (mol)
mFe = moxit - mO = 16 - 0.3*16 = 11.2 (g)
nFe = 11.2/56 = 0.2 (mol)
nFe : nO = 0.2 : 0.3 = 2 : 3
CT oxit : Fe2O3
Đúng 1
Bình luận (1)
nCO= 0,4(mol)
yCO + FexOy \(\rightarrow\) xFe + yCO2 (phản ứng có nhiệt độ) (1)
CO2 + Ca(OH)2 \(\rightarrow\) CaCO3 + H2O (2)
nCaCO3= nCO2(2) = nCO2(1) = 0,3(mol)
nCO2 = nCO = 0,3(mol) => CO dư (0,4-0,3=0,1(mol))
1, Áp dụng định luật bảo toàn khối lượng, ta có:
mCO + mFexOy = mFe + mCO2
=> mfe = mCO + mfexOy - mCO2
\(\Leftrightarrow\) mfe = 0,3.28+ 16 - 0.3.44 = 11,2 (g)
2, Áp dụng định luật bảo toàn nguyên tố Fe, ta có
nFe(sau phản ứng) = nfe(fexOy) = \(\dfrac{11,2}{56}\)= 0,2(mol)
=> mFe(FexOy) = 11,2(g) => mO(fexOy) = 16-11,2= 4,8(g)
=> ta có: \(\dfrac{56x}{16y}\) = \(\dfrac{11,2}{4,8}\)\(\Rightarrow\)\(\dfrac{x}{y}\)=\(\dfrac{2}{3}\)
Vậy công thức oxit sắt là Fe2O3
Thấy ok là phải tích cho tui đó nhá=.=
Đúng 1
Bình luận (1)
Thổi luồng khí CO đến dư qua ống sứ chứa 18,56 gam oxit sắt, nung nóng. Sau khi kết thúc phản ứng, khí thoát ra khỏi ống sứ được hấp thụ hoàn toàn vào dung dịch Ca(OH)2 dư, thu được 34,8 gam kết tủa. Công thức oxit sắt là A. Fe3O4 B. FeO. C. Fe2O3. D. Fe2O3 hoặc Fe3O4
Đọc tiếp
Thổi luồng khí CO đến dư qua ống sứ chứa 18,56 gam oxit sắt, nung nóng. Sau khi kết thúc phản ứng, khí thoát ra khỏi ống sứ được hấp thụ hoàn toàn vào dung dịch Ca(OH)2 dư, thu được 34,8 gam kết tủa. Công thức oxit sắt là
A. Fe3O4
B. FeO.
C. Fe2O3.
D. Fe2O3 hoặc Fe3O4
Chọn C
Quá trình CO phản ứng với oxit chỉ là CO lấy đi O tạo CO2 nên số mol O bị lấy cũng chính bằng số mol CO2. Vì Ca(OH)2 dư ⟹ nCO2 = 34,8/100 = 0,348 = nO bị lấy
⟹ nFe trong oxit = (18,56 – 0,348×16)/56=0,232
⟹ n F e n O = 0 , 232 0 , 348 = 2 3 ⟹ Fe2O3
Đúng 0
Bình luận (0)
yCO+FexOy--t°--> yCO2+xFe
CO2+Ca(OH)2--->CaCO3+H2O nCaCO3=34,8/100=0,348(mol
Theopt2: nCO2=nCaCO3=0,348(mol)
Theo pt1:
nFexOy=1/y.nCO2=0,348/y (mol)
MFexOy=18,56/0,348/y=160y/3(g/mol)
=>56x+16y=160y/3
168x+48y=160y
168x=112y
=>x/y=112/168=2/3
Vậy công thức hoá học của Oxt sắt là Fe2O3
Đúng 0
Bình luận (0)
Thổi một luồng khí CO dư đi qua ống đựng hỗn hợp 2 oxit Fe3O4 và CuO nung nóng đến khi phản ứng xảy ra hoàn toàn thu được 2,32 gam hỗn hợp kim loại. Khí thoát ra được đưa vào bình đựng dung dịch Ca(OH)2 dư thấy có 5 gam kết tủa trắng. Khối lượng hỗn hợp 2 oxit kim loại ban đầu là
Ta có : nO(trong oxit) = nCO = nCO2 = nCaCO3 = 0,05 mol
moxit = mKL + moxi trong oxit = 2,32 + 0,05.16 = 3,12 gam
Đúng 4
Bình luận (0)
Dẫn khí CO dư đi qua ống sứ đựng bột oxit sắt nung nóng. Dẫn hết khí sinh ra vào dung dịch Ca(OH)2, thu được 8 gam kết tủa. Hòa tan hết lượng Fe thu được ở trên bằng dung dịch H2SO4 loãng, dư thì thoát ra 1,344 lít H2 (đktc). Công thức oxit sắt đem dùng là
$CO + O_{oxit} \to CO_2$
$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
$n_{O(oxit)} = n_{CaCO_3} = \dfrac{8}{100} = 0,08(mol)$
$Fe + H_2SO_4 \to FeSO_4 + H_2$
$n_{Fe} = n_{H_2} = \dfrac{1,344}{22,4} = 0,06(mol)$
Ta có :
$n_{Fe} : n_O = 0,06 : 0,08 = 3 : 4$
Vậy oxit là $Fe_3O_4$
Đúng 3
Bình luận (0)
Công thức oxit sắt có dạng: \(Fe_xO_y\)
\(Fe_xO_y+yCO\rightarrow xFe+yCO_2\uparrow\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
\(\Rightarrow n_{Fe}=n_{H_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\)
\(\Rightarrow n_{CO}=n_{CO_2}=n_{CaCO_3}=0,08\left(mol\right)\)
\(\Rightarrow n_{O\left(Fe_xO_y\right)}=n_{O\left(CO_2\right)}-n_{O\left(CO\right)}=2n_{CO_2}-n_{CO}=0,08\left(mol\right)\)
\(\Rightarrow n_{Fe}:n_O=0,06:0,08=3:4\)
\(\Rightarrow Fe_3O_4\)
Đúng 1
Bình luận (0)
\(Co+\left\{{}\begin{matrix}Fe:amol\\O:bmol\end{matrix}\right.\)\(\rightarrow\left[{}\begin{matrix}Fe\rightarrow H_2SO_4\\Co_2\rightarrow Ca\left(OH\right)_2\rightarrow caCo_3\end{matrix}\right.\)
\(\cdot m\downarrow=m_{CaCo_3}=8\Rightarrow n_{CaCo_3}=n_{Co_2}=\dfrac{8}{100}=0,08\)
\(\Rightarrow n_O=n_{CO}=n_{CO_2}=0,08\)
\(\cdot Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,06 0,06
\(n_{H_2}=\dfrac{1,344}{22,4}=0,06\Rightarrow n_{Fe}=n_{H_2}=0,06\)
\(\Rightarrow\dfrac{n_{Fe}}{n_O}=\dfrac{0,06}{0,08}=\dfrac{3}{4}\Rightarrow Fe_3O_4\)
Đúng 0
Bình luận (0)
Dùng CO để khử oxit sắt từ và H2 khử sắt (III) oxit ở nhiệt độ cao . Khối lượng sắt thu được ở hai thí nghiệm là 266g.
b) Khí sinh ra từ một trong hai phản ứng trên được dẫn vào bình chứa dung dịch Ca(OH)2 dư thấy xuất hiện kết tủa trắng có m là 200g
-Tính VCO và VH2 đã tham gia phản ứng
- Tính khối lượng mỗi oxit sắt đã tham gia phản ứng
\(n_{CaCO_3}=\dfrac{200}{100}=2\left(mol\right)\)
PTHH: CO2 + Ca(OH)2 ---> CaCO3 + H2O
2 2
\(n_{Fe}=\dfrac{266}{56}=4,75\left(mol\right)\)
PTHH:
Fe2O3 + 3CO --to--> 3CO2 + 2Fe
\(\dfrac{1}{3}\) 2 2 \(\dfrac{2}{3}\)
=> nFe (H2) = \(4,75-\dfrac{2}{3}=\dfrac{49}{12}\left(mol\right)\)
Fe2O3 + 3H2 --to--> 2Fe + 3H2O
\(\dfrac{49}{24}\) 6,125 \(\dfrac{49}{12}\)
\(\rightarrow\left\{{}\begin{matrix}V_{CO}=2.22,4=44,8\left(l\right)\\V_{H_2}=6,125.22,4=137,2\left(l\right)\\m_{Fe_2O_3}=\left(\dfrac{1}{3}+\dfrac{49}{24}\right).160=380\left(g\right)\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Hòa tan hết m gam hỗn hợp X gồm FeS2, FeS và Fe bằng dung dịch H2SO4 đặc nóng dư thu được dung dịch Y và khí Z. Hấp thụ hết Z vào 100ml dung dịch hỗn hợp Na2SO3 3M và NaOH 4M thu được dung dịch A chứa hai muối Na2SO3 và NaHSO3 với tỉ lệ mol 2 : 1. Cho Y tác dụng với dung dịch NaOH dư, lọc kết tủa nung đến khối lượng không đổi thu được chất rắn B. Cho khí CO đi qua ống sứ chứa toàn bộ chất rắn B, nung nóng thu được 5,76 gam hỗn hợp D gồm Fe và các oxit của Fe. Hấp thụ hết khí sinh ra vào bình chứ...
Đọc tiếp
Hòa tan hết m gam hỗn hợp X gồm FeS2, FeS và Fe bằng dung dịch H2SO4 đặc nóng dư thu được dung dịch Y và khí Z. Hấp thụ hết Z vào 100ml dung dịch hỗn hợp Na2SO3 3M và NaOH 4M thu được dung dịch A chứa hai muối Na2SO3 và NaHSO3 với tỉ lệ mol 2 : 1. Cho Y tác dụng với dung dịch NaOH dư, lọc kết tủa nung đến khối lượng không đổi thu được chất rắn B. Cho khí CO đi qua ống sứ chứa toàn bộ chất rắn B, nung nóng thu được 5,76 gam hỗn hợp D gồm Fe và các oxit của Fe. Hấp thụ hết khí sinh ra vào bình chứa dung dịch Ca(OH)2 dư thì thu được 4 gam kết tủa. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 6,40
B. 7,28
C. 7,04
D. 6,72
Cho V lít khí CO đktc đi qua ống sứ chứa 2,32g oxit sắt kim loại nung nóng đến phản ứng hoàn toàn thu được m gam kim loại và hỗn hợp khí có tỉ khối so với H2 bằng 18.Dẫn toàn bộ lượng khí này vào bình chứa 2000ml dung dịch Ca(OH)2 0,015M.Kết thúc phản ứng thu được 2g kết tủa và dung dịch A.Lọc tách kết tủa rồi cho dung dịch Ba(OH)2 dư vào dung dịch A ta thu được p gam kết tủa.Cho toàn bộ lượng kim loại thi được ở trên vào bình chứa dung dịch HCl dư,phản ứng kết thúc ta thu được 0,672 lít khí H2...
Đọc tiếp
Cho V lít khí CO đktc đi qua ống sứ chứa 2,32g oxit sắt kim loại nung nóng đến phản ứng hoàn toàn thu được m gam kim loại và hỗn hợp khí có tỉ khối so với H2 bằng 18.Dẫn toàn bộ lượng khí này vào bình chứa 2000ml dung dịch Ca(OH)2 0,015M.Kết thúc phản ứng thu được 2g kết tủa và dung dịch A.Lọc tách kết tủa rồi cho dung dịch Ba(OH)2 dư vào dung dịch A ta thu được p gam kết tủa.Cho toàn bộ lượng kim loại thi được ở trên vào bình chứa dung dịch HCl dư,phản ứng kết thúc ta thu được 0,672 lít khí H2 đktc.Viết các PTHH xảy ra.Tính C,m,p và xác định CT của oxit kim loại
Khử hoàn toàn 5,76 gam một oxit sắt bằng dòng khí CO dư thu được 4,48 lít Hỗn hợp khí A (đktc) .Hấp thụ khí A vào dung dịch chứa 6,96 gam Ca(OH)2 đến khi phản ứng kết thúc thì thu được m gam kết tủa trắng .lọc lấy kết tủa nung đến khối lượng không đổi thì thấy chất rắn giảm 3,52 gam.Xác định công thức của Oxit sắt và tính tỉ khối của A so với H2.
Lười gõ quá nên mình không làm chi tiết, không hiểu cái nào thì hỏi:v
Đặt CTHH của oxit sắt là \(Fe_xO_y\)
\(m_{giảm}=3,52\Rightarrow m_{CO_2}=3,52\left(g\right)\Rightarrow n_{CO_2}=\dfrac{3,52}{44}=0,08\left(mol\right)\)
\(\Rightarrow\dfrac{0,08}{y}=n_{Fe_xO_y}=\dfrac{5,76}{56x+16y}\)
\(\Rightarrow x:y=1:1\)
\(\Rightarrow CT:FeO\)
\(n_A=\dfrac{4,48}{22,4}=0,2\left(mol\right)\Rightarrow n_{CO}=0,2-0,08=0,12\left(mol\right)\)
\(\Rightarrow m_{CO}+m_{CO_2}=44.0,08+0,12.28=6,88\)
\(\Rightarrow d_{A/H_2}=\dfrac{6,88}{2}=3,44\)
Đúng 2
Bình luận (2)
câu 1 thổi 8,96 lít CO (dktc) qua 16 g một oxit sắt nung nóng.Dẫn toàn bộ khí sau phan rứng qua dung dịch Ca(OH)2 dư , tạo ra 30g kết tủa trắng (CaCO3), các phản ứng xảy ra hoàn toàn 1. tính khối lượng Fe thu dc 2. xác định công thức oxit sắtcâu 2 1. hòa tan 19,21g hỗn hợp Al,Mg,Al2O3,MgO trong dung dịch HCL , thấy thoát ra 0,896 lít H2(dktc) , sinh ra 0,18g H2O và còn lại 4,6g chất rắn ko tan . cô cạn dung dịch sau phản ứng thì thu dc m gam muối khan . tính m (biết oxit bazơ tác dụng với axit t...
Đọc tiếp
câu 1
thổi 8,96 lít CO (dktc) qua 16 g một oxit sắt nung nóng.Dẫn toàn bộ khí sau phan rứng qua dung dịch Ca(OH)2 dư , tạo ra 30g kết tủa trắng (CaCO3), các phản ứng xảy ra hoàn toàn
1. tính khối lượng Fe thu dc
2. xác định công thức oxit sắt
câu 2
1. hòa tan 19,21g hỗn hợp Al,Mg,Al2O3,MgO trong dung dịch HCL , thấy thoát ra 0,896 lít H2(dktc) , sinh ra 0,18g H2O và còn lại 4,6g chất rắn ko tan . cô cạn dung dịch sau phản ứng thì thu dc m gam muối khan . tính m (biết oxit bazơ tác dụng với axit tạo muối và nước ).
2. nhiệt phân 8,8g C3H8 thu dc hốn hợp khí X gầm CH4 , C2H4, C3H6, H2, C3H8 dư . các phản ứng như sau.
C3H8 ->CH4+ C2H4
C3H8 ->C3H6+ H2
tính khối lượng CO2 , khối lượng H2O thu dc khi đốt cháy hoàn toàn X.
câu 3
1. hòa tan hoàn toàn 17,8 gam hỗn hợp gồm mất kim loại R (hóa trị 1 ) và oxit của nó vào H2O , thu dc 0,6 mol ROH và 1,12 lít H2 ( ở dktc)
a) Xác định R
b) giả sử bài toán ko cho thể tích H2 thoát ra . hãy xác định R
2. đưa hỗn hợp khí gồm N2 và H2 có tỉ lệ mol tương ứng là 1:3 vào tháp tổng hợp NH3 sau phản ứng thấy thể tích khí đi ra giảm 1/10 so với ban đầu . tính hiệu suất phản ứng ( biết các khí đo ở cừng điều kiện )
câu 4
Y là hợp chất chứa 3 nguyên tố C ,H , O. trộn 1,344 lít CH4 với 2,688 lít khí Y thu dc 4,56g hỗn hợp khí Z . đốt cháy hoàn toàn Z thu dc 4,032 lít CO2 (các khí đo ở dktc)
1.tính khối lượng mol của Y
2.xác định công thức phân tử Y
Câu 1:
1) \(n_{CaCO_3}=\dfrac{30}{100}=0,3\left(mol\right)\)
=> \(n_{CO_2}=0,3\left(mol\right)\)
=> nO = 0,3 (mol)
=> mFe = 16 - 0,3.16 = 11,2 (g)
2) \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Xét nFe : nO = 0,2 : 0,3 = 2 : 3
=> CTHH: Fe2O3
Đúng 2
Bình luận (0)
n CaCO3=\(\dfrac{30}{100}\)=0,3 mol
bảo toàn nt:
CO+O->CO2
->nO=nCaCO3=0,3 mol
mFe =16-0,3.16=11,2g
->n Fe=\(\dfrac{11,2}{56}\)=0,2 mol
->\(\dfrac{nFe}{nO}=\dfrac{0,2}{0,3}=\dfrac{2}{3}\)
Công thức Sắt là Fe2O3
Đúng 2
Bình luận (0)
Câu 2:
1) \(n_{H_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
\(n_{H_2O}=\dfrac{0,18}{18}=0,01\left(mol\right)\)
=> nHCl = 0,1 (mol)
mchất rắn pư = 19,21 - 4,6 = 14,61 (g)
BTKL: mchất rắn pư + mHCl = mmuối + mH2 + mH2O
=> mmuối = 14,61 + 0,1.36,5 - 0,04.2 - 0,01.18 = 18 (g)
2)
\(n_{C_3H_8}=\dfrac{8,8}{44}=0,2\left(mol\right)\)
Bảo toàn C: nCO2 = 0,6 (mol) => mCO2 = 0,6.44 = 26,4 (g)
Bảo toàn H: nH2O = 0,8 (mol) => mH2O = 0,8.18 = 14,4 (g)
Đúng 2
Bình luận (0)
Xem thêm câu trả lời