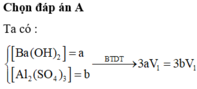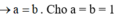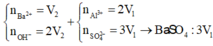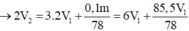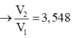Dung dịch X gồm Al2(SO4)3 0,75M và H2SO4 0,75M. Cho V1 ml dd KOH 1 M vào 100ml dd X thu được 3,9g kết tủa. Mặt khác cho V2 ml dd KOH 1M vào 100ml dd X cũng thu được 3,9g kết tủa. Biết các phản ứng xảy ra hoàn toàn. Tìm V2:V1

Những câu hỏi liên quan
Dung dịch X gồm Al2(SO4)3 0,75M và H2SO4 0,75M. Cho V1 ml dung dịch KOH 1M vào 100 ml dung dịch X, thu được 3,9 gam kết tủa. Mặt khác, khi cho V2 ml dung dịch KOH 1M vào 100 ml dung dịch X cũng thu được 3,9 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Tỉ lệ V2: V1 là A. 4 : 3. B. 25 : 9. C. 13 : 9. D. 7 : 3.
Đọc tiếp
Dung dịch X gồm Al2(SO4)3 0,75M và H2SO4 0,75M. Cho V1 ml dung dịch KOH 1M vào 100 ml dung dịch X, thu được 3,9 gam kết tủa. Mặt khác, khi cho V2 ml dung dịch KOH 1M vào 100 ml dung dịch X cũng thu được 3,9 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Tỉ lệ V2: V1 là
A. 4 : 3.
B. 25 : 9.
C. 13 : 9.
D. 7 : 3.
Dung dịch X gồm Al2(SO4)3 0,75M và H2SO4 0,75M. Cho V1 ml dung dịch KOH 1M vào 100 ml dung dịch X, thu được 3,9 gam kết tủa. Mặt khác, khi cho V2 ml dung dịch KOH 1M vào 100 ml dung dịch X cũng thu được 3,9 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Tỉ lệ V2: V1 là: A. 4 : 3. B. 25 : 9. C. 13 : 9. D. 7 : 3.
Đọc tiếp
Dung dịch X gồm Al2(SO4)3 0,75M và H2SO4 0,75M. Cho V1 ml dung dịch KOH 1M vào 100 ml dung dịch X, thu được 3,9 gam kết tủa. Mặt khác, khi cho V2 ml dung dịch KOH 1M vào 100 ml dung dịch X cũng thu được 3,9 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Tỉ lệ V2: V1 là:
A. 4 : 3.
B. 25 : 9.
C. 13 : 9.
D. 7 : 3.
vẽ đồ thị dung dịch X gồm Al2(So4)3 0.75M và H2SO4 0.75M.Cho V1 ml dd KOH 1M vào 100ml ddX,thu đc 3.9 g kết tủa.Mặt khác,khi cho V2 ml dd KOH vào 100ml X cũng thu đc 3.9 g kết tủa.V2:V1 là
2)
\(\dfrac{2}{x-1}+\dfrac{4}{x+3}=3\\ ĐKXĐ:\left[{}\begin{matrix}x-1\ne0\\x+3\ne0\end{matrix}\right.\Leftrightarrow\left[{}\begin{matrix}x\ne1\\x\ne-3\end{matrix}\right.\)
\(\Leftrightarrow\dfrac{2\left(x+3\right)+4\left(x-1\right)}{\left(x-1\right)\left(x+3\right)}=\dfrac{3\left(x-1\right)\left(x+3\right)}{\left(x-1\right)\left(x+3\right)}\\ \Leftrightarrow2x+6+4x-4=3\left(x^2+2x-3\right)\\ \Leftrightarrow6x+2=3x^2+6x-9\\ \Leftrightarrow3x^2+6x-6x-9-2=0\\ \Leftrightarrow3x^2-11=0\\ \Leftrightarrow x=\pm\sqrt{\dfrac{11}{3}}\left(TMĐK\right)\)
Đúng 0
Bình luận (0)
cho 200ml dung dịch chứa naoh 1M và KOH 1,5M vào 100ml dd chứa hcl 0,5M và AlCl3 xM. Sau khi các phản ứng xảy ra hoàn toàn thu được 3,9g kết tủa. Tính giá trị của x ( giai bang 2 truong hop giup em voi a)
Ta có: \(n_{NaOH}=0,2.1=0,2\left(mol\right)\)
\(n_{KOH}=0,2.1,5=0,3\left(mol\right)\)
\(\Rightarrow n_{OH^-}=n_{NaOH}+n_{KOH}=0,5\left(mol\right)\)
\(n_{HCl}=0,1.0,5=0,05\left(mol\right)=n_{H^+}\)
\(n_{AlCl_3}=0,1x\left(mol\right)=n_{Al^{3+}}\)
\(n_{Al\left(OH\right)_3}=\dfrac{3,9}{78}=0,05\left(mol\right)\)
TH1: Kết tủa chưa bị hòa tan
PT: \(H^++OH^-\rightarrow H_2O\)
_____0,05____0,05 (mol)
\(Al^{3+}+3OH^-\rightarrow Al\left(OH\right)_3\)
_________0,15_________0,05 (mol)
⇒ nOH- (pư) = 0,05 + 0,15 = 0,2 (mol) → OH- dư
⇒ Kết tủa phải bị hòa tan 1 phần.
→ Loại TH1.
TH2: Kết tủa đã bị hòa tan 1 phần.
PT: \(H^++OH^-\rightarrow H_2O\)
____0,05____0,05 (mol)
\(Al^{3+}+3OH^-\rightarrow Al\left(OH\right)_3\)
0,1x______0,3x________0,1x (mol)
\(Al\left(OH\right)_3+OH^-\rightarrow AlO_2^-+2H_2O\)
0,1x-0,05____0,1x-0,05 (mol)
⇒ 0,05 + 0,3x + 0,1x - 0,05 = 0,5 ⇒ x = 1,25 (M)
Đúng 3
Bình luận (0)
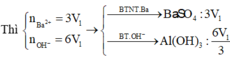
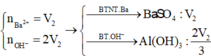
Nhỏ từ từ 3 V1 ml dung dịch Ba(OH)2 (dd X) vào V1 ml dung dịch Al2(SO4)3 (dd Y) thì phản ứng vừa đủ và ta thu được kết tủa lớn nhất là m gam. Nếu trộn V2 ml dung dịch X ở trên vào V1 ml dung dịch Y thì kết tủa thu được có khối lượng bằng 0,9m gam. So sánh tỉ lệ V2 / V1 thấy A. V2 / V1 2,7 hoặc V2 / V1 3,55 B. V2 / V1 2,5 hoặc V2 / V1 3,25 C. V2 / V1 2,7 hoặc V2 / V1 3,75 D. V2 / V1 2,5 hoặc V2 / V1 3,55
Đọc tiếp
Nhỏ từ từ 3 V1 ml dung dịch Ba(OH)2 (dd X) vào V1 ml dung dịch Al2(SO4)3 (dd Y) thì phản ứng vừa đủ và ta thu được kết tủa lớn nhất là m gam. Nếu trộn V2 ml dung dịch X ở trên vào V1 ml dung dịch Y thì kết tủa thu được có khối lượng bằng 0,9m gam. So sánh tỉ lệ V2 / V1 thấy
A. V2 / V1 = 2,7 hoặc V2 / V1 = 3,55
B. V2 / V1 = 2,5 hoặc V2 / V1 = 3,25
C. V2 / V1 = 2,7 hoặc V2 / V1 = 3,75
D. V2 / V1 = 2,5 hoặc V2 / V1 = 3,55
Cho 100ml dd A gồm NaOH xM & Ba(OH)2 1,5M vào 100ml dd B gồm H2SO4 1M & AlCl; y M thu được 31,1 gam kết tủa. Cho 150 ml dd A tác dụng với 200 ml dd B thu được 63,5 gam kết tủa . Tính x, y ?
Xem chi tiết
cho hỗn hợp x bao gồm al2(so4)3 0,75m và h2so4 xm
khi ta cho vào 300 ml dd koh ym vào 100ml x thu được 3,9 gam kết tủa
mặt khác khi ta cho vào 700 ml dd koh ym vào 100 ml x vẫn thu được 3,9 gam kết tủa
tìm nồng độ x và y
bài này kq giải ra x = 1,5 y = 1 bài này khá hay nên mình đăng lên cho 500 ae giải ae cố gắng giải nhe
Dung dịch X chứa KOH 1M và Ba(OH)2 0,5M. Dung dịch Y chứa Al(NO3)3 2M và Al2(SO4)3 0,5M. Cho V1 lít dd X vào V2 lít dd Y, sau khi các phản ứng xảy ra hoàn toàn thu được 56,916g kết tủa. Nếu cho dd Ba(NO3)2 vào V2 lít dd Y thu được 41,94g kết tủa. Tính V1, V2
nBaSO4 = 0,18 mol
→nAl2(SO4)3 = 0,06
→V2 = 0,12 (l) → nAl3+=0,24 , nSO42-= 0,18 mol
nBa2+ = 0,5V1 mol
nOH- = 2V1 + 0,5V1 < 0,18
→ nOH- < 3nAl3+
→ Kết tủa tính theo Ba2+ và OH-
→ 56,916 = 233.0,5V1 + 78.2V1/3
→V1= 0,34 + 0,5V1 ≥ 0,18
→ nBaSO4 = 0,18 mol
→ nAl(OH)3 =0,192 mol
→ nOH- = 2V1 = 4nAl3+ − nkt = 0,768 mol
→ V1=0,384 (l)
Cù Văn Thái Giúp e với thầy
V1 = 288 ml
V2 = 156 ml
Xem thêm câu trả lời
cho 200ml dung dịch chứa naoh 1M và KOH 1,5M vào 100ml dd chứa hcl 0,5M và AlCl3 xM. Sau khi các phản ứng xảy ra hoàn toàn thu được 3,9g kết tủa. Tính giá trị của x
\(n_{Al\left(OH\right)_3}=\dfrac{3,9}{78}=0,05mol\)
\(n_{NaOH}=0,2mol\)
\(n_{KOH}=0,2.1,5=0,3mol\)
\(\rightarrow n_{OH^-}=0,2+0,3=0,5mol\)
\(n_{H^+}=n_{HCl}=0,05mol\)
\(n_{Al^{3+}}=0,1xmol\)
H++OH-\(\rightarrow\)H2O
\(n_{OH^-\left(pu\right)}=n_{H^+}=0,05mol\)
\(n_{OH^-\left(dư\right)}=0,5-0,05=0,45mol\)
Al3++3OH-\(\rightarrow\)Al(OH)3(1)
Al(OH3+OH-\(\rightarrow\)AlO2-+H2O(2)
- Sau phản ứng (2) Al(OH)3 còn dư 0,05 mol
\(n_{OH^-\left(1\right)}=3n_{Al^{3+}}=0,3xmol\)
\(n_{Al\left(OH\right)_3\left(1\right)}=n_{Al^{3+}}=0,1xmol\)
\(n_{Al\left(OH\right)_3\left(2\right)}=0,1x-0,05\) mol
\(n_{OH^-\left(2\right)}=n_{Al\left(OH\right)_3\left(2\right)}=0,1x-0,05\)
Theo PTHH (1,2) ta có:
\(n_{OH^-}=n_{OH^-\left(1\right)}+n_{OH^-\left(2\right)}\)
\(\rightarrow\)0,45=0,3x+0,1x-0,05\(\rightarrow\)0,4x=0,5\(\rightarrow\)x=1,25M
Đúng 0
Bình luận (0)