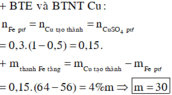nhúng 1 thanh Fe có khối lượng 50 g vào 400ml dd CuSO4sau 1 thời giam pư khối lượng thanh Fe 4%
a Xđ mCu thoát ra
b Tính Cm /l của FeSO4 . Gỉa sử thể tích tăng không đáng kể
mọi người giúp mik với .... mik cần gấp... và gải cụ thể cho mik nhé
CẢM ƠN Ạ !!!!!!!!