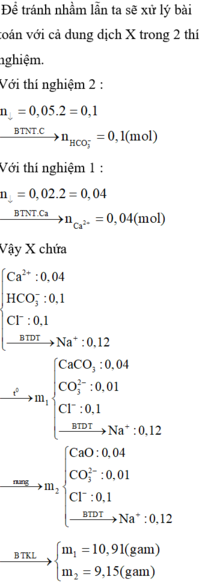Có 166,5 gam dung dịch MSO4 41,561%ở 100°C .Hạ nhiệt độ dung dịch xuống 20°C thì thấy có m1 gam MSO4×5H20 kết tinh và còn lại m2 gam dung dịch X. Biết m1-m2 =6,5 và độ tan của MSO4 ở 20°C là 20,92 gam trong 100gam H2O. Xác định công thức muối MSO4

Những câu hỏi liên quan
Có 166,5 gam dung dịch MSO4 41,561%ở 100°C .Hạ nhiệt độ dung dịch xuống 20°C thì thấy có m1 gam MSO4×5H20 kết tinh và còn lại m2 gam dung dịch X. Biết m1-m2 =6,5 và độ tan của MSO4 ở 20°C là 20,92 gam trong 100gam H2O. Xác định công thức muối MSO4
Pha trộn m1(g) dung dịch chứa chất tan X nồng độ C1% với m2 (g) dung dịch cũng chứa chất tan X nồng độ C2%, thu được dung dịch có nồng độ C3%. Thiết lập biểu thức liên hệ giữa m1, m2, C1, C2, C3.2. Khi cho 2 gam MgSO4 khan vào 200 gam dung dịch MgSO4 bão hòa ở ^{ }t^o C đã làm cho m gam muối kết tinh lại. Nung m gam tinh thể muối kết tinh đó đến khối lượng không đổi, được 3,16 gam MgSO4 khan. Xác định công thức phân tử của tinh thể muối MgSO4 kết tinh (biết độ tan của MgSO4 ở toC là 35,1 gam).
Đọc tiếp
Pha trộn m1(g) dung dịch chứa chất tan X nồng độ C1% với m2 (g) dung dịch cũng chứa chất tan X nồng độ C2%, thu được dung dịch có nồng độ C3%. Thiết lập biểu thức liên hệ giữa m1, m2, C1, C2, C3.2. Khi cho 2 gam MgSO4 khan vào 200 gam dung dịch MgSO4 bão hòa ở \(^{ }t^o\) C đã làm cho m gam muối kết tinh lại. Nung m gam tinh thể muối kết tinh đó đến khối lượng không đổi, được 3,16 gam MgSO4 khan. Xác định công thức phân tử của tinh thể muối MgSO4 kết tinh (biết độ tan của MgSO4 ở toC là 35,1 gam).
lớp 5 ?
xác định khối lượng NaNO3 kết tinh khi hạ nhiệt độ của 168 g dung dịch NaNO3 bão hòa từ 100 độ C xuống 20 độ C. Biết độ tan của NaNO3 ở 100 độ C là 180 gam và có 88 gam
Ở `100^oC` : `m_(NaNO_3) = (180 . 168)/(180+100) =108g`
`-> m_(H_2O) = 168 -108 = 60g`
Ở `20^o` : `m_(NaNO_3) = (60 . 88)/(100) =52,8g`
Vậy `m_(NaNO_3 (kt)) = 108 - 52,8 =55,2g`
Công thức :
- Ở nhiệt độ `t_1` biết `S_1 -> m_(ct_1) = (md^2 . S_1)/(100+S_1)`
Suy ra `m_(H_2O) = m_(dd1) - m_(ct_1)`
- Ở nhiệt độ `t_2` biết `S_2 -> m_(ct_2) = (m_(H_2O) . S_2)/(100)`
Giả sử `t_1 >t_2` : Khối lượng kết tinh khi hạ nhiệt : `m_(ct_1)-m_(ct_2)`
Đúng 4
Bình luận (0)
a) Trộn 500 gam dung dịch HCl 3% vào 300 gam dung dịch HCl 10% thì thu được dung dịch có nồng độ bao nhiêu % ?
b) Tính khối lượng NaCl kết tinh khi hạ nhiệt tinh của 1800 gam dung dịch NaCl 30% ở 40 độ C xuống 20 độ C . Biết độ tan ở 20 độ C là 36 gam
a) Số gam chất tan có trong 500g dd HCl 3% là:
\(m_{HCl}=\dfrac{500.3}{100}=15\left(g\right)\)
Số gam chất tan có trong 300g dd HCl 10%:
\(m_{HCl}=\dfrac{300.10}{100}=30\left(g\right)\)
Nồng độ phần trăm dd axit mới:
\(C\%_{ddHCl\left(mới\right)}=\dfrac{15+30}{500+300}.100=5,625\%\)
Đúng 0
Bình luận (0)
a) - Khối lượng HCl trong 500 gam dung dịch 3% : \(\dfrac{500\cdot3}{100}\)
- Khối lượng HCl trong 300 gam dung dịch 10% : \(\dfrac{300\cdot10}{100}\)
- Tính theo công thức tính nồng độ phần trăm :
\(\dfrac{\left[\left(\dfrac{500\cdot3}{100}\right)+\left(\dfrac{300\cdot10}{100}\right)\right]\cdot100\%}{\left(500+300\right)}=5,625\%\)
b) Khối lượng NaCl trong 1800 gam dung dịch 30%
\(\dfrac{1800\cdot30}{100}=540\left(g\right)\)
Khối lượng nước : 1800 - 540 = 1260 ( g )
Khối lượng muối tan bão hòa trong 1260 gam nước ở 20oC :
\(\dfrac{36\cdot1260}{100}=453,6\left(g\right)\)
Lượng muối kết tinh : 540 - 453,6 = 86,4 ( g )
Đúng 0
Bình luận (0)
b) Số gam muối NaCl có trong 1800g dd NaCl 30% ở 40oC:
\(m_{NaCl}=\dfrac{1800.30}{100}=540\left(g\right)\)
Số gam muối NaCl có trong 1800g dd NaCl 30% ở 20 độ C:
\(m_{NaCl}=\dfrac{1800.36}{100}=648\left(g\right)\)
Số gam muối NaCl kết tinh:
\(m_{NaCl\left(kết-tinh\right)}=648-540=108\left(g\right)\)
ko chắc câu b lắm đâu nhé!
Đúng 0
Bình luận (0)
Dung dịch X chứa các ion: Ca2+, Na+, HCO3– và Cl–, trong đó số mol của ion Cl– là 0,1. Thí nghiệm 1: cho 1/2 dung dịch X phản ứng với dung dịch NaOH dư, thu được 2 gam kết tủa. Thí nghiệm 2: Cho 1/2 dung dịch X còn lại phản ứng với dung dịch Ca(OH)2 dư, thu được 5 gam kết tủa. Mặt khác, nếu đem đun nóng để cô cạn dung dịch X thì thu được m1 gam chất rắn khan Y, lấy m1 gam chất rắn khan Y trên nung ở nhiệt độ cao đến khối lượng không đổi thu được m2 gam chất rắn khan Z. Giá trị của m1 và m2 lầ...
Đọc tiếp
Dung dịch X chứa các ion: Ca2+, Na+, HCO3– và Cl–, trong đó số mol của ion Cl– là 0,1.
Thí nghiệm 1: cho 1/2 dung dịch X phản ứng với dung dịch NaOH dư, thu được 2 gam kết tủa.
Thí nghiệm 2: Cho 1/2 dung dịch X còn lại phản ứng với dung dịch Ca(OH)2 dư, thu được 5 gam kết tủa.
Mặt khác, nếu đem đun nóng để cô cạn dung dịch X thì thu được m1 gam chất rắn khan Y, lấy m1 gam chất rắn khan Y trên nung ở nhiệt độ cao đến khối lượng không đổi thu được m2 gam chất rắn khan Z. Giá trị của m1 và m2 lần lượt là:
A. 10,26 và 8,17
B. 14,01 và 9,15
C. 10,91 và 8,71
D. 10,91 và 9,15
Có 166,5 gam chât rắn MSO4 41,561 % ở 100 °C .Hạ nhiệt độ dd xuống 20°C thì thấy có m1 gam MSO4×5H2O kết tinh và còn lại m2gam dd X .Biết m1-m2=6,5 và độ tan của MSO4 ở 20°C là 20,29 gam trong 100 gam H2O .Xác định công thức muối MSO4
Hòa tan m1 gam Na vào m2 gam H2O thu được dung dịch B có khối lượng riêng là d. Viết phương trình phản ứng. 1. Tính nồng độ % của dung dịch B theo m1 và m2. 2. Cho C% = 5%, d = 1,2g/ml. Tính nồng độ mol của dung dịch thu được.
\(Na+H_2O->NaOH+\dfrac{1}{2}H_2\\ a.n_{Na}=\dfrac{m_1}{23}\left(mol\right)\\ m_{ddsau}=\dfrac{m_1}{23}+m_2-\dfrac{m_1}{46}=\dfrac{m_1}{46}+m_2\left(g\right)\\ C\%_B=\dfrac{\dfrac{40}{23}m_1}{\dfrac{m_1}{46}+m_2}\cdot100\%.\\ b.C_M=\dfrac{10dC\%}{M}=10\cdot1,2\cdot\dfrac{0,05}{40}=0,015\left(M\right)\)
Đúng 1
Bình luận (0)
\(Na+H_2O->NaOH+\dfrac{1}{2}H_2\\ a.n_{Na}=\dfrac{m_1}{23}\left(mol\right)\\ m_{ddsau}=m_1+m_2-\dfrac{m_1}{23}=\dfrac{22}{23}m_1+m_2\left(g\right)\\ C\%_B=\dfrac{\dfrac{40}{23}m_1}{\dfrac{22}{23}m_1+m_2}\cdot100\%.\\ b.C_M=\dfrac{10dC\%}{M}=10\cdot1,2\cdot\dfrac{0,05}{40}=0,015\left(M\right)\)
Đúng 0
Bình luận (1)
100 ml dung dịch KOH 2M tác dụng với 100 ml dung dịch hỗn hợp H2 SO4 0,4 m và mgso4 0,8 m thu được M1 gam kết tủa và dung dịch X nung kết tủa đến khi khối lượng không thay đổi thì được m2 gam chất rắn tính m1 m2 nồng độ mol chất có trong X
\(n_{KOH}=0,1.2=0,2mol\\ n_{MgSO_4}=0,1.0,8=0,08mol\\ n_{H_2SO_4}=0,1.0,4=0,04mol\)
Vì bazo và axit luôn pư trc nên H2SO4 hết MgSO4 dư.
\(2KOH+H_2SO_4\rightarrow K_2SO_4+2H_2O\)
0,08 0,04 0,04 0,08
\(2KOH+MgSO_4\rightarrow Mg\left(OH\right)_2+K_2SO_4\)
0,12 0,06 0,06 0,06
\(Mg\left(OH\right)_2\underrightarrow{t^0}MgO+H_2O\)
0,06 0,06 0,06
\(m_1=m_{Mg\left(OH\right)_2}=0,06.58=3,48g\\ m_2=m_{MgO}=0,06.40=2,4g\\ C_{M\left(K_2SO_4\right)}=\dfrac{0,04+0,06}{0,1+0,1}=0,5M\\ C_{M\left(MgSO_4\right)}=\dfrac{0,08-0,06}{0,1+0,1}=0,1M\)
Đúng 3
Bình luận (0)
Cho 19,5 gam gồm kim loại M hóa trị II, oxit và muối caccbonat của kim loại đó tan vào dd H2SO4 loãng dư thu được dd M1 và 8,4 lít một chất khí ở đktc. Cho dung dịch NaOH dư vào M1 thu được kết tủa M2. Nung M2 đến nhiệt độ cao thì còn lại 21 gam chất rắn.Mặt khác, cho lượng hỗn hợp trên vào 0,3 lít dd CuSO4 2M. Sau khi phản ứng kết thúc, tách bỏ chất kết tủa rồi đem cô cạn dd thì thu được 76,8 gam chất rắn. Xác định kim loại.
Đọc tiếp
Cho 19,5 gam gồm kim loại M hóa trị II, oxit và muối caccbonat của kim loại đó tan vào dd H2SO4 loãng dư thu được dd M1 và 8,4 lít một chất khí ở đktc. Cho dung dịch NaOH dư vào M1 thu được kết tủa M2. Nung M2 đến nhiệt độ cao thì còn lại 21 gam chất rắn.
Mặt khác, cho lượng hỗn hợp trên vào 0,3 lít dd CuSO4 2M. Sau khi phản ứng kết thúc, tách bỏ chất kết tủa rồi đem cô cạn dd thì thu được 76,8 gam chất rắn.
Xác định kim loại.