Hoà tan hoàn toàn 5,58 g hỗn hợp Al , Mg trong 200ml dung dịch HNO3 loãng thu đuoejc 4,032l NO duy nhất (dktc)
A , xác định thành phần trăm về khối lượng mỗi chất trong hỗn hợp đó
B, tính nồng độ mol của HNO3 đã tham gia phảm ứng
hoà tan hoàn toàn 18,54g hỗn hợp A gồm Al và Al2O3 trong dung dịch H2SO4 loãng dư,sau phản ứng thu được 4,032l khí.Tính thành phần phần trăm về khối lượng mỗi chất trong hỗn hợp ban đầu?
Cũng với lượng hỗn hợp A trên hoà tan hoàn toàn bằng dung dịch H2so4 đặc,nóng thu được khí SO2 duy nhất,hấp thụ hoàn toàn lượng khí trên bằng 360ml dung dịch KOH 1M.Tính nồng độ mol các chất trong dung dịch sau phản ứng?
Giả sử: \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Al_2O_3}=y\left(mol\right)\end{matrix}\right.\)
⇒ 27x + 102y = 18,54 (1)
Ta có: \(n_{H_2}=\dfrac{4,032}{22,4}=0,18\left(mol\right)\)
Theo ĐLBT mol e, có: 3x = 0,18.2 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,12\left(mol\right)\\y=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,12.27}{18,54}.100\%\approx17,5\%\\\%m_{Al_2O_3}\approx82,5\%\end{matrix}\right.\)
_ Khi cho hỗn hợp tác dụng với H2SO4 đặc, nóng.
Giả sử: \(n_{SO_2}=a\left(mol\right)\)
Theo ĐLBT mol e, có: 3.0,12 = 2a ⇒ x = 0,18 (mol)
Ta có: \(n_{KOH}=0,36.1=0,36\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{n_{KOH}}{n_{SO_2}}=\dfrac{0,36}{0,18}=2\)
⇒ Pư tạo muối trung hòa K2SO3.
PT: \(SO_2+2KOH\rightarrow K_2SO_3+H_2O\)
___0,18____________0,18 (mol)
\(\Rightarrow C_{M_{K_2SO_3}}=\dfrac{0,18}{0,36}=0,5M\)
Bạn tham khảo nhé!
Hoà tan hoàn toàn 3,42 gam hỗn hợp X (gồm Mg, Al) trong dung dịch HNO3 10% (loãng) thu được dung dịch Y và 2,464 lít khí NO (đktc, sản phẩm khử duy nhất).
a. Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp X.
b. Tính khối lượng dung dịch axit HNO3 cần dùng.
nNO=23a+b=0,11
→a=0,075(mol),b=0,06(mol)
%mMg=(0,075.24/3,42).100%=52,63%
%mAl=100%−52,63%=47,37%
b)
nHNO3=4nNO=0,44(mol)
mdd HNO3=(0,44.63)/10%=277,2(g)
PTHH: \(MgO+2HNO_3\rightarrow Mg\left(NO_3\right)_2+H_2O\) (1)
\(3Mg+8HNO_3\rightarrow3Mg\left(NO_3\right)_2+2NO+4H_2O\) (2)
Ta có: \(n_{NO}=\dfrac{0,336}{22,4}=0,015\left(mol\right)\) \(\Rightarrow n_{Mg}=0,0225\left(mol\right)\)
\(\Rightarrow\%m_{Mg}=\dfrac{0,0225\cdot24}{9,4}\cdot100\%\approx5,74\%\) \(\Rightarrow\%m_{MgO}=94,26\%\)
Theo PTHH: \(\left\{{}\begin{matrix}n_{Mg\left(NO_3\right)_2\left(2\right)}=0,0225mol\\n_{Mg\left(NO_3\right)_2\left(1\right)}=n_{MgO}=\dfrac{9,4-m_{Mg}}{40}=0,2215\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\Sigma n_{Mg\left(NO_3\right)_2}=0,244\left(mol\right)\) \(\Rightarrow m_{Mg\left(NO_3\right)_2}=0,244\cdot148=36,112\left(g\right)\)
Hòa tan hoàn toàn 4g hỗn hợp G gồm Mg và MgO vào lượng vừa đủ dung dịch HNO3 40%, thì thu được 672 ml khí N2 (sản phẩm khử duy nhất ở đkc). a. Tính khối lượng mỗi chất có trong hỗn hợp G. b. Khối lượng dung dịch HNO3. c. Tính nồng độ phần trăm dung dịch muối thu được.
hoà tan 46.4 g hỗn hợp cu và cuo trong 1.5 lít dung dịch hno3 2M thu được 8.96 lít khí no và dung dịch X
a) tinh % khoi luong Cuo trong hon hop
B) tính nồng độ mol các chất trong dung dịch X
B2) hòa tan hoàn toàn 5.5g hỗn hợp bột zn và cuo trong 28ml dung dịch hno3 vừa đủ thu được 2.688l(dktc) khi màu nâu đỏ (sản phẩm khử duy nhất )
a) tính % khối lượng mỗi chất trong hỗn hợp
B) tính nồng độ mol\l dung dịch Hno3 đã dùng
Hoà tan hoàn toàn 7,8 gam hỗn hợp Al và Mg trong dung dịch H2SO4 đăc nóng thu được 8,96 lit khí SO2 ( đtkc) . Xác định thành phần phần trăm về khối lượng của mỗi kim loại trong hỗn hợp.
nSO2= 0,4(mol)
Đặt: nAl=a(mol); nMg=b(mol) (a,b>0)
PTHH: 2 Al + 6 H2SO4(đ) -to-> Al2(SO4)3 + 3 SO2 + 6 H2O
a____________3a______0,5a___________1,5a(mol)
Mg + 2 H2SO4(đ) -to-> MgSO4 + SO2 + 2 H2O
b_____2b________b________b(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}27a+24b=7,8\\1,5a+b=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
=> mMg=0,1.24=2,4(g)
=>%mMg=(2,4/7,8).100=30,769%
=> %mAl= 69,231%
PTHH: \(CaO+2HCl\rightarrow CaCl_2+H_2O\) (1)
\(CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\uparrow\) (2)
a) Ta có: \(n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)=n_{CaCO_3}\)
\(\Rightarrow m_{CaCO_3}=0,2\cdot100=20\left(g\right)\) \(\Rightarrow\%m_{CaCO_3}=\dfrac{20}{25,6}\cdot100\%=78,125\%\)
\(\Rightarrow\%m_{CaO}=21,875\%\)
b) Theo 2 PTHH: \(\left\{{}\begin{matrix}n_{HCl\left(2\right)}=2n_{CaCO_3}=0,4mol\\n_{HCl\left(1\right)}=2n_{CaO}=2\cdot\dfrac{25,6-20}{56}=0,2mol\end{matrix}\right.\)
\(\Rightarrow\Sigma n_{HCl}=0,6mol\) \(\Rightarrow C\%_{HCl}=\dfrac{0,6\cdot36,5}{210\cdot1,05}\cdot100\%\approx9,93\%\)
Hòa tan hoàn toàn hỗn hợp X gồm Al và Mg trong 680ml dung dịch HNO3 1M thu được dung dịch Y và khí NO (sản phẩm khử duy nhất). Cho từ từ dung dịch NaOH vào dung dịch Y, lượng kết tủa tạo thành được biểu diễn theo đồ thị sau:
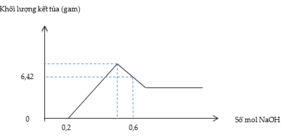
Phần trăm khối lượng của Al trong hỗn hợp đầu là?
A. 53,06%
B. 63,24%
C. 78,95%
D. 72,79%
Định hướng tư duy giải
Từ đồ thị ta thấy số mol HNO3 dư là 0,2 → H + n N O = 0 , 12 → n e = 0 , 36
Tại vị trí 0,6 mol, điền số
→ N a + : 0 , 6 N O 3 - : 0 , 56 → A l O 2 - : 0 , 04 → 6 , 42 M g ( O H ) 2 : a A l ( O H ) 3 : b - 0 , 04 → a = 0 , 03 b = 0 , 1 → % A l = 78 , 95 %
Hòa tan hoàn toàn hỗn hợp X gồm Al và Mg trong 680ml dung dịch HNO3 1M thu được dung dịch Y và khí NO (sản phẩm khử duy nhất). Cho từ từ dung dịch NaOH vào dung dịch Y, lượng kết tủa tạo thành được biểu diễn theo đồ thị sau:
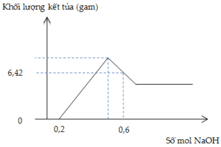
Phần trăm khối lượng của Al trong hỗn hợp đầu là?
A. 53,06%.
B. 63,24%.
C. 78,95%.
D. 72,79%.