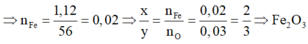Có 1 oxit sắt chưa rõ công thức . Chia lượng oxit này làm hai phần bằng nhau
a, Để hoà tan hết 1 phần phải dùng 150ml dung dịch HCL 3M
b, Cho 1luồng khí CO2 dư đi qua phần 2 nung nóng , phản ứng xong thu được 8,4g sắt . Tìm CT oxit sắt trên
Có một oxit sắt chưa rõ công thức, chia oxit này làm 2 phần bằng nhau.
a/ Để hoà tan hết phần 1 cần dùng150ml dung dịch HCl 1,5M.
b/ Cho luồng khí H2 dư đi qua phần 2 nung nóng, phản ứng xong thu được 4,2g sắt.
Tìm công thức của oxit sắt nói trên.
Có một oxit sắt chưa rõ công thức. Chia oxit này làm hai phần bằng nhau :
- Hòa tan hết phần 1 phải dùng 150 ml dung dịch HCl 3M
- Cho một luồng CO dư đi qua phần II nung nóng, phản ứng xong thu được 8,4g sắt
Tìm công thức oxit sắt trên.
nO(Oxit)=\(\dfrac{1}{2}n_{HCl}=\dfrac{1}{2}.0,15.3=0,225mol\)
\(n_{Fe}=\dfrac{8,4}{56}=0,15mol\)
-Gọi công thức là FexOy
-Ta có:
x:y=0,15:0,225=2:3\(\rightarrow\)Fe2O3
Có một oxit sắt A (hợp chất của sắt và oxi) chưa rõ công thức, chia oxit A này làm 2 phần
bằng nhau.
- Để hoà tan hết phần 1 cần dùng dung dịch chứa 8,2125 gam HCl tạo thành muối X và nước.
- Cho luồng khí H2 dư đi qua phần 2 nung nóng, phản ứng xong thu được 4,2g sắt và một lượng
nước.
a. Lập công thức hóa học của muối X, biết X là hợp chất của sắt và Cl. Viết PTHH.
b. Tìm công thức của oxit sắt nói trên, và khối lượng nước sinh ra sau phản ứng, thể tích khí hydro cần dùng.
Có 1 oxit sắt chưa rõ hóa trị của sắt. Chia lượng oxit này thành 2 phần bằng nhau:
- Hòa tan hết phần 1 phải dùng 150ml dd HCl 3M
- Cho luồng CO dư qua phần 2 nung nóng thu được 8,4g Fe
Tìm công thức của oxit sắt
Ct FexOy
FexOy + 2yHCl ====xFeCl2y/x + yH2O
a.............2ay
=> 2ay = 0,45 => ay = 0,225
FexOy + yCO ====xFe + yCO2
a.............................ax
=> ax = 8,4/56 = 0,15
=> ay/ax = 0,225/0,15 = 3 : 2
=> Ct sắt oxit là Fe2O3
có một oxit sắt chưa rõ công thứcchia oxit này làm 2 phần bằng nhau
a) để hòa tan hết phần 1 cần dùng 150ml dd HCl 1,5M
b) cho luồng khí H2 dư đi qua phần 2 nung nóng sâu phản ứng thu đc 4,2 g sắt tìm công thức oxit nói trên
Giúp mình nha mình sẽ tích cho 5 tick
FexOy+2yHCl->xFeCl2y/x+yH2O
nHCl=0.225(mol)
->nFexOy=0.225*1/2y=0.225/2y
FexOy+yH2->xFe+yH2O
nFe=0.075(mol)->nFe=0.075*1/x=0.075/x
Vì lượng oxit sắt ở hai pt bằng nhau
->số mol oxit sắt cũng bằng nhau
->\(\frac{0.225}{2y}=\frac{0.075}{x}\)
->0.225x=2y*0.075
0.225x=0.15y
->x/y=0.15:0.225=2/3
->công thức của oxit sắt đó là Fe2O3
Có 1 oxit sắt chưa rõ công thức. Chia 1 lượng oxit sắt này tahnhf 2 phần bằng nhau
- để htan hết P1 phải dùng dd chứa 0.45mol HCl
-Cho 1 luồng khí CO dư đi qua phần 2 nung nóng. Pư xong thu được 8,4g Fe. Tìm CTHH của oxit sắt
Gọi a, b là nồng độ mol ban đầu của H2SO4 và NaOH
ta có: 3b - 2a.2 = 0,5
3a.2 - 2b = 1
=> a = 0,4 ; b = 0,7
PTHH
OH(-) + H(+) ---> H2O
Chú ý: nH(+)=2nH2SO4
nOH(-)=nNaOH
Gọi công thức của oxit sắt là: FexOy
Chia làm 2 phần:
- P1:
FexOy+2yHCl→xFeCl2y/x+yH2O
- P2:
FexOy+yCO→xFe+yCO2
Ta có:
+) Ở P1: nHCl=0,45 (mol)
nFe=8,456=0,15 (mol)
⇒xy=2/3
Vậy công thức của oxit sắt là Fe2O3
có một oxit sắt chia lượn oxit này thành 2 phần bằng nhau .
a,để hòa tan hết phần 1 phải dùng 150ml dung dịch HCl 3M
b,cho luồng khí CO dư đi qua phần 2 nung nóng , phản ứng xong thu được 8,4 gam sắt.tìm công thức của oxit sắt trên
Đặt CTDC của oxit sắt: FexOy
Chia làm hai phần bằng nhau:
+ Phần 1:
\(Fe_xO_y\left(\dfrac{0,225}{y}\right)+2yHCl\left(0,45\right)--->xFeCl_{\dfrac{2y}{x}}+yH_2O\)\(\left(1\right)\)
\(n_{HCl}=3.0,15=0,45\left(mol\right)\)
\(Theo\left(1\right)\)\(n_{Fe_xO_y}=\dfrac{0,225}{y}\left(mol\right)\)
+ Phần 2:
\(yCO+Fe_xO_y\left(\dfrac{0,15}{x}\right)-t^o->xFe\left(0,15\right)+yCO_2\)\(\left(2\right)\)
\(n_{Fe}=0,15\left(mol\right)\)
Theo (2) \(n_{Fe_xO_y}=\dfrac{0,15}{x}\left(mol\right)\)
Ta có lượng oxit Fe trên được chia làm hai phần bằng nhau
\(\Rightarrow\dfrac{0,225}{y}=\dfrac{0,15}{x}\)
\(\Leftrightarrow\dfrac{x}{y}=\dfrac{0,15}{0,225}=\dfrac{2}{3}\)
\(\Rightarrow\)CT của oxit Sắt cần tìm là: \(Fe_2O_3\)
Có 1 oxit sắt chưa công thức. chia 2 phấn bằng nhau để Hòa tan hết phần 1 phải dùng 150 ml dd HCl 3M . Mặt khác, khử toàn bộ m gam oxit sắt bằng CO nóng, dư thu được 8,4 gam sắt. Công thức oxit sắt là j
giúp e nhanh vs ak
\(P2:\)
\(n_{Fe}=\dfrac{8.4}{56}=0.15\left(mol\right)\)
\(Fe_xO_y+yCO\underrightarrow{^{^{t^0}}}xFe+yCO_2\)
\(\dfrac{0.15}{x}..............0.15\)
\(P1:\)
\(n_{HCl}=0.15\cdot3=0.45\left(mol\right)\)
\(Fe_xO_y+2yHCl\rightarrow xFeCl_{\dfrac{2y}{x}}+yH_2\)
\(\dfrac{0.225}{y}.......0.45\)
\(\Rightarrow\dfrac{0.15}{x}=\dfrac{0.225}{y}\)
\(\Leftrightarrow\dfrac{x}{y}=\dfrac{0.15}{0.225}=\dfrac{2}{3}\)
\(CT:Fe_2O_3\)
Tại mới lớp 8 nên anh giải hơi chi tiết á :))
Phần 1 :
n HCl= 0,15.3 = 0,45(mol)
=> n O(oxit) = 1/2 n HCl = 0,225(mol)
n Fe = 8,4/56 = 0,15(mol)
Ta có :
n Fe / n O = 0,15/0,225 = 2/3
Vậy oxit là Fe2O3
Gọi CT oxit sắt là \(Fe_xO_y\)
PTHH: \(Fe_xO_y+2yHCl\rightarrow xFeCl_{\dfrac{2y}{x}}+yH_2O\left(1\right)\\ Fe_xO_y+yCO\rightarrow xFe+yCO_2\left(2\right)\)
\(n_{HCl}=0,15.3=0,45\left(mol\right)\)
\(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\)
\(\left(1\right)\Rightarrow n_{\text{O trong }Fe_xO_y}=n_{\text{O trong }H_2O}=n_{H_2O}=\dfrac{1}{2}n_{HCl}=\dfrac{1}{2}.0,45=0,225\left(mol\right)\)
\(\left(2\right)\Rightarrow n_{Fe trong Fe_xO_y}=n_{Fe}=0,15\left(mol\right)\)
\(x:y=0,15:0,225=2:3\)
Vậy CT oxit sắt là \(Fe_2O_3\)
Một hỗn hợp gồm Al và một oxit sắt, chia thành 2 phần bằng nhau.
- Để hoà tan hết phần 1 cần 200ml dung dịch HCl 0,675M, thu được 0,84 lít H2 (đktc).
- Nung phần 2, phản ứng hoàn toàn, lấy sản phẩm tác dụng với NaOH dư thấy còn l,12g rắn không tan.
Công thức của oxit sắt là:
A. Fe2O3
B. FeO
C. Fe3O4
D. Không xác định
Đáp án A
Phần 1: Hỗn hợp tác dụng với HC1 gồm Al và FexOy
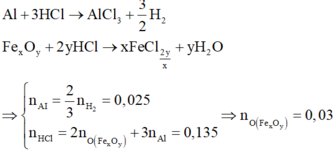
Phần 2: Có thể coi quá trình nhiệt nhôm với phản ứng xảy ra hoàn toàn như sau:

Vì phản ứng xảy ra hoàn toàn nên hỗn hợp sau phản ứng gồm Fe, A12O3 và Al dư. Khi cho hỗn hợp này vào dung dịch NaOH dư thì chất rắn còn lại là Fe.