trong phòng thí nghiệm để điều chế được 5,6 l O2( đktc) thì cần dùng bao nhiêu g kali clorat. Biết khí O2 thu được sau pư bị hao hụt 10%

Những câu hỏi liên quan
[Tự Luận] Trong phòng thí nghiệm để điều chế được 5,6 lít khí O2 (đktc) cần phải dùng bao nhiêu gam Kali Clorat?
\(2KClO_3\xrightarrow[]{t^o}2KCl+3O_2\)
\(n_{O_2}=\dfrac{V_{O_2}}{22,4}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Theo PTHH: \(n_{KClO_3}=\dfrac{0,25.2}{3}\approx0,17\left(mol\right)\)
Vậy muốn điều chế 5,6 lít O2 cần dùng số gam Kali clorat:
\(m_{KClO_3}=n_{KClO_3}.M_{KClO_3}=0,17.122,5=20,825g\)
Đúng 2
Bình luận (1)
\(n_{O2}\)=\(\dfrac{V}{22,4}\)=\(\dfrac{5,6}{22,4}\)=0,25 (mol)
PT : 2KClO3 →to 2KCl + 3O2
số mol: \(\dfrac{1}{6}\) ← \(\dfrac{1}{6}\) ← 0,25
⇒ mKClO3 = n . M = \(\dfrac{1}{6}\) . 122,5 ∼∼ 20,41(g)
Đúng 0
Bình luận (1)
Trong phòng thí nghiệm để điều chế được 5,6 lít khí O2 (đktc) cần phải dùng bao nhiêu gram Kali Clorat vậy mọi ng
\(n_{O_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PT: \(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
Theo PT: \(n_{KClO_3}=\dfrac{2}{3}n_{O_2}=\dfrac{1}{6}\left(mol\right)\Rightarrow m_{KClO_3}=\dfrac{1}{6}.122,5=\dfrac{245}{12}\left(g\right)\)
Đúng 2
Bình luận (0)
| Hóa học 8 - Thanks for your helpingg!!!!!!!!!!!!!~ |
Trong phòng thí nghiệm, người ta nhiệt phân Kali clorat KClO3 thu được Kaliclorua và khí Oxi
a. Muốn điều chế được 6,72 lít khí O2 ở đktc cần dùng bao nhiêu g KClO3?
b. Nếu có 490g KClO3 tham gia phản ứng sẽ thu được bao nhiêu g chất rắn và chất khí?
a) \(n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2KClO3 --to--> 2KCl + 3O2
0,2<-------------------0,3
=> \(m_{KClO_3}=0,2.122,5=24,5\left(g\right)\)
b) \(n_{KClO_3}=\dfrac{490}{122,5}=4\left(mol\right)\)
PTHH: 2KClO3 --to--> 2KCl + 3O2
4-------------->4---->6
=> \(m_{KCl}=4.74,5=298\left(g\right)\)
=> \(m_{O_2}=6.32=192\left(g\right)\)
Đúng 2
Bình luận (0)
2KClO3 \(\underrightarrow{t^o}\) 2KCl + 3O2
a, \(n_{O_2}=\dfrac{6,72}{22,4}=0,3mol\\ n_{KClO_3}=\dfrac{0,3.2}{3}=0,2mol\\ m_{KClO_3}=0,2.122,5=24,5g\)
b, \(n_{KClO_3}=\dfrac{490}{122,5}=4mol\)
\(\Rightarrow m_{KCl}=4.74,5=298g\)
\(n_{O_2}=\dfrac{4.3}{2}=6mol\\ m_{O_2}=6.32=192g\)
Đúng 0
Bình luận (0)
Phân hủy 24,5 gam Kali clorat. tính thể tích CO2 thu được (đkc) .Tính khối lượng KMnO4 được dùng để thu 2,24 lít CO2(đkc) biết lượng hao hụt khí thu được và 10% .Tính khối lượng Fe và thể tích O2 cần để điều chế 3,48 g Fe304 .Để có lượng O2 trên cần phân hủy bao nhiêu gam KClO3?
a)
\(n_{KClO_3}=\dfrac{24.5}{122.5}=0.2\left(mol\right)\)
\(2KClO_3\underrightarrow{^{^{t^0}}}2KCl+3O_2\)
\(n_{O_2}=\dfrac{3}{2}\cdot0.2=0.3\left(mol\right)\)
\(V_{O_2}=0.3\cdot22.4=6.72\left(l\right)\)
Đúng 4
Bình luận (0)
\(n_{O_2}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(2KMnO_4\underrightarrow{^{^{t^0}}}K_2MnO_4+MnO_2+O_2\)
\(0.2...............................................0.1\)
\(n_{KMnO_4\left(bđ\right)}=\dfrac{0.2}{90\%}=\dfrac{2}{9}\left(mol\right)\)
\(m_{KMnO_4}=\dfrac{2}{9}\cdot158=35.11\left(g\right)\)
Đúng 3
Bình luận (0)
\(n_{Fe_3O_4}=\dfrac{3.48}{232}=0.015\left(mol\right)\)
\(3Fe+2O_2\underrightarrow{^{^{t^0}}}Fe_3O_4\)
\(0.045....0.03......0.015\)
\(m_{Fe}=0.045\cdot56=2.52\left(g\right)\)
\(V_{O_2}=0.03\cdot22.4=0.672\left(l\right)\)
\(2KClO_3\underrightarrow{^{^{t^0}}}2KCl+3O_2\)
\(0.02......................0.03\)
\(m_{KClO_3}=0.02\cdot122.5=2.45\left(g\right)\)
Đúng 3
Bình luận (0)
Để chuẩn bị cho buổi thí nghiệm thực hành của lớp cần thu 20 lọ khí oxi, mỗi lọ có dung tích 100ml. a) Tính khối lượng kali pemanganat phải dùng, giả sử khí oxi thu được ở điều kiện tiêu chuẩn và hao hụt 10%? b) Nếu dùng kali clorat có thêm một lượng nhỏ MnO2 thì lượng kali clorat cần dùng là bao nhiêu? Viết phương trình phản ứng và chỉ rõ điều kiện phản ứng.
Đọc tiếp
Để chuẩn bị cho buổi thí nghiệm thực hành của lớp cần thu 20 lọ khí oxi, mỗi lọ có dung tích 100ml.
a) Tính khối lượng kali pemanganat phải dùng, giả sử khí oxi thu được ở điều kiện tiêu chuẩn và hao hụt 10%?
b) Nếu dùng kali clorat có thêm một lượng nhỏ MnO2 thì lượng kali clorat cần dùng là bao nhiêu? Viết phương trình phản ứng và chỉ rõ điều kiện phản ứng.
a) Do khí oxi thu được hao hụt 10% nên hiệu suất phản ứng là 90%.
Thể tích khí oxi thu được là:
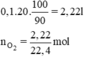
Phương trình hóa học của phản ứng nhiệt phân KMnO4:
2KMnO4 -to→ O2 + K2MnO4 + MnO2.
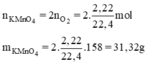
b) Ý b) tách biệt so với ý a), ngoài ra ở ý b) không cho lượng oxi hao hụt là bao nhiêu nên ta lấy hiệu suất phản ứng đạt 100%.
Thể tích khí oxi thu được là: V = 0,1.20 = 2 (lít)

Đúng 0
Bình luận (0)
Để chuẩn bị cho buổi thí nghiệm thực hành cần 20 lọ khí oxi, mỗi lọ có dung tích 100ml.
a) Tính khối lượng kali pemangarat phải dùng, giả sử khí oxi thu được ở điều kiện tiêu chuẩn và bị hao hụt 10%.
b) Nếu dùng kali clorat có thêm lượng nhỏ MnO2 thì lượng kali clorat cần dùng là bao nhiêu ? Viết phương trình hóa học và chỉ rõ điều kiện phản ứng.
a) \(V_{O_2\left(thu.được\right)}=20.0,1=2\left(l\right)\)
=> \(V_{O_2\left(sinh.ra\right)}=\dfrac{2.100}{90}=\dfrac{20}{9}\left(l\right)\)
=> \(n_{O_2\left(sinh.ra\right)}=\dfrac{\dfrac{20}{9}}{22,4}=\dfrac{25}{252}\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
\(\dfrac{25}{126}\)<----------------------------\(\dfrac{25}{252}\)
=> \(m_{KMnO_4}=\dfrac{25}{126}.158=\dfrac{1975}{63}\left(g\right)\)
b)
PTHH: 2KClO3 --to,MnO2--> 2KCl + 3O2
\(\dfrac{25}{378}\)<---------------------\(\dfrac{25}{252}\)
=> \(m_{KClO_3}=\dfrac{25}{378}.122,5=\dfrac{875}{108}\left(g\right)\)
Đúng 2
Bình luận (0)
Để chuẩn bị cho buổi thí nghiệm thực hành của lớp cần thu 20 lọ khí oxi, mỗi lọ có dung tích 100ml. a) Tính khối lượng kali pemanganat phải dùng, giả sử khí oxi thu được ở điều kiện tiêu chuẩn và hao hụt 10%? b) Nếu dùng kali clorat có thêm một lượng nhỏ MnO2 thì lượng kali clorat cần dùng là bao nhiêu? Viết phương trình phản ứng và chỉ rõ điều kiện phản ứng. giải cụ thể bài này hộ mình nha
Đọc tiếp
Để chuẩn bị cho buổi thí nghiệm thực hành của lớp cần thu 20 lọ khí oxi, mỗi lọ có dung tích 100ml. a) Tính khối lượng kali pemanganat phải dùng, giả sử khí oxi thu được ở điều kiện tiêu chuẩn và hao hụt 10%? b) Nếu dùng kali clorat có thêm một lượng nhỏ MnO2 thì lượng kali clorat cần dùng là bao nhiêu? Viết phương trình phản ứng và chỉ rõ điều kiện phản ứng.
giải cụ thể bài này hộ mình nha
a, Thể tích khí oxi cần thu là: 20*100 = 2000(ml) = 2(l).
Vì hao hụt 10% nên thể tích khí oxi cần có là: 100*2/90 = 20/9 (l).
Số mol khí oxi là: 20/(22,4*9) = 0,099 (mol)
2KMnO4 => K2MnO4 + MnO2 + O2
Số mol KMnO4 là: 0,099 * 2 = 0,2 (mol)
Khối lượng KMnO4 là: 0,2*158 = 31,3 (g)
b, 2KClO3 => 2KCl + 3O2
Số mol KClO3 là: 0,099*2/3 = 0,066 (mol).
Khối lượng cần dùng là: 0,066*122,5 = 8,085 (g)
2 PTPU trên đều có nhiệt độ
Đúng 0
Bình luận (0)
ae làm cụ thể nhá , đừng search mạng , mình search rồi =.=
Đúng 0
Bình luận (0)
a, Thể tích khí oxi cần thu là: 20*100 = 2000(ml) = 2(l).
Vì hao hụt 10% nên thể tích khí oxi cần có là: 100*2/90 = 20/9 (l).
Số mol khí oxi là: 20/(22,4*9) = 0,099 (mol)
2KMnO4 => K2MnO4 + MnO2 + O2
Số mol KMnO4 là: 0,099 * 2 = 0,2 (mol)
Khối lượng KMnO4 là: 0,2*158 = 31,3 (g)
b, 2KClO3 => 2KCl + 3O2
Số mol KClO3 là: 0,099*2/3 = 0,066 (mol).
Khối lượng cần dùng là: 0,066*122,5 = 8,085 (g)
2 PTPU trên đều có nhiệt độ
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Để điều chế oxi trong phòng thí nghiệm người ta phân hủy kali clorat (KClO3) thu được kali clorua (KCl ) và khí oxi (O2).a. Tính thể tích khí oxi (đktc) thu được khi phân hủy 12,25 gam KClO3.b. Tính thể tích không khí chứa lượng oxi trên biết rằng c. Dùng toàn bộ lượng oxi trên cho tác dụng với 28 gam sắt. Sau phản ứng chất nào còn dư ? (Cho biết:K 39; Cl 35,5 ; O 16; Fe 56) Bài làm:
Đọc tiếp
Để điều chế oxi trong phòng thí nghiệm người ta phân hủy kali clorat (KClO3) thu được kali clorua (KCl ) và khí oxi (O2).
a. Tính thể tích khí oxi (đktc) thu được khi phân hủy 12,25 gam KClO3.
b. Tính thể tích không khí chứa lượng oxi trên biết rằng ![]() =
= ![]()
c. Dùng toàn bộ lượng oxi trên cho tác dụng với 28 gam sắt. Sau phản ứng chất nào còn dư ?
(Cho biết:K = 39; Cl = 35,5 ; O = 16; Fe = 56)
Bài làm:
a.\(n_{KClO_3}=\dfrac{m_{KClO_3}}{M_{KClO_3}}=\dfrac{12,25}{122,5}=0,1mol\)
\(2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\)
2 2 3 ( mol )
0,1 0,15
\(V_{O_2}=n_{O_2}.22,4=0,15.22,4=3,36l\)
b.\(V_{kk}=V_{O_2}.5=3,36.5=16,8l\)
c.\(n_{Fe}=\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{28}{56}=0,5mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
3 2 1 ( mol )
0,5 > 0,15 ( mol )
0,225 0,15 ( mol )
\(m_{Fe\left(du\right)}=n_{Fe\left(du\right)}.M_{Fe}=\left(0,5-0,225\right).56=15,4g\)
Đúng 1
Bình luận (0)


























