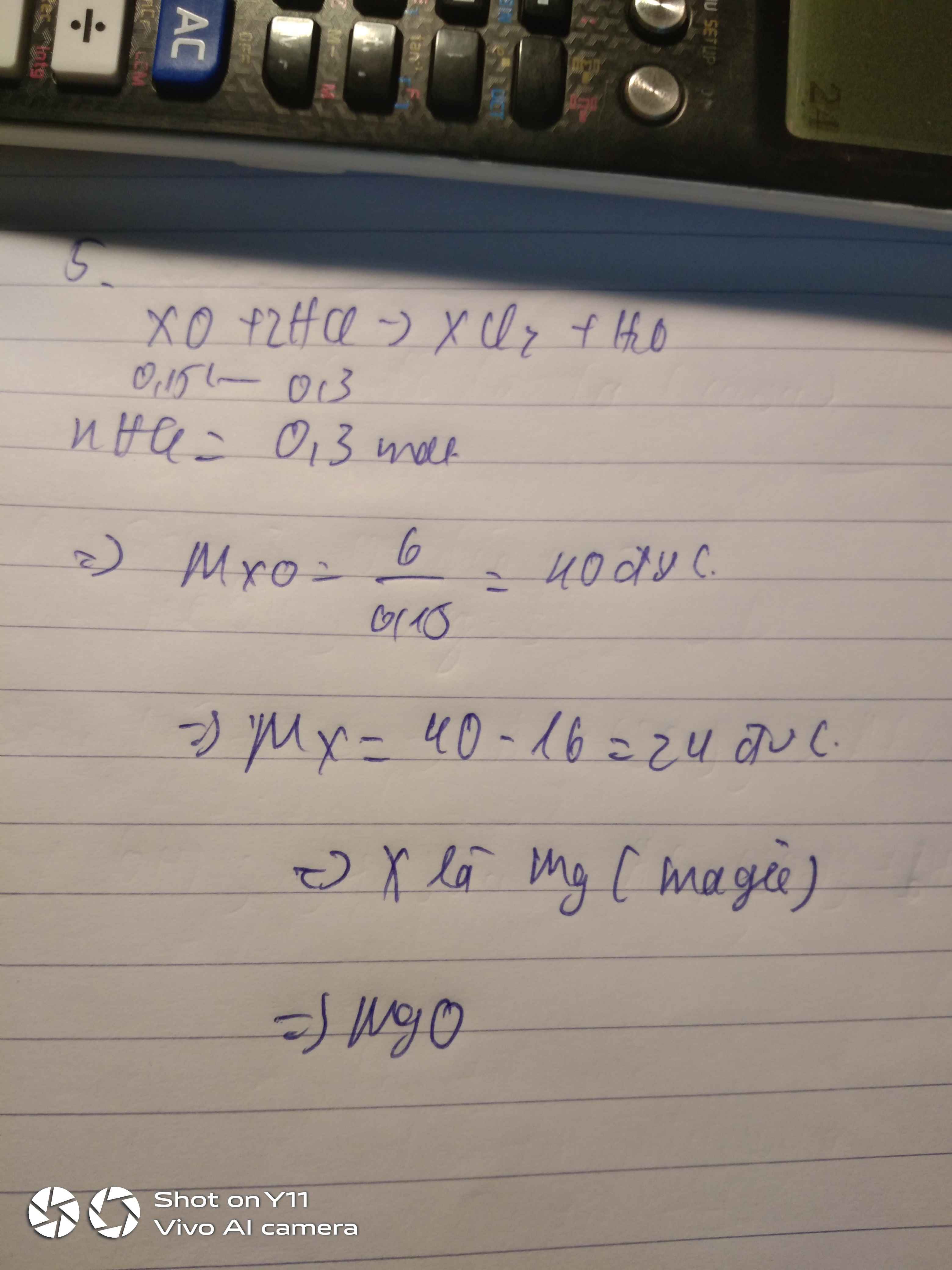biết rằng 300 ml dung dịch axit sunfuric 1M đủ để hòa tan hết 5,1 g oxit của một kim loại hóa trị 3. xác định kim loại và oxit tương ứng

Những câu hỏi liên quan
Hòa tan 22,7g hỗn hợp gồm kim loại kiềm A và oxit của nó tan hết vào nước thu được dung dịch B, trung hòa hết 1/5 dung dịch B bằng 50 ml dung dịch axit sunfuric 1M (vừa đủ). Hãy xác định kim loại A?
ct A va AO
A+2H2O \(\rightarrow\) A(OH)2 +H2x xAO+H2O\(\rightarrow\)A(OH)2y ynH2SO4=0.05*1=0.05molA(OH)2 +2HCL\(\rightarrow\)ACl2 +2H2O 0.125 0.25trung hoà 1/5 dd B cần 0.125 mol H2SO4=> 5 phan dd B cần 0.625 mol H2SO4=>x+y=0.625mhh=xA+y(A+16)=Ax+Ay+16y=22.7 \(\Leftrightarrow\)A(x+y)+16y=22.7 \(\Leftrightarrow\) 0.625A+16y=22.7 \(\Rightarrow\)y=(22.7-0.625A)/16ta có 0y<0.625 mà y là số dương\(\Rightarrow\)0\(\Leftrightarrow\) 0<(22.7-0.625A)/16<0.625giải ra
Đúng 0
Bình luận (0)
Hòa tan hết 10,2 gam oxit bazo (của kim loại hóa trị III) cần dùng 300 ml dung dịch H2SO4 1M. Xác định công thức của oxit bazo?
Ta có: \(n_{H_2SO_4}=0,3.1=0,3\left(mol\right)\)
Gọi CTHH của oxit bazo đó là A2O3.
PT: \(A_2O_3+3H_2SO_4\rightarrow A_2\left(SO_4\right)_3+3H_2O\)
Theo PT: \(n_{A_2O_3}=\dfrac{1}{3}n_{H_2SO_4}=0,1\left(mol\right)\)
\(\Rightarrow M_{A_2O_3}=\dfrac{10,2}{0,1}=102\left(g/mol\right)\)
⇒ 2MA + 16.3 = 102 ⇒ MA = 27 (g/mol)
→ A là Al.
Vậy: CTHH cần tìm là Al2O3.
Đúng 2
Bình luận (0)
Hãy xác định công thức của một oxit kim loại có hóa trị 3 biết rằng hòa tan 8 g oxit này bằng 300mlH2SO4 loãng 1M, sau Phản ứng phải trung hòa lượng axit còn dư bằng 50 gam dung dịch NaOH 2 4%
Xem chi tiết
\(H_2SO_4 + 2NaOH \to Na_2SO_4 + 2H_2O\\ n_{H_2SO_4\ dư} = \dfrac{1}{2}n_{NaOH} = \dfrac{1}{2}.\dfrac{50.24\%}{40} = 0,15(mol)\\ \Rightarrow n_{H_2SO_4\ pư} = 0,3 - 0,15 = 0,15(mol)\)
Oxit kim loại hóa trị III : R2O3
\(R_2O_3 + 3H_2SO_4 \to R_2(SO_4)_3 + 3H_2O\\ n_{Oxit} = \dfrac{1}{3}n_{H_2SO_4} = 0,05(mol)\\ \Rightarrow M_{oxit} = 2R + 16.3 = \dfrac{8}{0,05} = 160\\ \Rightarrow R = 56(Fe)\)
Vậy oxit cần tìm : Fe2O3
Đúng 5
Bình luận (0)
5. Hòa tan 6 gam oxit kim loại hóa trị II cần 300 ml dung dịch HCl 1M. Xác định CTHH của oxit
biết rằng 300ml dung dịch Hcl 1M vừa đủ hoà tan hết 5.1g một oxit của kim loại M chưa rõ hoá trị hãy xác định tên kim loại và và công thức oxit
Xem chi tiết
Bạn tham khảo lời giải ở đây nhé!
biết rằng 300ml dung dịch Hcl 1M vừa đủ hoà tan hết 5.1g một oxit của kim loại M chưa rõ hoá trị hãy xác định tên kim loại và và công thức oxit - Hoc24
Đúng 1
Bình luận (0)
Biết rằng 300 ml dung dịch HCl 1M đủ để hòa tan 5,1g oxit của kim loại R hóa trị III. Xác định kim loại R.
https://i.imgur.com/v1S1Xuo.jpg
Bài 7: Hỗn hợp gồm một kim loại kiềm (hóa trị I) và oxit của nó có khối lượng 19,3 gam tan hết trong nước thoát ra 3,36 lít H2 (đktc) và thu được một dung dịch kiềm. Để trung hòa dung dịch kiềm này cần dùng hết 350 ml H2SO4 1M. Xác định kim loại kiềm.Bài 8: Một hỗn hợp gồm Zn và Fe có khối lượng là 30,7 gam. Hòa tan hỗn hợp này trong 400 ml dung dịch H2SO4 2M.a/ Chứng tỏ rằng hỗn hợp này tan hết.b/ Nếu dùng một lượng hỗn hợp Zn và Fe gấp đôi trường hợp trước, lượ...
Đọc tiếp
Bài 7: Hỗn hợp gồm một kim loại kiềm (hóa trị I) và oxit của nó có khối lượng 19,3 gam tan hết trong nước thoát ra 3,36 lít H2 (đktc) và thu được một dung dịch kiềm. Để trung hòa dung dịch kiềm này cần dùng hết 350 ml H2SO4 1M. Xác định kim loại kiềm.
Bài 8: Một hỗn hợp gồm Zn và Fe có khối lượng là 30,7 gam. Hòa tan hỗn hợp này trong 400 ml dung dịch H2SO4 2M.
a/ Chứng tỏ rằng hỗn hợp này tan hết.
b/ Nếu dùng một lượng hỗn hợp Zn và Fe gấp đôi trường hợp trước, lượng H2SO4 vẫn như cũ thì hỗn hợp mới này có tan hết hay không?
c/ Trong trường hợp (a), hãy tính khối lượng mỗi kim loại trong hỗn hợp biết rằng khi đốt cháy lượng H2 sinh ra trong phản ứng, thì thu được 8,1 gam nước (lượng nước bị hao hụt 10%).
Bài 1.Để hòa tan hoàn toàn 8 g oxit kim loại m chưa rõ hóa trị cần dùng 200 ml dung dịch HCl 1,5 m xác định công thức hóa học của oxit kim loại
Gọi CTHH của oxit là \(R_xO_y\left(x,y\in N\text{*},\text{2y/x là hoá trị của kim loại R}\right)\)
\(n_{HCl}=1,5.0,2=0,3\left(mol\right)\)
PTHH: \(R_xO_y+2yHCl\rightarrow xRCl_{2y\text{/}x}+yH_2O\)
\(\dfrac{0,15}{y}\)<--0,3
\(\rightarrow n_R=xn_{R_xO_y}=x.\dfrac{0,15}{y}=\dfrac{0,15x}{y}\left(mol\right)\)
Theo PTHH: \(n_O=\dfrac{1}{2}n_{HCl}=\dfrac{1}{2}.0,3=0,15\left(mol\right)\)
\(\xrightarrow[]{\text{BTNT}}m_R=8-0,15.16=5,6\left(g\right)\)
\(\rightarrow M_R=\dfrac{5,6}{\dfrac{0,15x}{y}}=\dfrac{112y}{3x}=\dfrac{56}{3}.\dfrac{2y}{x}\left(g\text{/}mol\right)\)
Vì 2y/x là hoá trị R nên ta có:
| \(\dfrac{2y}{x}\) | 1 | 2 | 3 | \(\dfrac{8}{3}\) |
| \(\dfrac{56}{3}\) | \(\dfrac{112}{3}\) | 56 | \(\dfrac{896}{9}\) | |
| Loại | Loại | Sắt (Fe) | Loại |
=> R là Fe
\(\rightarrow\dfrac{2y}{x}=3\Leftrightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
Do \(x,y\in N\text{*}\rightarrow\left\{{}\begin{matrix}x=2\\y=3\end{matrix}\right.\)
Vậy CTHH của oxit là \(Fe_2O_3\)
Đúng 5
Bình luận (0)
Hòa tan hoàn toàn 9,4 gam một oxit kim loại M (hóa trị n) cần dùng vừa đủ 100ml dung dịch H2SO4 1M. Xác định M và CTHH của oxit.
\(n_{H_2SO_4} = 0,1(mol)\\ M_2O_n + nH_2SO_4 \to M_2(SO_4)_n + nH_2O\\ n_{M_2O_n} = \dfrac{1}{n}n_{H_2SO_4} = \dfrac{0,1}{n}(mol)\\ \Rightarrow \dfrac{0,1}{n}(2M + 16n) = 9,4\\ \Rightarrow M = 39n\)
Với n = 1 thì M = 39(Kali)
CTHH của oxit : K2O
Đúng 3
Bình luận (0)