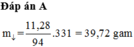cho 9,4 g phenol td vs Br dư . tính lhoois lượng kết tủa thu được

Những câu hỏi liên quan
cho m (g) hh ancol etynic và phenol td vs Na dư thu đc 2,24 (L) H\(_2\) ở đktc . cũng m (g) hh trên cho td vs Br dư thu đc 33,1 g kết tủa trắng viết các pt phản ứng xảy ra và tính m
chia m gam hh x gồm khco3 và nahco3 thành 2 phần. phần 1 cho tác dụng với lượng dư bacl2 thu được 19,7 g kết tủa. phần 2 td với ca(oh)2 dư, thu được 30 g kết tủa. tính giá trị m
- Phần 1:
PT: \(Na_2CO_3+BaCl_2\rightarrow2NaCl+BaCO_{3\downarrow}\)
Ta có: \(n_{BaCO_3}=\dfrac{19,7}{197}=0,1\left(mol\right)\)
Theo PT: \(n_{Na_2CO_3}=n_{BaCO_3}=0,1\left(mol\right)\)
- Phần 2:
Ta có: \(n_{CaCO_3}=\dfrac{30}{100}=0,3\left(mol\right)\)
PT: \(KHCO_3+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+KOH+H_2O\)
\(Na_2CO_3+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+2NaOH\)
Theo PT: \(n_{CaCO_3}=n_{KHCO_3}+n_{Na_2CO_3}\)
\(\Rightarrow0,3=n_{KHCO_3}+0,1\Rightarrow n_{KHCO_3}=0,2\left(mol\right)\)
⇒ X gồm: 0,4 (mol) KHCO3 và 0,2 (mol) Na2CO3
⇒ m = 0,4.100 + 0,2.106 = 61,2 (g)
Đúng 3
Bình luận (0)
Bạn xem lại đề nhé, cả KHCO3 và NaHCO3 đều không có pư với BaCl2 đâu.
Đúng 0
Bình luận (3)
Câu 1: Cho m gam phenol tác dụng với natri dư thấy thoát ra 0.56 lít khí H2 (đktc) Tính khối lượng phenol cần dùng. Câu 2: Chi 4,7 gam phenol tác dụng với nước brom dư, thu được m gam kết tủa Tính m
Câu 1:
\(n_{H_2}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\)
PTHH: \(2C_6H_5OH+2Na\underrightarrow{t^o}2C_6H_5ONa+H_2\)
0,05<--------------------------0,025
=> m = 0,05.94 = 4,7 (g)
Câu 2:
\(n_{C_6H_5OH}=\dfrac{4,7}{94}=0,05\left(mol\right)\)
PTHH: \(C_6H_5OH+3Br_2\rightarrow C_6H_2Br_3OH\downarrow+3HBr\)
0,05--------------->0,05
=> m = 0,05.331 = 16,55 (g)
Đúng 4
Bình luận (0)
Cho 11,28 gam phenol tác dụng hết với nước brom dư, khối lượng kết tủa 2,4,6-tribromphenol thu được là
A. 39,72.
B. 30,24.
C. 30,48.
D. 20,08.
Cho 4,7 gam phenol phản ứng với V ml dung dịch Br2 3% (D=1,3 gam/ml) dư thu được a gam kết tủa trắng. Tính a và V (biết lượng brom dư 10% so với lượng Brom phản ứng)
Có một dd chuaa đồng thời 2 muối là CuCl2 và MgCl2.Chia 50g dd làm 2 phần bằng nhau:
- Phần 1: cho phản ứng với lượng dư dd AgNO3 thu được 14,35 g kết tủa
- Phần 2: cho phản ứng vs lượng dư dd NaOH.Lọc lấy kết tủa,rửa sạch rồi nung ở nhiệt độ cao thu được 3,2g hỗn hợp chất rắn
Tính khối lượng của mỗi muối trong hỗn hợp.
Khối lượng dd mỗi phần=50/2= 25g
Gọi số mol của MgCl2 và CuCl2 trong 25g dung dịch lần lượt là x và y Phần 1:
MgCl2 +2AgNO3 -------> 2AgCl + Mg(NO3)2
x ............................................2x
CuCl2 + 2AgNO3 ------> 2AgCl + Cu(NO3)2
y............................................ 2y
nAgCl = 14,35/143,5 = 0,1 mol
Ta có pt: 2x+2y = 0,1 (I)
Phần 2:
MgCl2 + 2NaOH -------> Mg(OH)2 + 2NaCl
x .............................................x
CuCl2 + 2NaOH ---------> Cu(OH)2 + 2NaCl
y............................................... y
Mg(OH)2 -----------> MgO + H2O
x.................................... x
Cu(OH)2 ------------> CuO + H2O
y................................... y
Số gam chất rắn = tổng số gam MgO và CuO
Từ pt (3,4,5,6) ta có: 40x + 80y = 3,2 (II)
Giải hệ (I) và(II) ta được x = 0,02 ; y = 0,03
Suy ra: mMgCl2 = 0,02. 95 = 1,9 g
số gam CuCl2 = 0,03. 135 = 4,05 g
%m MgCl2 là: 1,9.100/25 = 7,6%
%m CuCl2 là: 4,05.100/25 = 16,2%
Có thể viết pt ion rút gọn để giải nhanh hơn
Đúng 0
Bình luận (2)
cho hỗn hợp x gồm phenol và ancol etylic tâc dụng với k dư thu được 13,44 lí khí(đktc)cũng hỗn hợp trên tâc dụng với dd br2 dư thu được 33,1 gam kết tủa trắng A)viết các phương trình phản ứng B) tính khối lượng hỗn hợp X
a, \(C_6H_5OH+K\rightarrow C_6H_5OK+\dfrac{1}{2}H_2\)
\(C_2H_5OH+K\rightarrow C_2H_5OK+\dfrac{1}{2}H_2\)
\(C_6H_5OH+3Br_2\rightarrow C_6H_2Br_3\left(OH\right)+3HBr\)
b, \(n_{C_6H_2Br_3\left(OH\right)}=\dfrac{33,1}{331}=0,1\left(mol\right)\)
Theo PT: \(n_{C_6H_5OH}=n_{C_6H_2Br_3\left(OH\right)}=0,1\left(mol\right)\)
Mà: \(n_{H_2}=\dfrac{1}{2}n_{C_6H_5OH}+\dfrac{1}{2}n_{C_2H_5OH}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
\(\Rightarrow n_{C_2H_5OH}=1,1\left(mol\right)\)
\(\Rightarrow m_X=0,1.94+1.1.46=60\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 6,08g hhX (Al2O3 và MgO) vào 85ml dd HCl 4M lấy vừa đủ,cho pứ xong thu đc ddY
a. Tính thành pần khối lượng hhX
b. Cho ddY td vs dd KOH dư thì sau pứ thu đc mấy gam kết tủa
Hòa tan hoàn toàn 7,8g hh Mg, Al vào HCl dư thu được 8,96l H2 và dd A
a) Tính %m mỗi kim loại
b) Cho dd A td với NaOH dư thu đc m(g) kết tủa. Tính m
Đặt nMg=a(mol); nAl=b(mol)
PTHH: Mg +2 HCl -> MgCl2 + H2
a________2a_______a_____a(mol)
2 Al + 6 HCl -> 2 AlCl3 +3 H2
b_____3b____b_____1,5b(mol)
Ta có hpt: \(\left\{{}\begin{matrix}24a+27b=7,8\\a+1,5b=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,2\end{matrix}\right.\)
=> %mMg=[(0,1.24)/7,8].100=30,769%
=>%mAl= 69,231%
c) MgCl2 + 2 NaOH -> Mg(OH)2 + 2 NaCl
0,1_______________0,1(mol)
AlCl3 + 3 NaOH -> Al(OH)3 + 3 NaCl
0,2____________0,2(mol)
=> m=m(kết tủa)= mMg(OH)2+ mAl(OH)3= 58.0,1+ 78.0,2= 21,4(g)
Đúng 1
Bình luận (0)