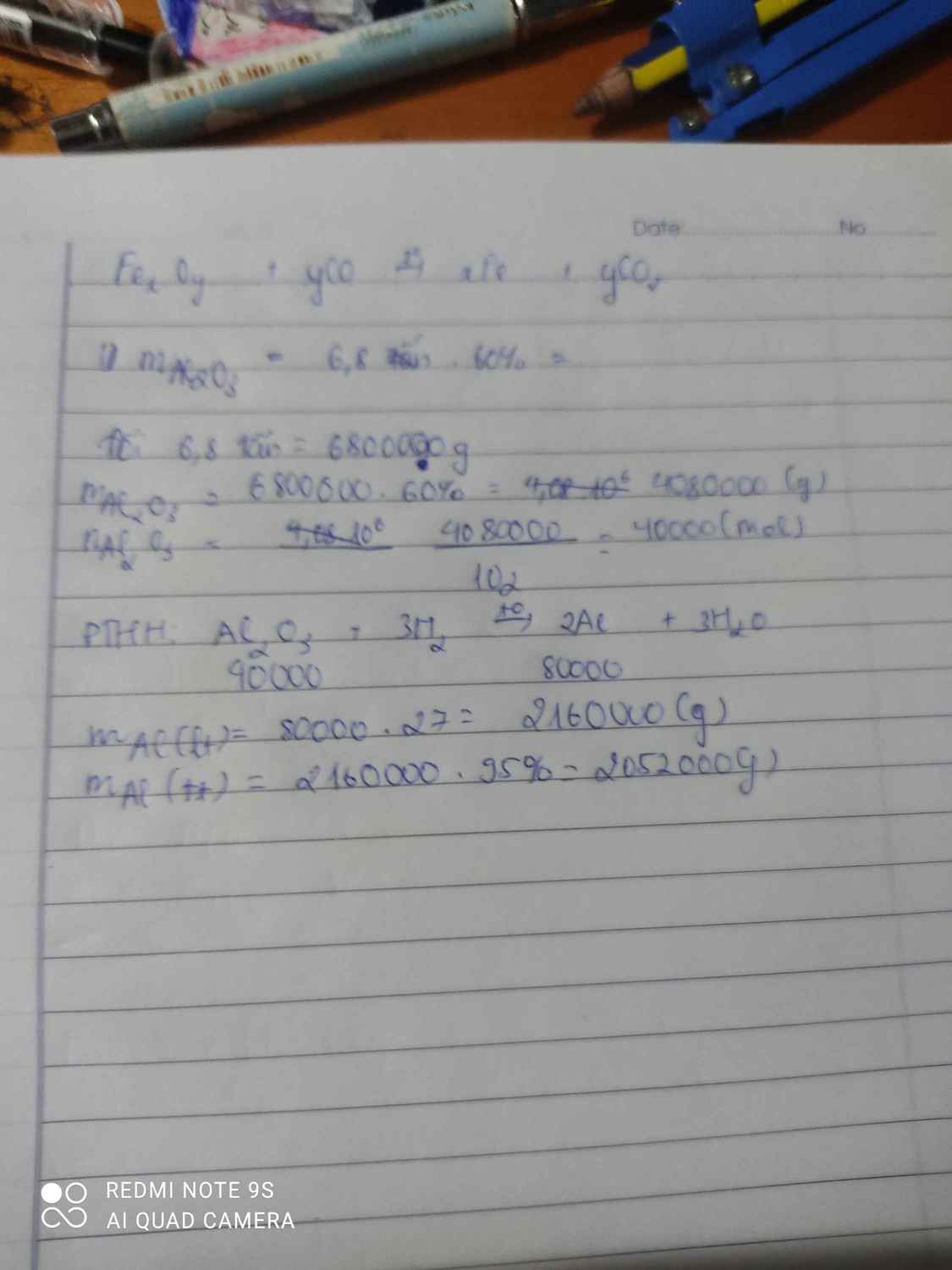Từ 1 tấn quặng boxit ( có chứa 81,6% Al2O3 còn lại là tạp chất ko chứa Al hỏi người ta sản xuất được bao nhiêu tấn Al

Những câu hỏi liên quan
người ta dùng quặng boxit để sản xuất al. hàm lượng al2o3 trong quặng là 40%. để có được 4 tấn nhôm nguyên chất thì cần bao nhiêu tấn quặng?
Người ta dùng quặng boxit để sản xuất Al. Hàm lượng Al 2 O 3 trong quặng là 40%. Để có được 4 tấn nhôm nguyên chất cần bao nhiêu tấn quặng ? Biết rằng hiệu suất của quá trình sản xuất là 90%.
Thực tế do một số nguyên nhân, chất tham gia phản ứng không tác dụng hết, nghĩa là hiệu suất dưới 100%. Người ta có thể tính hiệu suất phản ứng như sau :
1. Dựa vào một trong các chất tham gia phản ứng, công thức tính :

2.Dựa vào một trong các chất tạo thành, công thức tính :
2 Al 2 O 3 → 4Al + 3 O 2
Dựa vào phương trình ta có: Cứ 204g Al 2 O 3 thì tạo ra 108g Al
⇒ Để tạo ra 4 tấn Al thì khối lượng Al 2 O 3 cần = 4.204/108 = 7,55g
Hiệu suất phản ứng là 90%, có nghĩa là 7,55 tấn Al 2 O 3 chỉ chiếm 90% khối lượng phải dùng.
Khối lượng oxit phải dùng : 7,55x100/90 = 8,39 tấn
Khối lượng quặng boxit: 8,39x100/40 = 20,972 tấn
Đúng 2
Bình luận (0)
1 loại quặng boxit có chứa 60% tạp chất AL2O3. AL luyện từ oxit đó có chứa % tạp chất. tính khối lượng AL thu được khi luyện 6,8 tấn quặng trên. Biết hiệu suất =95%
Giải hộ mình vớiiiiiii
chứa % tạp chất vậy đó là bao nhiêu phần trăm em ơi?
Đúng 1
Bình luận (0)
Tính khối lượng Al thu được khi luyện 1 tấn quặng boxit biết quặng boxit này có chứa 20% Al2O3. Al luyện từ oxit đó có chứa 1,5% tạp chất cho hiệu suất phản ứng đạ 95%
Mong giải dùm các anh chị ơi~
2Al2O3\(\rightarrow\) 4Al + 3O2
mAl2O3= \(\frac{1000.20}{100}\)=200(kg)
Theo PTHH: mAl= 400(kg)
Vì có chứa 1,5% tạp chất
\(\rightarrow\)mAl thu được là trên lí thuyết là \(\frac{\text{400 - 400.1,5}}{100}\)=394(kg)
vì H=95% \(\Rightarrow\) mAl thực tế thu được là \(\frac{\text{394.95}}{100}\)=374,3(kg)
Một loại quặng boxit chứa 60% Al2O3. Sản xuất Al từ 2,125 tấn quặng boxit đó bằng phương pháp điện phân nóng chảy Al2O3 thu được 0,54 tấn Al. Tính hiệu suất quá trình sản xuất Al.
\(\text{m Al2O3 = 0,6.2,125 = 1,275 tấn}\)
2Al2O3 --->4 Al + 3O2
2.102.............4.27.H
1,275 tấn.........0,54 tấn
\(\text{---> 2.102.0,54 = 4.27.H. 1,275}\)
\(\text{--> H = 0,8 = 80%}\)
buithianhtho, Pham Van Tien, Duong Le, Nguyễn Thị Kiều, Dương Chung, Linh, Luân Trần, Arakawa Whiter, Trần Quốc Toàn, Đặng Anh Huy 20141919, Nguyễn Nhật Anh, Trần Hữu Tuyển, Phùng Hà Châu, Quang Nhân, Hoàng Tuấn Đăng, Nguyễn Trần Thành Đạt, Nguyễn Thị Minh Thương , Nguyễn Anh Thư,...
Trong quặng Bô-xit trung bình có 50% Al2O3. Kim loại luyện được từ Oxit đó có chứa 1,5% tạp chất. Tính lượng Al nguyên chất được điều chế từ nửa tấn quặng Bô-xít. Cho biết rằng để luyện nhân nguyên chất dùng phương trình hóa học luyện Al:
Al2O3 = Al + O2
Nửa tấn=500000g
2Al2O3-->4Al+3O2
Khối lượng Al2O3 nguyên chất trong nửa tấn quặng bô-xít là
500000.50%=250000(g)
Số mol của Al2O3 là
n=m/M=250000/102
=125000/51(mol)
Số mol của Al là
nAl=2nAl2O3=2.125000/51
=250000/51(mol)
Khối lượng của Al là
m=n.M=250000/51.27
=2250000/17( g)
Khối lượng của Al nguyên chất là
2250000/17-
(2250000/17.1.5%)
=2216250/17(g)
Đúng 0
Bình luận (0)
tính khối lượng Al sản suất được từ 1,5 tấn quặng boxit chứa 90% Al2O3 biết hiệu suất quá trình phản ứng là 90%
mAl2O3=1,35 tấn
2Al2O3=> 4Al+ 3O2
204 ............108
1,35............x
=> x=0,71 tấn
mAl thu được= 90%*0,71=0,639 tấn=639 kg
Đúng 0
Bình luận (0)
Bài 1: Người ta dùng quặng Ôxít để sản xuất Nhôm theo sơ đồ sau:
Al2O3 --> Al + O2
Hàm lượng Al2O3 trong Ôxít là 40%. Để có được 4 tấn Al nguyên chất cần bao nhiêu tấn quặng? Biết H = 90%?
Bài 2: Có thể điều chế được bao nhiêu kg Al từ 1 tấn quặng Ôxít có chứa 95% Nhôm Ôxít biết H của quá trình phản ứng là 98%
Hematit là quặng phổ biến nhất của sắt trong tự nhiên, được dùng để sản xuất gang. Từ 1 tấn quặng hematit (chứa 70% oxit sắt về khối lượng, còn lại là tạp chất trơ) có thể sản xuất được lượng gang thành phẩm (chứa 5% C về khối lượng) tối đa là A. 506,9 kg B. 515,8 kg C. 533,6 kg D. 490 kg
Đọc tiếp
Hematit là quặng phổ biến nhất của sắt trong tự nhiên, được dùng để sản xuất gang. Từ 1 tấn quặng hematit (chứa 70% oxit sắt về khối lượng, còn lại là tạp chất trơ) có thể sản xuất được lượng gang thành phẩm (chứa 5% C về khối lượng) tối đa là
A. 506,9 kg
B. 515,8 kg
C. 533,6 kg
D. 490 kg
Đáp án B
Ta có: m(Fe2O3) = 7.103 (kg) → n(Fe2O3) = 4,375 mol → n(Fe trong gang) = 4,375. 2 = 8,75
→ m(Fe trong gang) = 490 → m(gang) = 490. 100 : 95 = 515,8 (kg)
Đúng 0
Bình luận (0)