Đốt cháy hoàn toàn 23 gam chất A cần 33,6 lít ôxi (đktc) và thu được thể tích CO2 bằng 2/3 thể tích hơi nước. Xác định CTHH của A. Biết rằng tỉ khối của A so với khí ôxi là 1,4375

Những câu hỏi liên quan
2. Đốt cháy hoàn toàn 23 gam hợp chất A cần 33,6 lít ôxi (đktc) và thu được thể tích CO2 bằng 2/3 thể tích hơi nước . Xác định CTHH của A. Biết rằng tỉ khối hơi của A so với khí ôxi là 1,4375.
Do đốt cháy A thu được sản phẩm chứa C, H, O
=> Trong A chứa C, H và có thể có O
Gọi \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{2}{3}a\left(mol\right)\\n_{H_2O}=a\left(mol\right)\end{matrix}\right.\)
\(n_{O_2}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\)
Theo ĐLBTKL: \(44.\dfrac{2}{3}a+18a=23+1,5.32=71\)
=> a = 1,5 (mol)
=> \(\left\{{}\begin{matrix}n_C=n_{CO_2}=1\left(mol\right)\\n_H=2.n_{H_2O}=3\left(mol\right)\end{matrix}\right.\)
=> \(n_O=\dfrac{23-1.12-3.1}{16}=0,5\left(mol\right)\)
Xét nC : nH : nO = 1 : 3 : 0,5 = 2 : 6 : 1
=> CTPT: (C2H6O)n
Mà MA = 1,4375.32 = 46 (g/mol)
=> n = 1
=> CTPT: C2H6O
Đúng 3
Bình luận (0)
\(n_{O_2}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\\ m_{O_2}=1,5.32=48\left(g\right)\)
Bảo toàn khối lượng: mH2O + mCO2 = mA + mO2 = 23 + 48 = 71 (g)
Ta có:
\(\dfrac{V_{CO_2}}{V_{H_2O}}=\dfrac{2}{3}\Rightarrow\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{2}{3}\\ \Rightarrow\dfrac{m_{CO_2}}{m_{H_2O}}=\dfrac{2}{3}.\dfrac{44}{18}=\dfrac{44}{27}\\ \Rightarrow\dfrac{m_{CO_2}}{44}=\dfrac{m_{H_2O}}{27}\)
Theo t/c của dãy tỉ số bằng nhau:
\(\dfrac{m_{CO_2}}{44}=\dfrac{m_{H_2O}}{27}=\dfrac{m_{CO_2}+m_{H_2O}}{44+27}=\dfrac{71}{71}=1\)
=> \(\left\{{}\begin{matrix}m_{CO_2}=1.44=44\left(g\right)\\m_{H_2O}=1.27=27\left(g\right)\end{matrix}\right.\)
Bảo toàn C và H: \(\left\{{}\begin{matrix}n_C=n_{CO_2}=\dfrac{44}{44}=1\left(mol\right)\\n_H=2n_{H_2O}=\dfrac{2.27}{18}=3\left(mol\right)\end{matrix}\right.\)
Bảo toàn O: \(n_O=\dfrac{23-12-3}{16}=0,5\left(mol\right)\)
MA = 1,4375.32 = 46 (g/mol)
CTPT của A có dạng: CxHyOz
=> x : y : z = 1 : 3 : 0,5 = 2 : 6 : 1
=> (C2H6O)n = 46
=> n = 1
=> CTPT của A là C2H6O
Đúng 2
Bình luận (1)
Đốt cháy hoàn toàn 23 gam hợp chất A cần 33,6 lít oxi (đkt) và thu được thể tích CO2 bằng 2 phần 3 thể tích hơi nước. Xác định công thức hoá của A. Biết rằng tỉ khối hơi của A so với khí oxi là 1,4375.
Tham khảo:
Đốt cháy A chỉ tạo ra CO2 và H2O nên A chứa C;H;O
Vậy A có dạng CxHyOz
Phản ứng xảy ra:
CxHyOz+(x+y/4−z/2)O2to→xCO2+y2H2O
Ta có:
MA=1,4375MO2=1,4375.32=46
→12x+y+16z=46
Ta có:
nA=23/46=0,5 mol
nO2=33,6/22,4=1,5 mol
→x+y/4−z/2=nO2/nA=1,5/0,5=3
Ta có:
nCO2:nH2O=x:y2=2:3→x:y=2:6=1:3
Giải được: x=2;y=6;y=1
Vậy A là C2H6O
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 23g hợp chất A cần 33,6 lít oxi (đ.k.t.c) và thu được thể tích \(CO_2\) bằng 2/3 thể tích hơi nước. Xác định CTHH của A. Biết rằng tỉ khối hơi của A si với khí oxi là 1,4375
Vì đốt cháy A sinh ra \(CO_2\)và nước nên \(\Rightarrow\)hợp chất ban đầu chứa C,H,O
\(M_A=1,4375.32=46\left(đvC\right)\)
Vì tỉ lệ thể tích cũng là tỉ lệ mol nên: \(\dfrac{V_{CO_2}}{V_{H_2O}}=\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{2}{3}\)vì \(n_{CO_2}< n_{H_2O}\)
\(\Rightarrow\)Hợp chất A no
Gọi A có CTC là \(C_nH_{2n+2}O\)và số mol A là 1 mol, ta có:
\(C_nH_{2n+2}O+\dfrac{3n}{2}O_2\rightarrow nCO_2+\left(n+1\right)H_2O\)
\(\dfrac{n}{n+1}\)\(=\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{2}{3}\)⇒ n=2
\(C_2H_6O\)(46 đvC)
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 1,88 gam chất hữu cơ A (chứa C, H, O) cần 1,904 lít O2 (đktc) thu được CO2 và hơi nước theo tỉ lệ thể tích 4:3. Hãy xác định công thức phân tử của A. Biết tỉ khối của A so với không khí nhỏ hơn 7. A. C8H12O5. B. C4H8O2. C. C8H42O3. D. C6H12O6.
Đọc tiếp
Đốt cháy hoàn toàn 1,88 gam chất hữu cơ A (chứa C, H, O) cần 1,904 lít O2 (đktc) thu được CO2 và hơi nước theo tỉ lệ thể tích 4:3. Hãy xác định công thức phân tử của A. Biết tỉ khối của A so với không khí nhỏ hơn 7.
A. C8H12O5.
B. C4H8O2.
C. C8H42O3.
D. C6H12O6.
Thông thường khi đề bài cho số mol O2 cần để đốt cháy thì chắc chắn ta sẽ phải sử dụng hoặc định luật bảo khối lượng, hoặc bảo toàn nguyên tố Oxi.
Quay trở lại bài toán này, ta thấy đề cho cần dùng 1,904 lít O2, không cho khối lượng CO2 và H2O mà chỉ cho tỉ lệ thể tích (tỉ lệ số mol), do đó nhận ra được nếu ta sử dụng phương pháp bảo toàn khối lượng ta sẽ tính được số mol CO2 và số mol H2O, từ đó tính được số mol O trong A. Tiếp theo đó ta sẽ xác định công thức đơn giản nhất để tìm ra công thức phân tử.
Có: n O 2 = 1 , 904 22 , 4 = 0 , 085 ( m o l ) ⇒ m O 2 = 0 , 085 . 32 = 2 , 72 ( g a m )
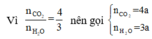
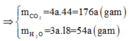
Sơ đồ phản ứng: A + O2 ⇒ CO2 + H2O
Áp dụng định luật bảo toàn khối lượng ta có: m A + m O 2 = m C O 2 + m H 2 O
Hay 1,88 + 2,72 = 176a + 54a ⟺ a = 0,02
⇒ 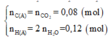
![]()
![]()
Vì C : H : O = nC : nH : nO =0,08 : 0,12 : 0,05 = 8 : 12 : 5
Nên công thức đơn giản nhất của A là C8H12O5.
Khi đó công thức phân tử của A có dạng (C8H12O5)n
Mà MA < 7Mkhôngkhí nên 188n < 7.29 ⇒ n < 1,08 ⇒ n = l
Do đó công thức phân tử của A là C8H12O5.
Đáp án A.
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 23 gam hợp chất A cần 33,6 lít oxi ( dktc) và thu được thể tích CO2 bằng 2/3 thể tích hơi nước Xác định CTHH của A biết tỉ khối của A đối với Oxi bằng 1,4375
Gọi công thức của A là CxHyOz
CxHyOz(0,5) + (x+\(\frac{y}{4}\)−\(\frac{z}{2}\))O2(0,5x+0,125y−0,25z) → xCO2(0,5x) + \(\frac{y}{2}\)H2O(0,25y)
Ta có: MA = 32.1,4375 = 46
⇒ 12x + y + 16z = 46 (1)
⇒ nCxHyOz = 23/46 = 0,5(mol)
Thể tích khí CO2 bằng 2:3 thể tích hơi nước
⇒ \(\frac{0,5x}{0,25y}\) = \(\frac{2}{3}\)
⇔ y = 3x (2)
nO2 = \(\frac{33,6}{22,4}\) = 1,5(mol)
⇒ 0,5x + 0,125y − 0,25z = 1,5(3)
Từ (1), (2), (3) ta có hệ: \(\left\{{}\begin{matrix}12x+y+16z=46\\y=3x\\0,5x=0,125y-0,25z=1,5\end{matrix}\right.\)
Giải hệ phương trình ta có:
x=2
y=6
z=1
Vậy công thức hóa học của A là :C2H6O
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 6,9 gam hợp chất hữu cơ A sau phản ứng thu được 13,2 gam khí CO2 và 8,1 gam nước
a) Chứng minh A không phải là hidrocacbon
b) Xác định CTPT của A. Biết tỉ khối hơi của A so với khí oxi bằng 1,4375
c) Cho hết lượng chất A trên vào Axit axetic thu được hỗn hợp B. Đun nóng hỗn hợp B với H2SO4 xúc tác.
- Hỏi PƯHH có xảy ra không? Viết PTHH, cho biết tên phản ứng và tên sản phẩm hữu cơ (nếu có)
- Trong trường hợp có xảy ra phản ứng và thu được 7,92 gam sản phẩm hữu cơ thì hiệu suất...
Đọc tiếp
Đốt cháy hoàn toàn 6,9 gam hợp chất hữu cơ A sau phản ứng thu được 13,2 gam khí CO2 và 8,1 gam nước a) Chứng minh A không phải là hidrocacbon b) Xác định CTPT của A. Biết tỉ khối hơi của A so với khí oxi bằng 1,4375 c) Cho hết lượng chất A trên vào Axit axetic thu được hỗn hợp B. Đun nóng hỗn hợp B với H2SO4 xúc tác. - Hỏi PƯHH có xảy ra không? Viết PTHH, cho biết tên phản ứng và tên sản phẩm hữu cơ (nếu có) - Trong trường hợp có xảy ra phản ứng và thu được 7,92 gam sản phẩm hữu cơ thì hiệu suất của phản ứng là bao nhiêu?
Đốt cháy hoàn toàn 2,82 gam chất hữu cơ A cần 2,856 lít khs O2 thu được khí CO2 và hơi nước theo tỉ lệ thể tích Vco2/Vh2o = 4/3 ( các khi đo ở điều kiện tiêu chuẩn ) . Hãy xác định công thức phân tử của A . Biết tỉ khối của A với không khí nhỏ hơn 7
Ta có: \(n_{O_2}=\dfrac{2,856}{22,4}=0,1275\left(mol\right)\)
\(\dfrac{V_{CO_2}}{V_{H_2O}}=\dfrac{4}{3}\Rightarrow\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{4}{3}\)
Gọi: nCO2 = 4x (mol) ⇒ nH2O = 3x (mol)
Theo ĐLBT KL, có: mA + mO2 = mCO2 + mH2O
⇒ 2,82 + 0,1275.32 = 4x.44 + 3x.18
⇒ x = 0,03
⇒ nCO2 = 0,03.4 = 0,12 (mol) = nC
nH2O = 0,03.3 = 0,09 (mol) ⇒ nH = 0,09.2 = 0,18 (mol)
Ta có: mC + mH = 0,12.12 + 0,18.1 = 1,62 (g) < 2,82 (g)
→ A chứa C, H và O.
⇒ mO = 2,82 - 1,62 = 1,2 (g) \(\Rightarrow n_O=\dfrac{1,2}{16}=0,075\left(mol\right)\)
Gọi CTPT của A là CxHyOz
⇒ x:y:z = 0,12:0,18:0,075 = 8:12:5
→ CTPT của A có dạng là (C8H12O5)n (n nguyên dương)
Mà: \(M_A< 29.7=203\left(g/mol\right)\)
\(\Rightarrow\left(12.8+12.1+16.5\right)n< 203\)
⇒ n < 1,08 ⇒ n = 1
Vậy: CTPT của A là C8H12O5.
Đúng 1
Bình luận (2)
Anh chị làm ơn giúp e mấy bài này ạ.E cảm ơn!Bài 1:Khi đốt cháy hoàn toàn một lượng hợp chất hữu cơ X cần 0,8 gam O2 người ta thu được 1,1 gam CO2,0,45 gam H2O và không có sản phẩm nào khác. Xác định công thức phân tử của X. Biết rằng khi cho bay hơi hoàn toàn 0,6gam X ở điều kiện nhiệt độ và áp suất thích hợp đã thu được một thể tích hơi đúng bằng thể tích hơi của 0,32 gam O2 trong cùng điều kiện.Bài 2:Đốt cháy hoàn toàn một hợp chất hữu cơ A có thành phần C,H,O thu được CO2 có thể tích bằng 3/...
Đọc tiếp
Anh chị làm ơn giúp e mấy bài này ạ.E cảm ơn!
Bài 1:
Khi đốt cháy hoàn toàn một lượng hợp chất hữu cơ X cần 0,8 gam O2 người ta thu được 1,1 gam CO2,0,45 gam H2O và không có sản phẩm nào khác. Xác định công thức phân tử của X. Biết rằng khi cho bay hơi hoàn toàn 0,6gam X ở điều kiện nhiệt độ và áp suất thích hợp đã thu được một thể tích hơi đúng bằng thể tích hơi của 0,32 gam O2 trong cùng điều kiện.
Bài 2:
Đốt cháy hoàn toàn một hợp chất hữu cơ A có thành phần C,H,O thu được CO2 có thể tích bằng 3/4 thể tích hơi nước và bằng 6/7 thể tích O2 dùng để đốt cháy. Mặt khác, 1l hơi A có khối lượng bằng 46 lần khối lượng 1 lít H2 ở cùng điều kiện.Tìm công thức phân tử của A.
Bài 3: Đốt cháy hoàn toàn 4,3 gam hợp chất hữu cơ thu được 6,72 lít CO2 và 0,35 mol H2O. Khi đốt cháy hoàn toàn 1 mol chất A cần 212,8l O2.Xác định CTPT của A.
Đốt cháy hoàn toàn 7g hợp chất hữu cơ A thu được 11,2 l khí CO2 đo ở đktc và 9 g nước.
a, Xác định CTHH của A biết tỉ khối dA/CH4=1,75
b, Tính thể tích không khí cần dùng để đốt cháy hoàn toàn a biết oxi chiếm 20% không khí























