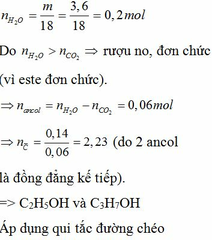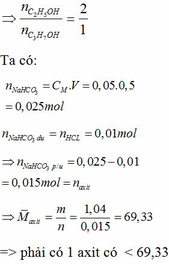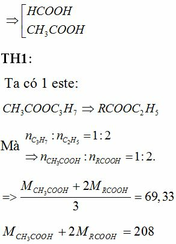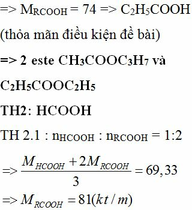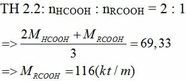Chỉ có bơm đựng khí CO2, dd NaOH không rõ nồng độ và hai cốc thủy tinh có chia độ. Hãy điều chế dd Na2CO3 không lẫn NaOH va muối NaHCO3 mà không dùng thêm một phương pháp hoặc nguyên liệu nào khác.

Những câu hỏi liên quan
1/. Cho BaO vào dung dịch H2SO4 thu được kết tủa A, dung dịch B. Thêm một lượng dư bột nhôm vào dung dịch B thu được dung dịch C và khí H2 bay lên. Thêm dung dịch K2CO3 vào dung dịch C thấy tách ra kết tủa D. Xác định thành phần A, B, C, D và viết các phương trình phản ứng xảy ra.2/. Chỉ dùng bơm khí CO2, dung dịch NaOH không rõ nồng độ, hai cốc thủy tinh có chia vạch thể tích. Hãy nêu cách điều chế dung dịch Na2CO3 không lẫn NaOH hay NaHCO3 mà không dùng thêm hóa chất và các phương tiện khác
Đọc tiếp
1/. Cho BaO vào dung dịch H2SO4 thu được kết tủa A, dung dịch B. Thêm một lượng dư bột nhôm vào dung dịch B thu được dung dịch C và khí H2 bay lên. Thêm dung dịch K2CO3 vào dung dịch C thấy tách ra kết tủa D. Xác định thành phần A, B, C, D và viết các phương trình phản ứng xảy ra.
2/. Chỉ dùng bơm khí CO2, dung dịch NaOH không rõ nồng độ, hai cốc thủy tinh có chia vạch thể tích. Hãy nêu cách điều chế dung dịch Na2CO3 không lẫn NaOH hay NaHCO3 mà không dùng thêm hóa chất và các phương tiện khác
2 Lấy cùng một thể tích dd NaOH cho vào 2 cốc thủy tinh riêng biệt. Giả sử lúc đó mối cốc chứa a mol NaOH.
Sục CO2 dư vào một cốc, phản ứng tạo ra muối axit.
CO2 + 2NaOH → Na2CO3 + H2O (1)
CO2 + Na2CO3 + H2O → 2NaHCO3 (2)
Theo pt (1,2) nNaHCO3 = nNaOH = a (mol)
* Lấy cốc đựng muối axit vừa thu được đổ từ từ vào cốc đựng dung dịch NaOH ban đầu. Ta thu được dung dịch Na2CO3 tinh khiết
NaHCO3 + NaOH → Na2CO3 + H2O
Đúng 0
Bình luận (0)
1.Kết tủa A là BaSO4, dung dịch B có thể là H2SO4 dư hoặc Ba(OH)2
TH1: Dung dịch B là H2SO4 dư
Dung dịch C là Al2(SO4)3 ; Kết tủa D là Al(OH)3
TH2: Dung dịch B là Ba(OH)2
Dung dịch C là: Ba(AlO2)2 ; Kết tủa D là BaCO3
các pthh
BaO + H2SO4 → BaSO4 + H2O
BaO + H2O → Ba(OH)2
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Al2(SO4)3 + 3Na2CO3 + 3H2O → 2Al(OH)3 + 3CO2 + 3Na2SO4
Ba(OH)2 + 2H2O + 2Al → Ba(AlO2)2 + 3H2
Ba(AlO2)2 + Na2CO3 → BaCO3 + 2NaAlO2
Đúng 0
Bình luận (0)
có các hóa chất và dụng vụ sau: khí co2, bình tam giác có vạch chia, dd B. cho naoh và ỗng hút. Trình bày ngắn gọn phương pháp điều chế na2co3 tinh khiết
Cho 3 miếng Al vào 3 cốc đựng dd HNO3 có nồng độ khác nhau. Cốc 1 thấy có khí không màu bay ra và hoá nâu ngoài không khí. Cốc 2 thấy thoát ra khí không màu ko mùi, không cháy, nhẹ hơn oxi. Cốc 3 không thấy có khí nào bay ra, thu được dd trong suốt.
a, Viết các PTHH
b, Nếu lượng Al tan ra ở mỗi cốc là 5,4g thì lượng HNO3 dùng trong mỗi trường hợp là bao nhiêu mol. Tính thể tích khí thoát ra ở cốc 1 và cốc 2 (điều kiện tiêu chuẩn)
Đọc tiếp
Cho 3 miếng Al vào 3 cốc đựng dd HNO3 có nồng độ khác nhau. Cốc 1 thấy có khí không màu bay ra và hoá nâu ngoài không khí. Cốc 2 thấy thoát ra khí không màu ko mùi, không cháy, nhẹ hơn oxi. Cốc 3 không thấy có khí nào bay ra, thu được dd trong suốt. a, Viết các PTHH b, Nếu lượng Al tan ra ở mỗi cốc là 5,4g thì lượng HNO3 dùng trong mỗi trường hợp là bao nhiêu mol. Tính thể tích khí thoát ra ở cốc 1 và cốc 2 (điều kiện tiêu chuẩn)
a) PTHH: \(Al+4HNO_3\rightarrow Al\left(NO_3\right)_3+NO\uparrow+2H_2O\) (1)
\(10Al+36HNO_3\rightarrow10Al\left(NO_3\right)_3+3N_2\uparrow+18H_2O\) (2)
\(8Al+30HNO_3\rightarrow8Al\left(NO_3\right)_3+3NH_4NO_3+9H_2O\) (3)
b) Ta có: \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}n_{HNO_3\left(1\right)}=0,8\left(mol\right)\\n_{HNO_3\left(2\right)}=0,72\left(mol\right)\\n_{HNO_3\left(3\right)}=0,75\left(mol\right)\end{matrix}\right.\)
Mặt khác: \(\left\{{}\begin{matrix}n_{NO}=0,2\left(mol\right)\\n_{N_2}=0,06\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{NO}=0,2\cdot22,4=4,48\left(l\right)\\V_{N_2}=0,06\cdot22,4=1,344\left(l\right)\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Thêm 8,96l khí CO2 đo ở ĐKTC vào 200g dd NaOH đủ được sản phẩm có muối natri cacbonat và nước.
a. lập PTHH xảy ra và tính nồng độ phần trăm của dd NaOH đã dùng ?
b. tính nồng độ phần trăm của dd muối thu được sau phản ứng?
nCO2=0,4(mol)
a) PTHH: 2 NaOH + CO2 -> Na2CO3 + H2O
0,8_________0,4________0,4(mol)
=> mNaOH=0,8.40=32(g)
=>C%ddNaOH=(32/200).100=16%
b) mddNa2CO3=mddNaOH+mCO2=200+0,4.44=217,6(g)
mNa2CO3=106.0,4=42,4(g)
=>C%ddNa2CO3=(42,4/217,6).100=19,485%
Chúc em học tốt!
Đúng 2
Bình luận (0)
nCO2=8,96/22,4=0,4mol
a/ CO2+2NaOH→Na2CO3+H2O
0,4 0,8 0,4 0,4
mNaOH=0,8.40=32g
C%ddNaOH=mct/mdd.100%=32/200.100%=16%
b/mCO2=0,4.44=17,6g
Theo định luật bảo toàn khối lượng:
mCO2+mNaOH=mNa2CO3
17,6g+200g=217,6g
mNa2CO3=0,4.106=42,4g
C%ddNa2CO3=mct/mdd.100%=42,4/217,6.100=19,4852g
Đúng 0
Bình luận (0)
Cho 4,48 lít CO2 (đktc) hấp thụ hết trong 400 ml dd NaOH thu được dd X chứa nồng độ của muối Na2CO3 0,1M ( coi thể tích dung dịch không bị thay đổi khi hấp thụ). Tính nồng độ CM của dd NaOH?
$n_{CO_2} = \dfrac{4,48}{22,4} = 0,2(mol)$
$n_{Na_2CO_3} = 0,4.0,1 = 0,04(mol)$
Bảo toàn Cacbon : $n_{NaHCO_3} = 0,2 - 0,04 = 0,16(mol)$
Bảo toàn Natri :$n_{NaOH} = 0,16 + 0,04.2 = 0,24(mol)$
$C_{M_{NaOH}} = \dfrac{0,24}{0,4} = 0,6M$
Đúng 1
Bình luận (0)
\(n_{Na_2CO_3}=0.1\cdot0.4=0.04\left(mol\right)\)
\(n_{CO_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\)
\(0.08...........0.04.............0.04\)
\(NaOH+CO_2\rightarrow NaHCO_3\)
\(0.16......0.2-0.04\)
\(n_{NaOH}=0.08+0.16=0.24\left(mol\right)\)
\(C_{M_{NaOH}}=\dfrac{0.24}{0.4}=0.6\left(M\right)\)
Đúng 1
Bình luận (0)
1. Tính khối lượng Na cần cho vào 150g dd NaOH 8% để thu được dd mới có nồng độ là 10,513%.2. Cho 8,5g hỗn hợp 2 kim loại kiềm A và B thuộc 2 chu kì liên tiếp nhau tan hết vào trong nước được 3,36 lít khí H2 (đktc). Xác định A và B.3.Cho 1ml dd A chứa NaOH và 0,3 mol NaAlO2. Cho 1 mol HCl vào A thu được 15,6g kết tủa. Tính khối lượng NaOH trong dd A.4. Cho Ba(OH)2 có dư vào dd FeCl2, CuSO4, AlCl3 thu được kết tủa. Nung kết tủa trong không khí đến khi có khối lượng không đổi thu được chất rắn A....
Đọc tiếp
1. Tính khối lượng Na cần cho vào 150g dd NaOH 8% để thu được dd mới có nồng độ là 10,513%.2. Cho 8,5g hỗn hợp 2 kim loại kiềm A và B thuộc 2 chu kì liên tiếp nhau tan hết vào trong nước được 3,36 lít khí H2 (đktc). Xác định A và B.3.Cho 1ml dd A chứa NaOH và 0,3 mol NaAlO2. Cho 1 mol HCl vào A thu được 15,6g kết tủa. Tính khối lượng NaOH trong dd A.4. Cho Ba(OH)2 có dư vào dd FeCl2, CuSO4, AlCl3 thu được kết tủa. Nung kết tủa trong không khí đến khi có khối lượng không đổi thu được chất rắn A. Trong A gồm có những chất nào?5. Có 4 lọ không nhãn, mỗi lọ đựng một dd không màu sau: CaCl2, Ba(OH)2, KOH, Na2SO4.Chỉ dùng quỳ tím hẫy nhận biết các dd đựng trong mỗi lọ. Viết các PTHH.6. Để sản xuất 1 tấn vôi chứa 85% CaO. Người ta phải tiêu thụ bao nhiêu kg đá vôi chứa 94% canxi cacbonat. Biết hiệu suất phản ứng là 85%.7. Có hỗn hợp A gồm Cuo và Fe2O3. Chỉ dùng Al, dung dịch HCl. Hẫy điều chế 2 kim loại tinh khiết từ A (làm 3 cách).8. Hãy tính toán và trình bày cách pha chế dd MgSO4 từ MgSO4.7H2O và nước để có:a) 80g dd MgSO4 6%.b) 200ml dd MgSO4 1M.9. Tính khối lượng CuSO4.5H2O và khối lượng nước cần lấy để điều chế được 200g dd CuSO4 15%.10. Dẫn luồng khí H2 qua ống thủy tinh chưa 28g bột CuO nung nóng. Sau một thời gian thu được 24g rắn.Xác định khối lượng hơi nước tạo thành.
\(n_{CuO}=\dfrac{28}{80}=0,35\left(mol\right)\)
\(n_{Cu}=\dfrac{24}{64}=0,375\left(mol\right)\)
CuO + H2 \(\rightarrow\) Cu + H2O
de: 0,375\(\rightarrow\) 0,375
\(m_{H_2O}=18.0,375=6,75g\)
Đúng 0
Bình luận (0)
Không dùng thêm hóa chất phân biệt các dd sau có cùng nồng độ NaHSO4, NaHCO3,NaCO3,BaCl2, NaCl,NaOH vt ptpu Cứu mai tui phải nộp zùiiiii
Bạn xem lại đề vì nếu ko dùng thuốc thử thì sẽ còn lại 2 chất ko phân biệt được là NaOH và NaCl
Đúng 0
Bình luận (1)
1. Đốt cháy từ CuO và FeO với C có dư thì được chất rắn A và khí B. Cho B tác dụng với nước vôi trong có dư thì được 8g kết tủa. Chất rắn A cho tác dụng với dd HCl có nồng độ 10% thì cần dùng một lượng axit là 73g sẽ vừa đủ. Tính khối lượng CuO và FeO trong hỗn hợp ban đầu và thể tích khí B.2. Có 4 lọ không nhãn, mỗi lọ đựng một dd không màu sau: CaCl2, Ba(OH)2, KOH, Na2SO4. Chỉ dùng quỳ tím hãy nhận biết các dd đựng trong mỗi lọ. Viết các PTHH.3. Trình bày phương pháp hóa học để tuinh chế khí C...
Đọc tiếp
1. Đốt cháy từ CuO và FeO với C có dư thì được chất rắn A và khí B. Cho B tác dụng với nước vôi trong có dư thì được 8g kết tủa. Chất rắn A cho tác dụng với dd HCl có nồng độ 10% thì cần dùng một lượng axit là 73g sẽ vừa đủ. Tính khối lượng CuO và FeO trong hỗn hợp ban đầu và thể tích khí B.
2. Có 4 lọ không nhãn, mỗi lọ đựng một dd không màu sau: CaCl2, Ba(OH)2, KOH, Na2SO4. Chỉ dùng quỳ tím hãy nhận biết các dd đựng trong mỗi lọ. Viết các PTHH.
3. Trình bày phương pháp hóa học để tuinh chế khí CO từ hỗn hợp khí: CO2, SO2, CO.
4. Tính khối lượng của CuSO4.5H2O và khối lượng nước cần lấy để điều chế được 200g dd CuSO4 15%.
câu 1 lớp 8 thì viết pt là xong ,còn không thì qui đổi hh ,C+2O-->CO2(C dư phi lí nên ko phải lớp 8 đề sai
2. quì: tím||xanh||xanh|| tím(phân xanh và tím cho xanh vào tím
Ba(OH)2 vẫn ***c trắng|| || ||kt trắng
KOH vẫn ***c trắng|| || ||ko ht
Ca2++2OH- -->Ca(OH)2
Ba2++SO42- -->BaSO4
3. cho hh qua CaO dư (khó nhận biết) hoạc dùng cách khác sục hh khí qua Ca(OH)2 khí thu được tiếp tục cho qua CaOkhan ( loại bỏ H2O)
4.
CuSO4.5H2O-->CuSO4+5H2O
0.1875 0.1875
n=mdd*C%/(100*M)=0.1875
=>mCuSO4.5H2O=n*M=46.875g
BT klg:mH2Othêm=md*** rắn=153.125g
Đúng 0
Bình luận (2)
Đun nóng hỗn hợp hai este đơn chức với dd NaOH vừa đủ thu được hỗn hợp 2 rượu đồng đẳng kế tiếp và hỗn hợp 2 muối. Đốt cháy hoàn toàn một lượng hỗn hợp rượu trên thu được 3,136 lít khí CO2 (đktc) và 3,6 gam H2O. Cho hỗn hợp hai muối trên tác dụng với dd H2SO4 vừa đủ được hỗn hợp hai axit cacboxylic. Cho từ từ 50ml dd NaHCO3 0,5M vào cốc đựng 1,04 gam hỗn hợp hai axit thu được ở trên, sau phản ứng cần phải dùng 10ml dd HCl 1M mới tác dụng vừa hết với lượng NaHCO3 dư. Xác định công thức cấu tạo củ...
Đọc tiếp
Đun nóng hỗn hợp hai este đơn chức với dd NaOH vừa đủ thu được hỗn hợp 2 rượu đồng đẳng kế tiếp và hỗn hợp 2 muối. Đốt cháy hoàn toàn một lượng hỗn hợp rượu trên thu được 3,136 lít khí CO2 (đktc) và 3,6 gam H2O. Cho hỗn hợp hai muối trên tác dụng với dd H2SO4 vừa đủ được hỗn hợp hai axit cacboxylic. Cho từ từ 50ml dd NaHCO3 0,5M vào cốc đựng 1,04 gam hỗn hợp hai axit thu được ở trên, sau phản ứng cần phải dùng 10ml dd HCl 1M mới tác dụng vừa hết với lượng NaHCO3 dư. Xác định công thức cấu tạo của hai este có trong hỗn hợp đầu. Biết khi đốt cháy 1 mol mỗi este thu được không quá 5mol CO2.