Tính khối lượng của Cu có trong 64g CuSO4

Những câu hỏi liên quan
Tính khối lượng đồng Cu có trong 64g đồng sunfat CuSO4?
nhanh vs ạ cần gấp!!!
Cách 1: Ta có: \(n_{CuSO_4}=\dfrac{64}{160}=0,4\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,4.64=25,6\left(g\right)\)
Cách 2:
Ta có: \(\%m_{Cu}=\dfrac{64}{64+32+16.4}.100\%=40\%\)
\(\Rightarrow m_{Cu}=64.40\%=25,6\left(g\right)\)
Bạn tham khảo nhé!
Đúng 3
Bình luận (1)
Hai bình điện phân (CuSO4/Cu và AgNO3/Ag) mắc nối tiếp . Trong một mạch điện . Sau 1 thời gian điện phân , khối lượng của catot của 2 bình tăng lên 2,8g . Biết đồng có khối lượng mol nguyên tử là 64g/mol , hóa trị 2 và bạc có khối lượng mol nguyên tử là 108 g/mol , hóa trị 1
a) Tính điện lượng qua các bình điện phân và khối lượng Cu và Ag được giải phóng ở catot
b) Nếu I0,5A . Tính thời gian điện phân .
Đọc tiếp
Hai bình điện phân (CuSO4/Cu và AgNO3/Ag) mắc nối tiếp . Trong một mạch điện . Sau 1 thời gian điện phân , khối lượng của catot của 2 bình tăng lên 2,8g . Biết đồng có khối lượng mol nguyên tử là 64g/mol , hóa trị 2 và bạc có khối lượng mol nguyên tử là 108 g/mol , hóa trị 1
a) Tính điện lượng qua các bình điện phân và khối lượng Cu và Ag được giải phóng ở catot
b) Nếu I=0,5A . Tính thời gian điện phân .
a/ \(m_{Cu}=\dfrac{I.A_{Cu}.t}{F.n_{Cu}};m_{Ag}=\dfrac{I.A_{Ag}.t}{F.n_{Ag}}\)
\(m_{Cu}+m_{Ag}=2,8\Leftrightarrow\dfrac{I.64.t}{96500.2}+\dfrac{I.108.t}{96500.1}=2,8\)
\(\Rightarrow q=I.t=2,8.\dfrac{4825}{7}=1930\left(C\right)\)
\(\Rightarrow m_{Cu}=\dfrac{1930.64}{96500.2}=...\left(g\right);m_{Ag}=\dfrac{1930.108}{96500}=...\left(g\right)\)
b/ \(q=I.t=1930\Rightarrow t=\dfrac{1930}{0,5}=3860\left(s\right)\)
Đúng 0
Bình luận (0)
1.Tính khối lượng Cu CÓ TRONG 48g CuSO4?
2.Tính lượng sắt có trong 60 tấn quặng sắt chứa 80% Fe2O3
1, \(n_{CuSO_4}=\dfrac{48}{160}=0,3 (mol)\)
\(n_{Cu}=n{CuSO_4}=0,3 mol\)
\(=> m_{Cu}=0,3 \) x 64 = 19, 2 (gam)
2, CHỊU
Đúng 1
Bình luận (0)
\(n=\dfrac{m}{M}=\dfrac{48}{160}=0,3\left(mol\right)\)
\(=>m=0,3.64=19,2\left(g\right)\)
Đúng 1
Bình luận (0)
Trong tự nhiên đồng có 2 đồng vị là 63Cu và 65Cu. Nguyên tử khối trung bình của Cu là 63,54. Tính thành phần % khối lượng của 63Cu trong CuSO4? A. 28,83%. B. 10,97% C. 11,00%. D. 28,74%.
Đọc tiếp
Trong tự nhiên đồng có 2 đồng vị là 63Cu và 65Cu. Nguyên tử khối trung bình của Cu là 63,54. Tính thành phần % khối lượng của 63Cu trong CuSO4?
A. 28,83%.
B. 10,97%
C. 11,00%.
D. 28,74%.
Đáp án A
Giả sử % nguyên tử 65Cu và 63Cu trong tự nhiên lần lượt là x, y.
Ta có hpt:
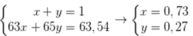
Phần trăm khối lượng của 63Cu trong CuSO4 là
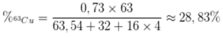
Đúng 0
Bình luận (0)
Cho dung dịch CuSO4 có chứa 64g CuSO4 phản ứng vừa đủ với 400ml dung dịch NaOH a.Viết phương trình hoá học xảy ra b.Tính khối lượng kết tủa thu được c.tính nồng độ mol của dung dịch NaOH
a) $CuSO_4 + 2NaOH \to Cu(OH)_2 + Na_2SO_4$
b) Theo PTHH : $n_{Cu(OH)_2} = n_{CuSO_4} = \dfrac{64}{160} = 0,4(mol)$
$m_{Cu(OH)_2} = 0,4.98 = 39,2(gam)$
c) $n_{NaOH} = 2n_{CuSO_4} = 0,8(mol)$
$C_{M_{NaOH}} = \dfrac{0,8}{0,4} = 2M$
Đúng 2
Bình luận (0)
1. Khối lượng của CuSO4 trong dd là 64g, khối lượng của tinh thể ngậm nước là 100g. Xác định CTHH muối ngậm nước
2. Tính khối lượng AgNO3 có thể tan trong 250 gam nước ở 25 độ C, biết độ tan của AgNO3 ở 25độ C là 222 gam
Tính khối lượng nguyên tố Cu trong 16g CuSO4
nCuSO4 = 16 / 160 = 0,1 mol
nCu = nCuSO4 = 0,1 mol
=> mCu = 0,1 x 64 = 6,4 gam
Đúng 0
Bình luận (0)
MCuSO4=64+4.16+32=160(g/mol)
•/•mCu=64:160.100•/• = 40 •/•
Suy ra: mCu=40•/• . 16=6,4
Đây là một cách khác nhưng mà dài hơn đấy
Đúng 0
Bình luận (0)
Trong tự nhiên copper có 2 đồng vị 63Cu chiếm 73% và 65Cu a)Tính khối lượng 63Cu trong 7.154g Cu2O b)Tính %m Cu trong CuSO4
`a)`
\(\%m_{^{65}Cu}=100-73=27\%\)
`->M_{Cu}={63.73+65.27}/{100}=63,54(g//mol)`
`n_{Cu_2O}={7,154}/{63,54.2+16}=0,05(mol)`
`->n_{Cu}=0,1(mol)`
\(\to m_{^{63}Cu}=0,1.63,54.73\%=4,63842(g)\)
`b)`
`\%m_{Cu}={63,54}/{63,54+32+16.4}.100\%\approx 39,827\%`
Đúng 2
Bình luận (0)
Ngâm 13g hỗn hợp gồm Zn và Cu trong dd CuSO4 dư. Phản ứng xong thu được chất rắn có khối lượng 12,84g. Thành phần % khối lượng của Cu trong hỗn hợp đầu là: A.98,77% B. 80% C.. 20% D. 1,23%
\(Zn+CuSO_4\to ZnSO_4+Cu\)
Đặt \(n_{Zn}=x(mol)\)
\(\Rightarrow m_{Zn(p/ứ)}-m_{Cu(p/ứ)}=65x-64x=13-12,84\\ \Rightarrow x=0,16(mol)\\ \Rightarrow \%_{Cu}=\dfrac{0,16.65}{13}.100\%=80\%\\ \Rightarrow B\)
Đúng 2
Bình luận (0)




























