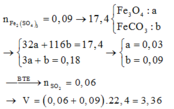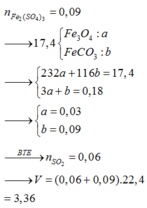Viết PTHH của phản ứng giữa dung dịch H2SO4 và muối Na2SO3, biết sản phẩm tạo thành là khí SO2, H2O và muối Na2SO4

Những câu hỏi liên quan
Cho a gam muối NaSO3 hòa tan vừa đủ vào dd H2SO4 24,5%.
a) Viết PTHH (đã làm: H2SO4 + Na2SO3 --> H2O + Na2SO4 + SO2)
b) Tính a
c) Tính khối lượng dung dịch H2SO4 biết rằng sau phản ứng thu được 3,36l SO2 ở đktc.
Cho 2,4g Mg vào dung dịch H2SO4 (sulfuric acid) nồng độ 1,5M (dư) ở nhiệt độ phòng. a. Viết PTHH của phản ứng, biết sản phẩm tạo thành gồm (MgSO4) và Khí Hydrogenb. Tính khối lượng muối MgSO4 thu được và thể tích khí hydrogen thu được ở đktc.c. Nếu giữ nguyên các điều kiện khác, chỉ tác động một trong các điều kiện sau đây thì tốc độ phản ứng thay đổi như thế nào (tăng lên, giảm xuống hay không đổi)? Giải thích?d. Thay dung dịch H2SO41,5M bằng dung dịch H2SO4 1Me. Thực hiệ...
Đọc tiếp
Cho 2,4g Mg vào dung dịch H2SO4 (sulfuric acid) nồng độ 1,5M (dư) ở nhiệt độ phòng.
a. Viết PTHH của phản ứng, biết sản phẩm tạo thành gồm (MgSO4) và Khí Hydrogen
b. Tính khối lượng muối MgSO4 thu được và thể tích khí hydrogen thu được ở đktc.
c. Nếu giữ nguyên các điều kiện khác, chỉ tác động một trong các điều kiện sau đây thì tốc độ phản ứng thay đổi như thế nào (tăng lên, giảm xuống hay không đổi)? Giải thích?
d. Thay dung dịch H2SO41,5M bằng dung dịch H2SO4 1M
e. Thực hiện phản ứng ở 55 độ C
Mọi người giúp mình với nhé !!![]()
\(a.Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ b.n_{Mg}=\dfrac{2,4}{24}=0,1mol\\ n_{MgSO_4}=n_{Mg}=0,1mol\\ m_{MgSO_4}=0,1.120=12g\)
c. Nếu thay bằng \(H_2SO_4\) 1M thì lượng Mg sẽ không ta hết.
Nếu Pứ ở \(55^0C\) thì pứ xảy ra nhanh hơn.
Đúng 1
Bình luận (0)
Cho Fe tác dụng hết với dung dịch H2SO4 đặc nóng thu được khí SO2 ( sản phẩm khử duy nhất) và 8,28 gam muối. Biết số mol Fe bằng 37,5% số mol H2SO4 phản ứng. Khối lượng Fe đã tham gia phản ứng là A. 2,52 gam B. 1,68 gam C. 1,12 gam D. 1,08 gam.
Đọc tiếp
Cho Fe tác dụng hết với dung dịch H2SO4 đặc nóng thu được khí SO2 ( sản phẩm khử duy nhất) và 8,28 gam muối. Biết số mol Fe bằng 37,5% số mol H2SO4 phản ứng. Khối lượng Fe đã tham gia phản ứng là
A. 2,52 gam
B. 1,68 gam
C. 1,12 gam
D. 1,08 gam.
2 Fe + 2n H2SO4 --> Fe2(SO4)n + n SO2 + n H2O
a------------an-----------0,5a
số mol Fe bằng 37,5% => a = 0,375*na => n = 2,667 khối lượng muối = 0,5a(56+96n) = 8,28 => a = 0,045 khối lượng Fe = 56*0,045 = 2,52
=> Đáp án A
Đúng 0
Bình luận (0)
Câu 3: Cho 3,36 lít khí SO2 (đktc) tác dụng với 300g dung dịch NaOH sau phản ứng chỉ tạo muối Na2SO3 và nước.
a) Viết phương trình hóa học.
b) Tính nồng độ phần trăm của dung dịch NaOH phản ứng.
c) Tính nồng độ phần trăm của dung dịch muối thu được sau phản ứng.
a) PTHH: SO2 + 2 NaOH -> Na2SO3 + H2O
b) Vì p.ứ chỉ tạo sp là muối Na2SO3 và H2O
=> nNaOH= 2.nSO2= 2. (3,36/22,4)= 0,3(mol)
=> mNaOH= 0,3.40=12(g)
=>C%ddNaOH= (12/300).100=4%
c) mddNa2SO3= mSO2 + mddNaOH= 0,15. 64+300= 309,6(g)
nNa2SO3=nSO2= 0,15(mol) => mNa2SO3= 0,15.126=18,9(g)
C%ddNa2SO3= (18,9/309,6).100=6,105%
Đúng 2
Bình luận (0)
Số mol của khí lưu huỳnh đioxit
nSO2 = \(\dfrac{V_{SO2}}{22,4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
a) Pt : SO2 + 2NaOH → Na2SO3 + H2O\(|\)
1 2 1 1
0,15 0,3 0,15
b) Số mol của natri hidroxit
nNaOH= \(\dfrac{0,15.2}{1}=0,3\left(mol\right)\)
Khối lượng của natri hidroxit
mNaOH = nNaOH . MNaOH
= 0,3 . 40
= 12 (g)
Nồng độ phần trăm của dung dịch natri hidroxit
C0/0NaOH = \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{12.100}{300}=4\)0/0
c) Số mol của muối natri sunfit
nNa2SO3 = \(\dfrac{0,3.1}{2}=0,15\left(mol\right)\)
Khối lượng của muối natri sunfit
mNa2SO3 = nNa2SO3 . MNa2SO3
= 0,15 . 126
= 18,9 (g)
Khối lượng của dung dịch sau phản ứng
mdung dịch sau phản ứng = mSO2 + mNaOH
= (0,15 . 64) + 300
= 309,6 (g)
Nồng độ phần trăm của muối natri sunfit
C0/0Na2SO3 = \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{18,9.100}{309,6}=6,1\)0/0
Chúc bạn học tốt
Đúng 0
Bình luận (0)
cho 44,2g hỗn hợp muối Na2SO3 và K2SO3 phản ứng với dung dịch H2SO4 20% thu được 6,72 lít khí (đktc)
a tính khối lượng dung dịch H2SO4 đủ phản ứng
b tính C% của dung dịch tạo thành sau phản ứng
c dẫn khí sinh ra vào 500 ml dd Ba ( OH )2 1M tính khối lượng muối thu được sau phản ứng
a, \(Na_2SO_3+H_2SO_4\rightarrow Na_2SO_4+SO_2+H_2O\)
\(K_2SO_3+H_2SO_4\rightarrow K_2SO_4+SO_2+H_2O\)
Ta có: \(n_{SO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: \(n_{H_2SO_4}=n_{SO_2}=0,3\left(mol\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{0,3.98}{20\%}=147\left(g\right)\)
b, Ta có: 126nNa2SO3 + 158nK2SO3 = 44,2 (1)
Theo PT: \(n_{SO_2}=n_{Na_2SO_3}+n_{K_2SO_3}=0,3\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Na_2SO_3}=0,1\left(mol\right)\\n_{K_2SO_3}=0,2\left(mol\right)\end{matrix}\right.\)
Có: m dd sau pư = 44,2 + 147 - 0,3.64 = 172 (g)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{Na_2SO_3}=\dfrac{0,1.126}{172}.100\%\approx7,33\%\\C\%_{K_2SO_3}=\dfrac{0,2.158}{172}.100\%\approx18,37\%\end{matrix}\right.\)
c, \(n_{Ba\left(OH\right)_2}=0,5.1=0,5\left(mol\right)\)
\(\Rightarrow\dfrac{n_{SO_2}}{n_{Ba\left(OH\right)_2}}=0,6< 1\) → Pư tạo BaSO3.
PT: \(SO_2+Ba\left(OH\right)_2\rightarrow BaSO_3+H_2O\)
\(n_{BaSO_3}=n_{SO_2}=0,3\left(mol\right)\Rightarrow m_{BaSO_3}=0,3.217=65,1\left(g\right)\)
Đúng 1
Bình luận (0)
Dùng 30g Na2SO3 cho vào 30g H2SO4 để điều chế SO2 biết ngoài SO2 còn sản phẩm là Na2SO4 và H2O.tính số g SO2 thu được sau phản ứng
\(n_{Na_2SO_3}=\dfrac{30}{126}=\dfrac{5}{21}\left(mol\right);n_{H_2SO_4}=\dfrac{30}{98}=\dfrac{15}{49}\left(mol\right)\)
PTHH: Na2SO3 + H2SO4 --> Na2SO4 + SO2 + H2O
Xét tỉ lệ \(\dfrac{\dfrac{5}{21}}{1}< \dfrac{\dfrac{15}{49}}{1}\) => Na2SO3 hết, H2SO4 dư
PTHH: Na2SO3 + H2SO4 --> Na2SO4 + SO2 + H2O
______\(\dfrac{5}{21}\)----------------------------------->\(\dfrac{5}{21}\)
=> \(m_{SO_2}=\dfrac{5}{21}.64=15,238\left(g\right)\)
Đúng 0
Bình luận (0)
\(Na_2SO_3+H_2SO_4\rightarrow SO_2+Na_2SO_4+H_2O\)
Đúng 0
Bình luận (0)
). Dẫn 112 ml khí SO2 (đktc) đi qua 700 ml dung dịch Ca(OH)2 có nồng độ 0,01M, sản phẩm thu được là muối sunfit và nước.
a. Viết PTHH xảy ra?
b. Tính khối lượng các chất sau phản ứng?
\(a,PTHH:SO_2+Ca(OH)_2\to CaSO_3\downarrow+H_2O\\ b,n_{Ca(OH)_2}=0,7.0,01=0,007(mol)\\ n_{SO_2}=\dfrac{0,112}{22,4}=0,005(mol)\)
Vì \(\dfrac{n_{SO_2}}{1}<\dfrac{n_{Ca(OH)_2}}{1}\) nên \(Ca(OH)_2\) dư
\(\Rightarrow n_{CaSO_3}=n_{H_2O}=0,005(mol)\\ \Rightarrow m_{CaSO_3}=0,005.120=0,6(g)\\ m_{H_2O}=0,005.18=0,09(g)\)
Đúng 4
Bình luận (0)
Hòa tan hết 17,4 gam hỗn hợp gồm
F
e
3
O
4
và
F
e
C
O
3
trong dung dịch
H
2
S
O
4
đặc, nóng dư. Kết thúc phản ứng thu được dung dịch X chứa 36,0 gam muối và V lít (đktc) hỗn hợp khí Y. Biết khí
S
O
2
là s...
Đọc tiếp
Hòa tan hết 17,4 gam hỗn hợp gồm F e 3 O 4 và F e C O 3 trong dung dịch H 2 S O 4 đặc, nóng dư. Kết thúc phản ứng thu được dung dịch X chứa 36,0 gam muối và V lít (đktc) hỗn hợp khí Y. Biết khí S O 2 là sản phẩm khử duy nhất của S 6 + Giá trị của V là
A. 3,36 lít
B. 2,688 lít
C. 8,064 lít
D. 2,016 lít
1.viết PTHH của các phản ứng nhiệt phân các muối sau:a,MgCO3;BaCO3(biết sản phẩm phản ứng là oxit kim loại và khí CO2)b,NaNO3,KNO3(biết sản phẩm phản ứng là muối nitrit kim loại và khí oxi)c,Mg(NO3)2;Cu(NO3)2;Pb(NO3)2 (biết sản phẩm phản ứng là oxit kim loại,nito đioxit và oxi)
Đọc tiếp
1.viết PTHH của các phản ứng nhiệt phân các muối sau:
a,MgCO3;BaCO3(biết sản phẩm phản ứng là oxit kim loại và khí CO2)
b,NaNO3,KNO3(biết sản phẩm phản ứng là muối nitrit kim loại và khí oxi)
c,Mg(NO3)2;Cu(NO3)2;Pb(NO3)2 (biết sản phẩm phản ứng là oxit kim loại,nito đioxit và oxi)
Hòa tan hết 17,4 gam hỗn hợp gồm Fe3O4 và FeCO3 trong dung dịch H2SO4 đặc, nóng dư. Kết thúc phản ứng thu được dung dịch X chứa 36,0 gam muối và V lít (đktc) hỗn hợp khí Y. Biết khí SO2 là sản phẩm khử duy nhất của S+6. Giá trị của V là A. 3,36 lít B. 2,688 lít C. 8,064 lít D. 2,016 lít
Đọc tiếp
Hòa tan hết 17,4 gam hỗn hợp gồm Fe3O4 và FeCO3 trong dung dịch H2SO4 đặc, nóng dư. Kết thúc phản ứng thu được dung dịch X chứa 36,0 gam muối và V lít (đktc) hỗn hợp khí Y. Biết khí SO2 là sản phẩm khử duy nhất của S+6. Giá trị của V là
A. 3,36 lít
B. 2,688 lít
C. 8,064 lít
D. 2,016 lít