Cho 10,8 l khí Cl2 ở đktc TD với m(g) Cu. Sau PỨ thu được 63.9g chất rắn
a, Chất nào hết , dư
b, Tinh m và % klg các chất sau PỪ
giúp vvs!!!!!!!!!!!!
Cho 10, 8 lít khí Cl ở đktc tác dụng với m (g) Cu. Sau phản ứng thu được 63,9 g
chất rắn. a) Chất nào phản ứng hết? Chất nào còn dư? b) Tính m và phần trăm khối lượng các chất sau phản ứng
Cu+Cl2->CuCl2
Bài này cũng dễ mà sao bạn cho số không đẹp tí nào zậy, rắc rối
Cho 10,8 l khí Cl ở đktc tắc dụng với m (g) Cu. Sau phản ứng thu được 63.9 g chất rắn.
a)Chất nào phản ứng hết? chất nào còn dư?
b)Tính m và phần trăm khối lượng các chất sau phản ứng.
PTHH: Cu + Cl2 -to-> CuCl2
Ta có: \(n_{Cl_2}=\frac{10,8}{22,4}\approx0,482\left(mol\right)\\ n_{CuCl_2}=\frac{63,9}{135}\approx0,473\left(mol\right)\)
Theo PTHH và đề bài, ta có:
\(\frac{0,482}{1}>\frac{0,473}{1}\)
=> Cl2 dư , Cu hết nên tính theo nCu
Theo PTHH và đề bài, ta có:
\(n_{CuCl_2}=n_{Cu}=0,473\left(mol\right)\)
b) Khối lượng CuCl2:
\(m_{CuCl_2}=0,473.135=63,855\left(g\right)\)
=> \(\%Cu=\frac{64}{135}.100=47,407\%\)
\(\%Cl=100\%-47,407\%=52,593\%0\)
cho 24,32 g hh E C2H7O2N và CH6N2O3 vào dd NaOH đung nóng dư, sau khi kết thúc pứ thấy xuất hiện a mol khí X duy nhất có khả năng đổi màu quỳ tím và dd chứa các hợp chất vô cơ . cô cạn Y , nung tới klg ko đổi thấy chất rắn giảm 2,24 g. sục a mol khí X và dd AlCl3 dư thu kết tủa m gam. m=? giúp mình với !!!
Cho 15,2g hh gồm Na, Al, Mg tác dụng hết với H2O dư thu được 4,48 l khí ở đktc và chất rắn A. Lấy chất rắn A tác dụng hết 300 ml dd CuSO4 2M được 32g đồng kim loại. Tính khối lượng mỗi kim loại có trong pứ ban đầu. Cho các pứ xảy ra hoàn toàn.
Cho 12,48 gam X gồm Cu và Fe tác dụng hết với 0,15 mol hỗn hợp khí gồm Cl2 và O2, thu được chất rắn Y gồm các muối và oxit. Hòa tan vừa hết Y cần dùng 360 ml dung dịch HCl 1M, thu được dung dịch Z. Cho dung dịch AgNO3 dư vào Z, thu được 75,36 gam chất rắn. Mặt khác, hòa tan hết 12,48 gam X trong dung dịch HNO3 nồng độ 31,5%, thu được dung dịch T và 3,36 lít khí NO (sản phẩm khử duy nhất, ở đktc). Nồng độ % của Fe(NO3)3 trong T gần nhất với giá trị nào sau đây?
A. 7,28.
B. 5,67.
C. 6,24.
D. 8,56.
Chọn B
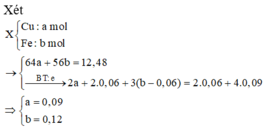
Khi cho X tác dụng với HNO3 thu được dung dịch T gồm Fe(NO3)2 (x); Fe(NO3)3 (y); Cu(NO3)2 (0,09).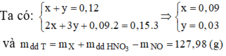
Vậy C% Fe(NO3)3 = 5,67%
Cho 12,48 gam X gồm Cu và Fe tác dụng hết với 0,15 mol hỗn hợp khí gồm Cl2 và O2, thu được chất rắn Y gồm các muối và oxit. Hòa tan vừa hết Y cần dùng 360 ml dung dịch HCl 1M, thu được dung dịch Z. Cho dung dịch AgNO3 dư vào Z, thu được 75,36 gam chất rắn. Mặt khác, hòa tan hết 12,48 gam X trong dung dịch HNO3 nồng độ 31,5%, thu được dung dịch T và 3,36 lít khí NO (sản phẩm khử duy nhất, ở đktc). Nồng độ % của Fe(NO3)3 trong T gần nhất với giá trị nào sau đây?
A. 7,28
B. 5,67
C. 6,24
D. 8,56
1, Cho 10,8 (g) bột nhôm vào 200(g) dung dịch HCl 27,375% được dung dịch A và V(l) khí B ở đktc.
a, Lập PTHH
b, Tính VB
c, Tính C% của chất tan có trong dung dịch A
2, Đốt cháy hoàn toàn 12,6(g) hỗn hợp X gồm S và P với khí O2. Sau phản ứng thu được 4,48(l) khí O2 ở đktc.
a, Lập PTHH xảy ra.
b, Tính khối lượng chất rắn sau phản ứng.
c, Tính %m mỗi chất rắn trong X.
Mình cần gấp lắm, mọi người giúp mình với!
câu 1: nAl=0,4 mol
mHCL=54,75g=> nHCl=1,5 mol
PTHH: 2Al+6HCl=> 2AlCl3+3H2
0,4mol: 1,5mol => nHCl dư theo nAl
0,4mol-->1,2 mol-->0,4mol-->0,6mol
thể tích H2 là V=0,6.22,4=13,44ml
b) theo định luật btoan khối lượng ta có : mAlCl3=200+10,8-0,6.2=209,6g
m AlCl3=0,4.(27+35,5.3)=53,4g
=> C% AlCl3= 25,48%
PTHH: 2Al + 6HCl → 2AlCl3 + 3H2 ↑
Khối lượng chất tan HCl là:
200 . 27,375% = 54,75(gam)
Số mol của HCl là: 54,75 : 36,5 = 1,5 (mol)
Số mol của Al là: 10,8 : 27 = 0,4 (mol)
So sánh: \( {0,4{} \over 2}\) < \({1,5} \over 6\)
=> HCl dư, tính theo Al
Số mol của khí hiđrô sinh ra là: 0,4 . \(3 \ \over 2\) = 0,6 (mol)
V= 0,6 . 22,4 = 13,44 (lít)
Sau đó áp dụng định luật bảo toàn khối lượng để tính khối lượng dung dịch A:
Khối lượng nhôm + Khối lượng dung dịch axit
= Khối lượng dung dịch A + khối lượng khí hiđrô
<=> Khối lượng dung dịch A là:
10,8 + 200 - 0,6 . 2 = 209,6 (gam)
Khối lượng chất tan AlCl3 trong dung dịch A là:
0,4 . 133,5 = 53,4 (gam)
C% chất tan trong dung dịch A là:
( 53,4 : 209,6 ) . 100% = 25,48%
hỗn hợp gồm Al, Al2O3 và Cu nặng 10 g. Nếu hòa tan hoàn toàn hỗn hợp bằng axit HCl dư thì thu được 3,36 dm3 khí (đktc); dd B và chất răn A. Đem nung nóng A trong không khí đến khối lượng không đổi thu được chất rắn D cân nặng 2,75g. tính % klg mỗi chất trong hh
giải giúp mik với
2Al+6HCl---->2AlCl3+3H2
Al2o3+6HCl--->2AlCl3+3H2O
Cu+HCl--> không p/u
2Cu + O2---->2CuO
ncuO=2,75/80=0.034375(mol)
Cứ 2 mol Cu---à 2 mol CuO
0.034375<------0.034375
mCu=0,034375.64=2,2(g)
--->%mCu=2,2.100/10=22%
nH2=3,36/22,4=0,15(mol)
cứ 2 mol Al----->3 mol H2
0.1<-----0.15
mAl :0,1.27=2.7(g)
--->%mAl=2,7.100/10=27%
---->%mAl2o3=100%-27%-22%=51%
Nung 31,6 gam KMNO4 một thời gian thu được khí oxi và 26,8 gam chất rắn . Toàn bộ khí oxi sinh ra cho pứ hết với m gam hỗn hợp X gồm Fe và Cu thu được 26 gam chất rắn Y . Tính giá trị m ? Giúp em với ạ
Khi nhiệt phân KMnO4, phần khí O2 sinh ra bay hơi nên lượng chất rắn còn lại gồm KMnO4 dư, K2MnO4 và MnO2. Dựa vào định luật bảo toàn khối lượng dễ dàng tìm được khối lượng O2. Xét sự thay đổi số oxi hóa của các nguyên tố trong toàn bộ quá trình, chỉ có Mn, O và Cl thay đổi số oxi hóa. Dựa vào định luật bảo toàn electron với số mol Mn và O đã biết ta suy ra được số mol electron Cl- đã nhận.
Chất rắn bao gồm K2MnO4 và MnO2
BTKL:
Khi cho chất rắn phản ứng với HCl sẽ xảy ra phản ứng oxi hóa – khử.
Khí X chính là Cl2.
Sử dụng định luật bảo toàn electron cho toàn bộ quá trình, ta có các bán phản ứng:
Phản ứng điều chế clorua vôi CaOCl2:
Khối lượng clorua vôi theo lý thuyết:
Clorua vôi này chứa 30% tạp chất tức là clorua vôi nguyên chất chỉ chiếm 70%.
Khối lượng clorua vôi thực tế thu được: