Dẫn 10 lít hỗn hợp khí \(\)CO và \(SO_2\) qua dung dịch \(Ba\left(OH\right)_2\) dư. Sau hản ứng thu được 81,375 gam kết tủa. Tính thành phần% theo thể tích mỗi khí trong hỗn hợp ban đầu?(Biết thể tích các khí đo ở (đktc)

Những câu hỏi liên quan
3. Dẫn 10 lít hỗn hợp khí CO và SO2 qua dung dịch Ba(OH)2 dư. Sau phản ứng thu được 81,375gam kết tủa. Tính thành phần % theo thể tích mỗi khí trong hỗn hợp ban đầu? (Biết thể tích cáckhí đo ở đktc).
Đọc tiếp
3. Dẫn 10 lít hỗn hợp khí CO và SO2 qua dung dịch Ba(OH)2 dư. Sau phản ứng thu được 81,375
gam kết tủa. Tính thành phần % theo thể tích mỗi khí trong hỗn hợp ban đầu? (Biết thể tích các
khí đo ở đktc).
![]()
![]()
nBaSO3 = \(\dfrac{81,375}{217}=0,375\left(mol\right)\)
Pt: SO2 + Ba(OH)2 --> BaSO3 + H2O
0,375 mol<------------0,375 mol
% VSO2 = \(\dfrac{0,375\times22,4}{10}.100\%=84\%\)
% VCO = 100% - 84% = 16%
Đúng 0
Bình luận (0)
Dẫn luồng khí CO dư đi qua 20,05 gam hỗn hợp hai oxit ZnO và
F
e
2
O
3
ở nhiệt độ cao, thu được hỗn hợp hai kim loại và khí
C
O
2
. Dẫn khí
C
O
2
sinh ra vào dung dịch
C
a
(
O
H
)
2
dư, thu được 35 gam kết tủa.Viết phản ứng xảy ra.Tính khối...
Đọc tiếp
Dẫn luồng khí CO dư đi qua 20,05 gam hỗn hợp hai oxit ZnO và F e 2 O 3 ở nhiệt độ cao, thu được hỗn hợp hai kim loại và khí C O 2 . Dẫn khí C O 2 sinh ra vào dung dịch C a ( O H ) 2 dư, thu được 35 gam kết tủa.
Viết phản ứng xảy ra.
Tính khối lượng mỗi kim loại tạo thành.
Tính thành phần phần trăm theo khối lượng mỗi oxit trong hỗn hợp ban đầu.
Dẫn 2,24 lít hỗn hợp gồm khí metan và etilen qua dung dịch brom ( lấy dư ), sau khi phản ứng kết thúc thấy 6,4 gam brom tham gia phản ứng.
a. Tính thể tích từng khí trong hỗn hợp ban đầu.
b. Tính thành phần % về thể tích của từng khí trong hỗn hợp đầu.
Biết ( H = 1 ; C = 12 ; Br = 80 ) (các khí đo ở đktc ). CẢM ƠN MỌI NGƯỜI ❤
\(a,n_{Br_2}=\dfrac{6,4}{160}=0,04\left(mol\right)\)
PTHH: C2H4 + Br2 ---> C2H4Br2
0,04<---0,04
\(\rightarrow\left\{{}\begin{matrix}V_{C_2H_4}=0,04.22,4=0,896\left(l\right)\\V_{CH_4}=2,24-0,896=1,344\left(l\right)\end{matrix}\right.\\ b,\rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,896}{2,24}.100\%=40\%\\\%V_{CH_4}=100\%-40\%=60\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Bài 3: Đốt cháy hết 11,2 lít (đktc) hỗn hợp gồm Metan và Axetilen, cho sản phẩm qua dung dịch Ca(OH)2 dư thu được 80g kết tủa. Tính thành phần phần trăm thể tích mỗi chất khí trong hỗn hợp ban đầu.
\(n_{hh}=\dfrac{11,2}{22,4}=0,5mol\)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=x\\n_{C_2H_2}=y\end{matrix}\right.\)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
x x ( mol )
\(2C_2H_2+5O_2\rightarrow\left(t^o\right)4CO_2+2H_2O\)
y 2y ( mol )
\(n_{CaCO_3}=\dfrac{80}{100}=0,8mol\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
0,8 0,8 ( mol )
Ta có:
\(\left\{{}\begin{matrix}x+y=0,5\\x+2y=0,8\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,3\end{matrix}\right.\)
\(\%V_{CH_4}=\dfrac{0,2}{0,5}.100=40\%\)
\(\%V_{C_2H_2}=100\%-40\%=60\%\)
Đúng 2
Bình luận (0)
Gọi a (mol) và b (mol) lần lượt là số mol của khí metan (CH4) và khí axetilen (C2H2).
Giả thiết: a+b=11,2/22,4=0,5 (1).
Số mol kết tủa CaCO3 là 80/100=0,8 (mol) bằng số mol sản phẩm khí CO2 (do dung dịch Ca(OH)2 dư).
Ta có: a+2b=0,8 (2).
Giải hệ phương trình gồm (1) và (2), ta suy ra a=0,2 (mol) và b=0,3 (mol).
Thành phần phần trăm thể tích mỗi chất khí trong hỗn hợp ban đầu:
%Vmetan=0,2/0,5.100%=40%, suy ra %Vaxetilen=100%-40%=60%.
Đúng 0
Bình luận (0)
Dẫn 6,72 lit hỗn hợp khí X gồm propan, etilen và axetilen đi qua dung dịch brom dư, thấy còn 1,68 lít khí không hấp thụ. Nếu dẫn 6,72 lit hỗn hợp khí X trên qua dung dịch AgNO3/NH3 thấy có 24,24 gam kết tủa. Các thể tích khí đo ở đktc. Tính thành phần phần trăm theo thể tích và theo khối lượng của mỗi khí trong hỗn hợp.
1,68 lit khí không bị dung dịch Br2 hấp thụ là propan
![]()
![]()
![]()
![]()
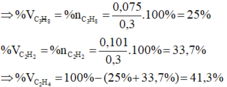
![]()
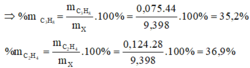
![]()
Đúng 1
Bình luận (0)
Cho 10 lít (đktc) hỗn hợp khí gồm N2 và CO2 tác dụng với 2 lít dung dịch Ca(OH)2 0,02 mol/l thu được 1 gam kết tủa. Thành phần % theo thể tích N2 trong hỗn hợp ban đầu là: A. 2,24% hoặc 84,32% B. 2,24% hoặc 15,68% C. 15,68% hoặc 97,76% D. 84,32% hoặc 97,76%
Đọc tiếp
Cho 10 lít (đktc) hỗn hợp khí gồm N2 và CO2 tác dụng với 2 lít dung dịch Ca(OH)2 0,02 mol/l thu được 1 gam kết tủa. Thành phần % theo thể tích N2 trong hỗn hợp ban đầu là:
A. 2,24% hoặc 84,32%
B. 2,24% hoặc 15,68%
C. 15,68% hoặc 97,76%
D. 84,32% hoặc 97,76%
Đáp án D
Ta có nCa(OH)2= 2.0,02= 0,04 mol; nCaCO3= 1/100= 0,01 mol
Ta có nCa(OH)2 > nCaCO3 nên có 2 trường hợp:
- TH1: Ca(OH)2 dư
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
Theo PT (1): nCaCO3= nCO2= 0,01 mol →VCO2=0,01.22,4=0,224 lít
→%VCO2= 2,24%→ %VN2= 100%- 2,24%=97,76%
- TH2: Ca(OH)2 phản ứng hết:
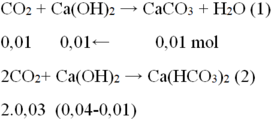
Ta có: nCO2= 0,01+ 2.0,03= 0,07 mol →VCO2= 0,07.22,4=1,568 lít
→%VCO2= 15,68%→ %VN2= 100%- 15,68%=84,32%
Đúng 0
Bình luận (0)
Dẫn 13,56 lít hỗn hợp 2 khí metan và etylen qua bình đựng dung dịch brom dư sao cho phản ứng xảy ra hoàn toàn , chất khí sau phản ứng đem đốt dẫn toàn bộ khí thu được qua vôi trong dư tạo thành 40g chất không tan màu trắng . Tính thành phần phần trăm theo thể tích của mỗi khí có trong hỗn hợp ban đầu .
Cho hỗn hợp qua dung dịch brom dư
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Khí thoát ra là \(CH_4\)
\(CH_4+2O_2\rightarrow^{t^o}CO_2+2H_2O\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
Ta có:
\(n_{CaCO_3}=\frac{40}{100}=0,4mol=n_{CO_2}=n_{CH_4}\)
\(\rightarrow V_{CH_4}=0,4.22,4=8,96l\)
\(\rightarrow\%V_{CH_4}=\frac{8,96}{13,56}=66\%\rightarrow\%V_{C_2H_4}=34\%\)
Cho 5,6 lít hỗn hợp X gồm hai khí CO và CO2 đi qua than nóng đỏ (không có không khí) thu được 7,0 lít hỗn hợp khí Y. Dẫn Y đi qua dung dịch canxi hiđroxit dư thì thu được 6,25 gam kết tủa. Biết các thể tích khí đó ở điều kiện tiêu chuẩn, các phản ứng xảy ra hoàn toàn. Phần trăm thể tích khí CO2 trong hỗn hợp X và Y tương ứng là A. 25% và 25%. B. 50% và 20%. C. 50% và 25%. D. 25% và 20%.
Đọc tiếp
Cho 5,6 lít hỗn hợp X gồm hai khí CO và CO2 đi qua than nóng đỏ (không có không khí) thu được 7,0 lít hỗn hợp khí Y. Dẫn Y đi qua dung dịch canxi hiđroxit dư thì thu được 6,25 gam kết tủa. Biết các thể tích khí đó ở điều kiện tiêu chuẩn, các phản ứng xảy ra hoàn toàn. Phần trăm thể tích khí CO2 trong hỗn hợp X và Y tương ứng là
A. 25% và 25%.
B. 50% và 20%.
C. 50% và 25%.
D. 25% và 20%.
Đáp án B
Khi cho CO và CO2 qua than nóng đỏ dó phản ứng:
CO2 + C → 2CO ⇒ Số mol hỗn hợp tăng lên chính là số mol CO2 đã tham gia phản ứng.
⇒ nCO2 đã pứ = (7 – 5,6) ÷ 22,4 = 0,0625 mol.
Số mol CO2 còn lại = nCaCO3 = 6,25 ÷ 100 = 0,0625 mol.
⇒ nCO2 ban đầu = 0,0625 + 0,0625 = 0,125 mol.
Tóm lại nCO2/X = 0,125 mol và nCO2/Y = 0,0625
Đúng 0
Bình luận (0)
Cho 5,6 lít hỗn hợp X gồm hai khí CO và CO2 đi qua than nóng đỏ (không có không khí) thu được 7,0 lít hỗn hợp khí Y. Dẫn Y đi qua dung dịch canxi hiđroxit dư thì thu được 6,25 gam kết tủa. Biết các thể tích khí đó ở điều kiện tiêu chuẩn, các phản ứng xảy ra hoàn toàn. Phần trăm thể tích khí CO2 trong hỗn hợp X và Y tương ứng là A. 25% và 25%. B. 50% và 20%. C. 50% và 25%. D. 25% và 20%.
Đọc tiếp
Cho 5,6 lít hỗn hợp X gồm hai khí CO và CO2 đi qua than nóng đỏ (không có không khí) thu được 7,0 lít hỗn hợp khí Y. Dẫn Y đi qua dung dịch canxi hiđroxit dư thì thu được 6,25 gam kết tủa. Biết các thể tích khí đó ở điều kiện tiêu chuẩn, các phản ứng xảy ra hoàn toàn. Phần trăm thể tích khí CO2 trong hỗn hợp X và Y tương ứng là
A. 25% và 25%.
B. 50% và 20%.
C. 50% và 25%.
D. 25% và 20%.
Đáp án B
Khi cho CO và CO2 qua than nóng đỏ dó phản ứng:
CO2 + C → 2CO ⇒ Số mol hỗn hợp tăng lên chính là số mol CO2 đã tham gia phản ứng.
⇒ nCO2 đã pứ = (7 – 5,6) ÷ 22,4 = 0,0625 mol.
Số mol CO2 còn lại = nCaCO3 = 6,25 ÷ 100 = 0,0625 mol.
⇒ nCO2 ban đầu = 0,0625 + 0,0625 = 0,125 mol.
Tóm lại nCO2/X = 0,125 mol và nCO2/Y = 0,0625
Đúng 0
Bình luận (0)



















