để trung hòa lượng axit béo tự do có trong 14g một mẫu chất béo cần 15 ml đ KOH 0,1M. Chỉ số axit maauc chất béo trên là
giúp em giải bài này vs: m(KOH)=0,015*0,1*56000=84g
56000 là từ đâu ra, giúp e giải thác mắc. e cám ơn thầy cô nhiều
Để đánh giá lượng axit béo tự do trong chất béo người ta dùng chỉ số axit. Đó là số miligam KOH cần dùng để trung hòa lượng axit béo tự do có trong 1 gam chất béo . Để trung hòa 14g một chất béo cần 15 ml dung dịch KOH 0,1M. Chỉ số axit của chất béo đó là :
A. 5,6
B. 6,0
C. 7,0
D. 6,5
Đáp án : B
nKOH = 0,0015 mol => mKOH = 0,084g = 84 mg
=> Chỉ số axit = 6,0
Trong chất béo luôn có một lượng nhỏ axit tự do. Số miligam KOH dùng trung hòa lượng axit tự do trong 1 gam chất béo gọi là chỉ số axit của chất béo. Để trung hòa 2,8 gam chất béo cần 3,0 ml dung dịch KOH 0,1 M. Tính chỉ số axit của mẫu chất béo trên.
Số mol KOH là: nKOH = 0,003. 0,1 = 0,0003 (mol)
Khối lượng KOH cần dùng là mKOH = 0,0003.56 = 0,0168 (g) = 16,8 (mg)
Trung hòa 2,8 gam chất béo cần 16,8 mg KOH
⇒ Trung hòa 1 gam chất béo cần x mg KOH
⇒ x = 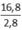 = 6
= 6
Vậy chỉ số axit của mẫu chất béo trên là 6.
Để trung hòa lượng axit tự do có trong 14 gam một mẫu chất béo cần 15 ml dung dịch KOH 0,1M. Chỉ số axit của mẫu chất béo trên là:
A. 7,2
B. 4,8
C. 6,0
D. 5,5
Đáp án C
Chỉ số axit = (0,0015×56×1000)/14=6,0
Trong chất béo luôn có một lượng nhỏ axit tự do. Số miligam KOH dùng để trung hoà lượng axit tự do trong 1 gam chất béo gọi là chỉ số axit của chất béo. Để trung hoà 2,8 gam chất béo cần 3,0 ml dung dịch KOH 0,1 M. Tính chỉ số axit của mẫu chất béo trên.
\(n_{H^+}=n_{OH^-}=0,003.0,1=3.10^{-4}\left(mol\right)\)
\(m_{KOH}=3.10^{-4}.56=0,0168\left(g\right)\)
\(0,0168\left(g\right)KOH\rightarrow2,8\left(g\right)chấtbeo\\ x\left(g\right)KOH\rightarrow1\left(g\right)chấtbeo\)
=> \(x=\dfrac{0,0168.1}{2,8}=6,10^{-3}\left(g\right)=6\left(miligam\right)\)
Vậy chỉ số của mẫu axit trên là 6
nKOH = 0,003. 0,1 = 0,0003 (mol)
mKOH = 0,0003.56 = 0,0168 (g) = 16,8 (mg)
Trung hòa 2,8 gam chất béo cần 16,8 mg KOH
⇒ Trung hòa 1 gam chất béo cần x mg KOH
⇒ x = 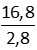
Chất béo luôn có một lượng nhỏ axit tự do. Số miligam KOH dùng để trung hòa lượng axit tự do trong một gam chất béo gọi là chỉ số axit của chất béo. Để trung hòa 2,8 gam chất béo cần 3,0 ml dung dịch KOH 0,1M. Tính chỉ số axit của mẫu chất béo trên.
Trong chất béo luôn có 1 lưownvj nhỏ axit tự do . Số kilôgam KOH dùng để trung hoà lượng axit tự do trong 1g chất béo gọi là chỉ số axit của chất béo. Để trung hoà 2,8g chất béo cần 3,0ml dd KOH 0,1M. Tính chỉ số axit của mẫu chất béo trên?
Để trung hòa lượng axit tự do có trong 14 gam một mẫu chất béo cần 15ml dung dịch KOH 0,1M. Chỉ số axit của mẫu chất béo trên là (Cho H = 1; O = 16; K = 39)
nKOH=15/1000.0,1=1,5.10^(-3) mol
=>mKOH=1,5.10^(-3).56=0,084g
Chỉ số axit là số mg KOH để trung hòa hết axit tự do trong 1g chất béo
Theo đề bài trung hòa axit trong 14g chất béo cần 0,084 gam KOH
=>trung hòa 1 gam chất béo cần 0,006 gam KOH=6mg KOH
Chỉ số axit=6
Muốn trung hòa 14 gam một chất béo X cần 15 ml dung dịch KOH 0,1M. Hãy tính chỉ số axit của chất béo X và khối lượng KOH cần để trung hòa 10 gam chất béo X có chỉ số axit bằng 5,6 ?
A. 5 và 14 mg KOH
B. 6 và 56 mg KOH
C. 6 và 28 mg KOH
D. 4 và 26 mg KOH
Chọn đáp án B
nKOH = 1,5 (mmol) → mKOH = 84 (mg)
→ Để trung hòa 1 gam chất béo cần 6 (mg) KOH → chỉ số axit của chất béo trên là 6.
Khối lượng KOH cần = 10 × 5,6 = 56 (mg)
Để trung hòa lượng axit tự do có trong 140 gam một mẫu chất béo cần 150ml dung dịch NaOH 0,1M. Chỉ số của mẫu chất béo trên là
A.4,8
B.7,2
C.6,0
D.5,5