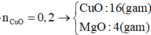Đem nung 6,66g hh X (2 hidroxit của nhôm và kẽm) sau khi phản ứng xảy ra xong thấy khối lượng chất rắn đem nung giảm đi 1,98g. Tính thành phần % khối lượng hh hidroxit?

Những câu hỏi liên quan
Cho m gam hh bột Cu và Mg chia hh thành 2 phần bằng nhau:
- phần 1 đem nung nóng ngoài kk đến khi phản ứng xảy ra hoàn toàn thì thấy khối lượng hh tăng thêm 8g
- phần 2 đem hoà tan trong dd HCL dư thấy thoát ra 3,36 lít khí H2 ở đktc.tìm m
Giả sử: \(\left\{{}\begin{matrix}n_{Cu}=x\left(mol\right)\\n_{Mg}=y\left(mol\right)\end{matrix}\right.\) (trong 1 phần)
_ Phần 1:
PT: \(2Cu+O_2\underrightarrow{t^o}2CuO\)
\(2Mg+O_2\underrightarrow{t^o}2MgO\)
Ta có: m hỗn hợp tăng = mO2 \(\Rightarrow n_{O_2}=\dfrac{8}{32}=0,25\left(mol\right)\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{Cu}+\dfrac{1}{2}n_{Mg}=\dfrac{1}{2}x+\dfrac{1}{2}y\left(mol\right)\)
\(\Rightarrow x+y=0,5\left(1\right)\)
_ Phần 2: Cu không tác dụng với dd HCl.
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
Ta có: \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Mg}=y\left(mol\right)\)
⇒ y = 0,15 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,35\left(mol\right)\\y=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m=2.\left(0,35.64+0,15.24\right)=52\left(g\right)\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (1)
Nung 2,22g hh A gồm Fe2O3,MgO,Al2O3 ,trong dòng khí CO dư đến khi phản ứng hoàn toàn .Thấy chất rắn còn lại có khối lượng 1,98g (Chất rắn B).Hòa tan hoàn toàn 1,98g chất rắn B này cần dùng 100ml dd HCl 1M
a/Viết các phương trình xảy ra
b/Tính thành phần phần trăm khối lượng mỗi chất rắn trong hh A
GIÚP MÌNH VỚI Ạ!!!!MÌNH ĐANG CẦN RẤT RẤT GẤPPP
\(a/Fe_2O_3+3CO\xrightarrow[]{t^0}2Fe+3CO_2\\ MgO+CO\xrightarrow[]{t^0}Mg+CO_2\\ Al_2O_3+3CO\xrightarrow[]{t^0}2Al+3CO_2\\ Fe+2HCl\rightarrow FeCl_2+H_2\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
\(b/n_{HCl}=0,1.1=0,1mol\\ n_{Fe_2O_3}=a\\ n_{MgO}=n_{Mg}=b\\ n_{Al_2O_3}=c\\ n_{Fe}=2a\\ \Rightarrow\left\{{}\begin{matrix}160a+40b+102c=2,22\\56a+24b+27c=1,98\\2.2a+2b+6c=0,1\end{matrix}\right.\\ \Rightarrow a=\)
đến đây số mol ra âm bạn coi lại đề nhé
Đúng 0
Bình luận (1)
Nung 18g rắn nhôm hidroxit được 10,2g rắn nhôm oxit (2 nguyên tố Al, O) và 5,4g H2O.
a) Lập PTHH
b) Tính khối lượng chất rắn bị nung
c) Tính khối lượng chất rắn sau phản ứng
PTHH: \(2Al\left(OH\right)_3\xrightarrow[]{t^o}Al_2O_3+3H_2O\)
Tính theo sản phẩm
Ta có: \(n_{Al_2O_3}=\dfrac{10,2}{102}=0,1\left(mol\right)\) \(\Rightarrow n_{Al\left(OH\right)_3\left(p.ứ\right)}=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Al\left(OH\right)_3\left(p.ứ\right)}=0,2\cdot78=15,6\left(g\right)\\m_{Al\left(OH\right)_3\left(dư\right)}=18-15,6=2,4\left(g\right)\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Nung 27,2 gam hỗn hợp sắt (III) hidroxit và magie hidroxit đến khi phản ứng hoàn toàn thấy khối lượng chất rắn thu được giảm 7,2 gam so với khối lượng hidroxit ban đầu. Tính khối lượng chất rắn tạo thành và phần trăm khối lượng mỗi hidroxit.
Gọi số mol Fe(OH)3, Mg(OH)2 là a,b (mol)
PTHH: \(2Fe\left(OH\right)_3\underrightarrow{t^o}Fe_2O_3+3H2O\)
________a ------------> 0,5a____________(mol)
\(Mg\left(OH\right)_2\underrightarrow{t^o}MgO+H_2O\)
b-----------------> b_________(mol)
=> \(\left\{{}\begin{matrix}107a+58b=27,2\\160.0,5a+40b=27,2-7,2\end{matrix}\right.\) => \(\left\{{}\begin{matrix}a=0,2\left(mol\right)\\b=0,11\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}m_{Fe\left(OH\right)_3}=0,2.107=21,4\\m_{Mg\left(OH\right)_2}=0,1.58=5,8\left(g\right)\\m_{Fe_2O_3}=160.0,5.0,2=16g\\m_{MgO}=40.0,1=4\left(g\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%m_{Fe\left(OH\right)_3}=\frac{21,4}{27,2}.100\%=78,68\%\\\%m_{Mg\left(OH\right)_2}=\frac{5,8}{27,2}.100\%=21,32\%\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Nung nóng 165 hh X gồm Mg(oh)2 va Fe(OH)3 đến khối lượng ko đổi ,thấy kl hh giảm 45 g va thu đưuọc chất rắn Y.
a)xác định thành phần % khối lượng mỗi hidroxit có trong hh
b) cho Y vào đ HCl 14,6% (D=1,15g/ml) thì cần mấy ml dd để hòa tan hết lượng Y trên
a) Đặt a=nMg(OH)2 ; b=nFe(OH)3 (a,b>0)
PTHH: Mg(OH)2 -to-> MgO + H2O
a______________a(mol)
2 Fe(OH)3 -to-> Fe2O3 +3 H2O
b_________0,5b(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}58a+107b=165\\40a+80b=165-45=120\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=1\\b=1\end{matrix}\right.\)
=> mMg(OH)=1.58=58(g)
=>%mMg(OH)2= (58/165).100=35,152%
=>%mFe(OH)3= 64,848%
b) PTHH: Fe(OH)3 + 3 HCl -> FeCl3 + 3 H2O
1_______________3(mol)
Mg(OH)2 + 2 HCl -> MgCl2 + H2O
1_______2(mol)
=> mHCl=(2+3).36,5= 182,5(g)
=> mddHCl= (182,5.100)/14,6=1250(g)
=> VddHCl= 1250/1,15= 1086,957(ml)
Đúng 2
Bình luận (0)
a) Khối lượng hỗn hợp giảm là khối lượng nước thoát ra
Mg(OH)2 -----to-------> MgO + H2O
x mol ------------------>x------->x (mol)
2Fe(OH)3 ------to----------> Fe2O3 + 3H2O
y mol -----------------------> y/2------->3/2y (mol)
Ta có:\(\left\{{}\begin{matrix}58x+107y=165\\x+\dfrac{3}{2}y=\dfrac{45}{18}=2,5\end{matrix}\right.\)
=> x = 1 và y = 1
=> mMg(OH)2 = 58g và mFe(OH)3 = 107 g
=> %mMg(OH)2 = \(\dfrac{58}{165}.100\) = 35,15%
=> %mFe(OH)3 = 64,85%
b) Y là MgO (1 mol) và Fe2O3 ( 0,5 mol)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
1--------->2 (mol)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
0,5-------->3 (mol)
=> \(m_{HCl}=\left(2+6\right).36,5=292\left(g\right)\)
=>\(m_{ddHCl}=\dfrac{292}{14,6\%}=2000\left(g\right)\)
=> \(V_{ddHCl}=\dfrac{m}{D}=\dfrac{2000}{1,15}=1739,13\left(ml\right)\)
Đúng 1
Bình luận (0)
Khi nung hỗn hợp CaCO3 và MgCO3 có khối lượng là 18,4 gam. Phản ứng xong, hỗn hợp chất rắn có khối lượng giảm 8,8 gam so với khối lượng hỗn hợp rắn trước khi nung. Tính thành phần phần trăm khối lượng của mỗi chất trong hỗn hợp trước khi đun nóng.
Gọi \(n_{CaCO_3}=a\left(mol\right)\) và \(n_{MaCO_3}=b\left(mol\right)\)
PTHH: \(CaCO_3\underrightarrow{t^o}CaO+CO_2\)
\(MgCO_3\underrightarrow{t^o}MgO+CO_2\)
\(\Rightarrow m_{hh}=100a+84b=18,4\)
\(n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)\Rightarrow a+b=0,2\left(mol\right)\)
\(\Rightarrow a=b=0,1\left(mol\right)\)
\(\Rightarrow m_{CaCO_3}=10g;m_{MgCO_3}=8,4g\)
\(\Rightarrow\%m_{CaCO_3}=\dfrac{100\%.10}{18,4}\approx54\%;\%m_{MgCO_3}=100\%-54\%=46\%\)
Đúng 2
Bình luận (0)
Một dd có chứa 25,1g hh gồm nạo và Ba(OH)2 phản ứng vừa đủ với dd CuCl2, thu được 19,6g kết tủa. Tính a/ Thành phần % theo khối lượng mỗi hidroxit trong hh ban đầu b/ Khối lượng CuCl2 10% đã phản ứng c/ Nồng độ % chất tan trong dd sau phản ứng
Một dd có chứa 25,1g hh gồm nạo và Ba(OH)2 phản ứng vừa đủ với dd CuCl2, thu được 19,6g kết tủa. Tính a/ Thành phần % theo khối lượng mỗi hidroxit trong hh ban đầu b/ Khối lượng CuCl2 10% đã phản ứng c/ Nồng độ % chất tan trong dd sau phản ứng
Cho luồng khí H2 có dư đi qua ống sứ có chứa 20 gam hỗn hợp X gồm MgO và CuO nung nóng. Sau khi phản ứng hoàn toàn, sấy khô đem cạn lại thấy khối lượng chất rắn giảm 3,2 gam. Khối lượng MgO và CuO trong hỗn hợp X là: A. 2 gam và 2 gam . B. 4 gam và 16 gam C. 8 gam và 12 gam D. 6 gam và 14 gam
Đọc tiếp
Cho luồng khí H2 có dư đi qua ống sứ có chứa 20 gam hỗn hợp X gồm MgO và CuO nung nóng. Sau khi phản ứng hoàn toàn, sấy khô đem cạn lại thấy khối lượng chất rắn giảm 3,2 gam. Khối lượng MgO và CuO trong hỗn hợp X là:
A. 2 gam và 2 gam .
B. 4 gam và 16 gam
C. 8 gam và 12 gam
D. 6 gam và 14 gam