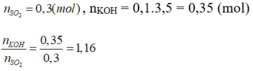Oxi hóa hoàn toàn 8 lít khí SO2 (đktc), sản phẩm thu được hòa tan vào 57,2 ml dd \(H_2SO_4\)60% (D=1,5g/ml)
Tính C% của dd axit thu được

Những câu hỏi liên quan
Oxi hóa hoàn toàn 8lit khí SO2 ( đktc). Sản phẩm thu được hòa tan hoàn toàn vào 57,2 ml dung dịch H2 SO4 60% (D=1,5g/ml). Tính nồng độ phần trăm của dung dịch axit thu được
\(BTNT\left(S\right):n_{SO3}=n_{SO2}=\dfrac{V}{22,4}=\dfrac{5}{14}\left(mol\right)\)
Ta có : \(n_{H2SO4}=\dfrac{9}{25}\left(mol\right)\)
\(\Rightarrow\Sigma n_{H2SO4}=\dfrac{5}{14}+\dfrac{9}{25}=\dfrac{251}{350}\left(mol\right)\)
\(\Rightarrow C\%=\dfrac{m_{H2SO4}}{m_{dd}}.100\%=64,7\%\)
Đúng 1
Bình luận (4)
Cho sản phẩm thu được khi oxi hóa hoàn toàn 3,36 lít khí sunfurơ (đkct) vào 57,2 ml dd H2SO4 60%(D=1,5g/ml) Hãy tính nồng độ % của dd thu được
Cho sản phẩm thu được khi oxi hóa hoàn toàn 3,36 lít khí sunfurơ (đkct) vào 57,2 ml dd H2SO4 60%(D=1,5g/ml). Hãy tính nồng độ % của dd thu được
mdd H2SO4 = 57.2 * 1.5 = 85.8 (g)
mH2SO4 = 85.8 * 60/100 = 51.48 (g)
nSO3 = 3.36/22.4 = 0.15 (mol)
SO3 + H2O => H2SO4
0.15......................0.15
mH2SO4 (tổng) = 0.15*98 + 51.48 = 66.18 (g)
mdd sau phản ứng = 0.15*80 + 85.8 = 97.8 (g)
C% H2SO4 = 66.18 / 97.8 * 100% = 67.66%
Đúng 1
Bình luận (1)
nSO2= 3,36/22,4=0,15 mol
SO2 + O2 -to-> SO3
0,15 0,15 mol
SO3 + H2O --> H2SO4
0,15 0,15 mol
mdd = 0,15*80 + 57,2*1,5=97,8 g
\(\Sigma\)H2SO4= 0,15 *98 + 57,2*1,5*0,6=66,18 g
C% H2SO4=66,18*100/97,8=67,67%
Đúng 1
Bình luận (5)
Oxi hóa hoàn toàn 7,84 lít lưu huỳnh đioxit ở (đktc) rồi cho toàn bộ sản phẩm đi vào bình chứa 57,2 ml dung dịch axit sunfuric 60%( trọng lượng riêng bằng 1,5g/ml).Tính nồng độ phần trăm của dung dịch thu được
\(n_{SO_2}=\dfrac{7.84}{22.4}=0.07\left(mol\right)\)
\(2SO_2+O_2\underrightarrow{^{t^0}}2SO_3\)
\(0.07.............0.07\)
\(m_{dd_{H_2SO_4}}=57.2\cdot1.5=85.8\left(g\right)\)
\(m_{H_2SO_4}=85.8\cdot60\%=51.48\left(g\right)\)
\(SO_3+H_2O\rightarrow H_2SO_4\)
\(0.07..................0.07\)
\(m_{dd}=0.07\cdot80+85.8=91.4\left(g\right)\)
\(\sum n_{H_2SO_4}=0.07\cdot98+51.48=58.34\left(g\right)\)
\(C\%_{H_2SO_4}=\dfrac{58.34}{91.4}\cdot100\%=63.8\%\)
Đúng 3
Bình luận (0)
Oxi hóa hoàn toàn 7,84 lít lưu huỳnh đioxit ở (đktc) rồi cho toàn bộ sản phẩm đi vào bình chứa 57,2 ml dung dịch axit sunfuric 60%( trọng lượng riêng bằng 1,5 g/ml).Tính nồng độ phần trăm của dung dịch thu được
$2SO_2 + O_2 \xrightarrow{t^o,xt} 2SO_3$
n SO3 = n SO2 = 7,84/22,4= 0,35(mol)
$SO_3 + H_2O \to H_2SO_4$
m dd H2SO4 60% = 57,2.1,5 = 85,8(gam)
Sau khi pha :
m H2SO4 = 85,8.60% + 0,35.98 = 85,78(gam)
m dd = 85,8 + 0,35.80 = 113,8(gam)
C% H2SO4 = 85,78/113,8 .100% = 75,38%
Đúng 3
Bình luận (0)
1.Cho 4.6 gam Na tác dụng với 200 gam dung dịch HCl 2.92%.Tính nồng độ phần trăm của mỗi chất có trong dung dịch thu được
2. Oxi hóa 8 lít khí SO2 (đktc) thu được sản phẩm cho hòa tan vào 57.2 ml dung dịch H2SO4 60%, khối lượng riêng 1.5 g/ml. TÍnh C% của dung dịch Axit thu được.
1 , \(n_{Na}=\frac{4,6}{23}=0,2\left(mol\right)\)
\(m_{HCl}=200.2,92\%=5,84\left(mol\right)\) => \(n_{HCl}=\frac{5,84}{36,5}=0,16\left(mol\right)\)
\(2Na+2HCl->2NaCl+H_2\left(1\right)\)
vì \(\frac{0,2}{2}>\frac{0,16}{2}\) => Na dư , HCl hết
dung dịch thu được là dung dịch NaCl
theo (1) \(n_{NaCl}=n_{HCl}=0,16\left(mol\right)\) => \(m_{NaCl}=0,16.58,5=9,36\left(g\right)\)
\(n_{H_2}=\frac{1}{2}n_{HCl}=0,08\left(mol\right)\)
khối lượng dung dịch sau phản ứng là
4,6+200-0,08.2=204,44(g)
\(C_{\%\left(NaCl\right)}=\frac{9,36}{204,44}.100\%\approx4,58\%\)
Đúng 0
Bình luận (0)
1.Cho 4.6 gam Na tác dụng với 200 gam dung dịch HCl 2.92%.Tính nồng độ phần trăm của mỗi chất có trong dung dịch thu được
2. Oxi hóa 8 lít khí SO2 (đktc) thu được sản phẩm cho hòa tan vào 57.2 ml dung dịch H2SO4 60%, khối lượng riêng 1.5 g/ml. TÍnh C% của dung dịch Axit thu được.
Oxi hóa hoàn toàn 8l SO2 ( đktc) sản phẩm thu được hòa tan vào 57,2 ml dd H2SO4 60% ( D = 1,5 g/ml ) .Tính C% của dung dịch axit thu được
PTHH : 2SO2+ O2--> 2SO3 ( điều kiện là nhiệt độ ,xúc tác V2O5);
--> nSO3= nSO2=8/22,4 = 5/14 (mol);
mH2SO4 trong dd = 57,2 * 1,5 * 60%=51,48 (g);
PTHH : SO3+ H2O--> H2SO4;
--> mH2SO4 tạo thành = 5/14 * 98=35(g);
C%dd axit thu được = (51,48+ 35) / (57,2* 1,5+35) =71,59%;
Đúng 0
Bình luận (0)
PTHH: 2SO2 + O2 --> 2SO3 (1)
SO3 + H2O --> H2SO4 (2)
Theo PT(1): nSO2=nSO3=8/22,4=5/14 mol
=> mSO3=5/14.80=200/7 g
Theo PT(2): nH2SO4=nSO3=5/14 mol
=> mH2SO4=5/14.98=35g
Mặt khác:
mdd.H2SO4 = 57,2.1,5 = 85,8g
=> mH2SO4 = 85,8.60% = 51,48g
=> Tổng khối lượng H2SO4 = 35 + 51,48 = 86,48g
=> mdd sau p/ứ = 85,8+200/7=4003/35g
=> C% của dd axit thu được = 86,48/4003/35.100%=75,61%
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 6,72 lít SO2 (đktc) vào 100 ml dd KOH 3,5M, muối thu được sau phản ứng là: A. K2SO3 B. KHSO3 C. K2SO3 và KHSO3 D. K2SO4
Đọc tiếp
Hòa tan hoàn toàn 6,72 lít SO2 (đktc) vào 100 ml dd KOH 3,5M, muối thu được sau phản ứng là:
A. K2SO3
B. KHSO3
C. K2SO3 và KHSO3
D. K2SO4