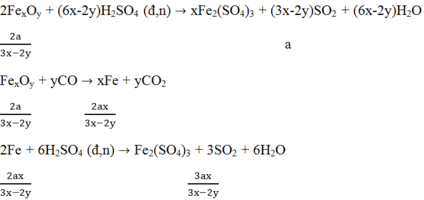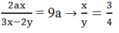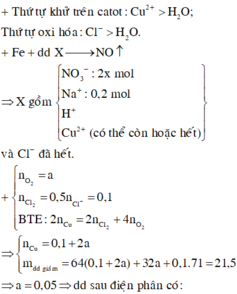Khử hoàn toàn 0.58 tấn quặng sắt chứa 90% là Fe3O4 bằng khí hidro. Khối lượng sắt thu được là

Những câu hỏi liên quan
Hòa tan hoàn toàn m (g) một oxit sắt bằng H2SO4 đặc nóng thu được a mol SO2 (duy nhất). Mặt khác, sau khi khử hoàn toàn m (g) oxit trên bằng H2 ở nhiệt độ cao rồi cho toàn bộ lượng sắt tạo thành vào H2SO4 đặc nóng dư thì thu được 9a mol SO2 (duy nhất). Vậy oxit sắt là: A. FeO B. Fe2O3 C. Fe3O4 D. FeO hoặc Fe2O3
Đọc tiếp
Hòa tan hoàn toàn m (g) một oxit sắt bằng H2SO4 đặc nóng thu được a mol SO2 (duy nhất). Mặt khác, sau khi khử hoàn toàn m (g) oxit trên bằng H2 ở nhiệt độ cao rồi cho toàn bộ lượng sắt tạo thành vào H2SO4 đặc nóng dư thì thu được 9a mol SO2 (duy nhất). Vậy oxit sắt là:
A. FeO
B. Fe2O3
C. Fe3O4
D. FeO hoặc Fe2O3
Quạng oxit sắt từ chứa 80% Fe3O4.Cần dùng bao nhiêu tấn kim loại quặng này để sản suất 100 tấn gang có 5% các nguyên tố không phải là sắt ?Biết rằng trong quá trình luyện gang lượng sắt bị hao hụt là 4%
nguyên tắc để sản xuất gang ,thép trong luyện kim là PỨ khử oxit sắt trong quặng sắt thành sắt:
a.khối lượng sắt khi khử hoàn toàn 4,64g Fe2SO4
b.hòa lượng sắt thu được vào 500ml dd H2SO4 loãng có nồng độ 0,1M. Sau khi PỨ xảy ra hoàn toàn, thì chất nào hết, chất nào dư
-tính thể tích khí thoát ra(đktc)
-tính nồng độ mol/lit của các chất còn lại sau PỨ
-cô cạn dd thu được bao nhiêu gam muối khan
Đọc tiếp
nguyên tắc để sản xuất gang ,thép trong luyện kim là PỨ khử oxit sắt trong quặng sắt thành sắt:
a.khối lượng sắt khi khử hoàn toàn 4,64g Fe2SO4
b.hòa lượng sắt thu được vào 500ml dd H2SO4 loãng có nồng độ 0,1M. Sau khi PỨ xảy ra hoàn toàn, thì chất nào hết, chất nào dư
-tính thể tích khí thoát ra(đktc)
-tính nồng độ mol/lit của các chất còn lại sau PỨ
-cô cạn dd thu được bao nhiêu gam muối khan
Fe3O4 mới đúng nhé.không phải Fe2SO4
a,\(Fe_3O_4+4H_2\rightarrow3Fe+4H_2O\)
\(n_{Fe3O4}=\frac{4,64}{232}=0,02\left(mol\right)\)
\(\Rightarrow n_{Fe}=0,06\left(mol\right)\)
\(m_{Fe}=0,06.56=3,36\left(g\right)\)
b,\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(n_{H2SO4}=0,05.0,1=0,05\left(mol\right)\)
Tỉ lệ: \(\frac{0,06}{1}>\frac{0,05}{1}\)
Nên Fe dư
\(n_{Fe\left(dư\right)}=0,06-0,05=0,01\left(mol\right)\)
\(m_{Fe\left(dư\right)}=0,01.56=0,56\left(g\right)\)
\(n_{H2}=n_{H2SO4}=0,05\left(mol\right)\)
\(V_{H2}=0,05.22,4=1,12\left(l\right)\)
\(CM_{FeSO4}=\frac{0,05}{0,5}=0,1M\)
\(m_{FeSO4}=0,05.152=7,6\left(g\right)\)
Đúng 0
Bình luận (0)
Cho m gam bột sắt tác dụng hoàn toàn với dung dịch HCl 10% thu được 1,12lit khí hidro ( ở đktc )
a , Viết PTHH của phản ứng trên
b , Tính khối lượng bột sắt ( m )
c , Tính khối lượng dung dịch HCl cần dùng ( Biết : Fe = 56 ; H=1 )
Ta có: \(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
a, PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
_____0,05__0,1____________0,05 (mol)
b, mFe = 0,05.56 = 2,8 (g)
c, mHCl = 0,1.36,5 = 3,65 (g)
\(\Rightarrow m_{ddHCl}=\dfrac{3,65}{10\%}=36,5\left(g\right)\)
Bạn tham khảo nhé!
Đúng 1
Bình luận (0)
\(n_{H_2}=\dfrac{1.12}{22.4}=0.05\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(0.05......0.1...................0.05\)
\(m_{Fe}=0.05\cdot56=2.8\left(g\right)\)
\(m_{dd_{HCl}}=\dfrac{0.1\cdot36.5\cdot100}{10}=36.5\left(g\right)\)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 20,88 gam một oxit sắt bằng dung dịch H2SO4 đặc, nóng thu được dung dịch X và 3,248 lít khí SO2 (sản phầm khử duy nhất, ở đktc). Cô cạn dung dịch X, thu được m gam muối sunfat khan. Giá trị của m là:
A. 52,2
B. 48,4
C. 54,0
D. 58,0
Đáp án D
Ta có: = 0,145 mol
Quy đổi 20,88 g oxit sắt FexOy thành 20,88 g Fe và O
Gọi nFe = x mol; nO = y mol
Quá trình nhường electron:
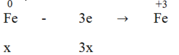
Quá trình nhận electron:
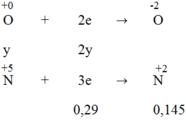
Áp dụng định luật bảo toàn electron, ta có:
3x = 2y + 0,29 → 3x - 2y = 0,29 (1)
Mặt khác: 56x + 16y = 20,88 (2)
Từ (1) và (2) → x = 0,29 và y = 0,29
Muối sinh ra là muối Fe2(SO4)3. Áp dụng ĐL bảo toàn nguyên tố ta có:
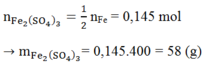
Đúng 0
Bình luận (0)
7- Hòa tan hoàn toàn 5,6g sắt(Fe) vào dung dịch Axit clohiđric(HCl) thu được sắt(II) clorua (FeCl2) và khí Hidro (H2)
a) Hãy lập phương trình hóa học xảy ra?
b) Tính khối lượng của FeCl2 tạo thành sau phản ứng?
c)Tính thể tích khí Hidro(ở đktc) tạo thành sau phản ứng?
a) Fe + 2HCl --> FeCl2 + H2
b) \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
_____0,1--------------->0,1---->0,1
=> mFeCl2 = 0,1.127 = 12,7(g)
c) VH2 = 0,1.22,4 = 2,24(l)
Đúng 2
Bình luận (0)
\(n_{Fe}=\dfrac{5,6}{56}=0,1(mol)\\ a,Fe+2HCl\to FeCl_2+H_2\\ \Rightarrow n_{FeCl_2}=n_{H_2}=0,1(mol)\\ a,m_{FeCl_2}=0,1.127=12,7(g)\\ b,V_{H_2}=0,1.22,4=2,24(l)\)
Đúng 1
Bình luận (0)
Điện phân dung dịch chứa 0,2 mol NaCl và x mol
Cu
NO
3
2
với điện cực trơ, sau một thời gian thu được dung dịch X và khối lượng dung dịch giảm 21,5 gam. Cho thanh sắt vào dung dịch X đến khi các phản ứng xảy ra hoàn toàn, thấy khối lượng thanh sắt giảm 1,8 gam và thấy thoát ra khí NO duy nhất. Giá trị của x là: A. 0,4 B. 0,5. C. 0,6 D. 0,3.
Đọc tiếp
Điện phân dung dịch chứa 0,2 mol NaCl và x mol Cu NO 3 2 với điện cực trơ, sau một thời gian thu được dung dịch X và khối lượng dung dịch giảm 21,5 gam. Cho thanh sắt vào dung dịch X đến khi các phản ứng xảy ra hoàn toàn, thấy khối lượng thanh sắt giảm 1,8 gam và thấy thoát ra khí NO duy nhất. Giá trị của x là:
A. 0,4
B. 0,5.
C. 0,6
D. 0,3.
Điện phân dung dịch chứa 0,2 mol NaCl và x mol Cu(NO3)2 với điện cực trơ, sau một thời gian thu được dung dịch X và khối lượng dung dịch giảm 21,5 gam. Cho thanh sắt vào dung dịch X đến khi các phản ứng xảy ra hoàn toàn, thấy khối lượng thanh sắt giảm 1,8 gam và thấy thoát ra khí NO duy nhất. Giá trị của x là A. 0,4. B. 0,5. C. 0,6. D. 0,3.
Đọc tiếp
Điện phân dung dịch chứa 0,2 mol NaCl và x mol Cu(NO3)2 với điện cực trơ, sau một thời gian thu được dung dịch X và khối lượng dung dịch giảm 21,5 gam. Cho thanh sắt vào dung dịch X đến khi các phản ứng xảy ra hoàn toàn, thấy khối lượng thanh sắt giảm 1,8 gam và thấy thoát ra khí NO duy nhất. Giá trị của x là
A. 0,4.
B. 0,5.
C. 0,6.
D. 0,3.
Điện phân dung dịch chứa 0,2 mol NaCl và x mol Cu(NO3)2 với điện cực trơ, sau một thời gian thu được dung dịch X và khối lượng dung dịch giảm 21,5 gam. Cho thanh sắt vào dung dịch X đến khi các phản ứng xảy ra hoàn toàn, thấy khối lượng thanh sắt giảm 1,8 gam và thấy thoát ra khí NO duy nhất. Giá trị của x là A. 0,3. B. 0,5. C. 0,6. D. 0,4.
Đọc tiếp
Điện phân dung dịch chứa 0,2 mol NaCl và x mol Cu(NO3)2 với điện cực trơ, sau một thời gian thu được dung dịch X và khối lượng dung dịch giảm 21,5 gam. Cho thanh sắt vào dung dịch X đến khi các phản ứng xảy ra hoàn toàn, thấy khối lượng thanh sắt giảm 1,8 gam và thấy thoát ra khí NO duy nhất. Giá trị của x là
A. 0,3.
B. 0,5.
C. 0,6.
D. 0,4.