Viết các phương trình phản ứng diều chế khí Oxi, Hiđro trong phòng thí nghiệm? So sánh cách thu khí Oxi với cách thu khí hiđro

Những câu hỏi liên quan
Trong phòng thí nghiệm ,người ta điều chế Hydrogen bằng cách cho Zine tác dụng với dung dịch Hydrochloric acid.A)Viết phương trình hóa học biểu diễn phản ứng điều chế trên.B)Tính thể tích hydrogen thu được ở đktc,nếu hòa tan hoàn toàn 7,89g Zine.C)Tính khối lượng nước thu được khi đốt cháy lượng khí hydrogen trên bằng 5,6l không khí (đktc)(biết Oxygen chiếm 1/5 thể tích không khí)
Đọc tiếp
Trong phòng thí nghiệm ,người ta điều chế Hydrogen bằng cách cho Zine tác dụng với dung dịch Hydrochloric acid.A)Viết phương trình hóa học biểu diễn phản ứng điều chế trên.B)Tính thể tích hydrogen thu được ở đktc,nếu hòa tan hoàn toàn 7,89g Zine.C)Tính khối lượng nước thu được khi đốt cháy lượng khí hydrogen trên bằng 5,6l không khí (đktc)(biết Oxygen chiếm 1/5 thể tích không khí)
A) Phương trình hóa học:
Zn + 2HCl→ZnCl2 + H2
B) nZn=\(\dfrac{7,89}{65}\)= ??? (số nó cứ bị sao sao ấy, bạn xem lại khối lượng Kẽm xem có sai không nhé)
đến đây thì mình khá ? bởi vì Zine là chất gì thì nghĩ là Zinc mà Zinc là Kẽm nên đó.
Đúng 0
Bình luận (0)
1) từ quăng pirit sắt ,nước biển , không khí hãy viết phương trình hóa học để điều chế các chất FeSO4 , FeCl3 , FeCl2 , NaHSO4.
2) khi điều chế khí Clo trong phòng thí nghiệm trước khi thu khí clo người ta dẫn khí clo thu đc qua bình đựng H2SO4 đặc và trên bình thu khí có đạy bông tẩm xút . hãy giải thích tại sao lại làm như vậy ?
Trong phòng thí nghiệm, bộ dụng cụ vẽ dưới đây có thể dùng điều chế bao nhiêu khí trong số các khí sau: Cl2, NH3, SO2, CO2, H2, C2H4 (các điều kiện phản ứng có đủ) A. 2. B. 5. C. 4. D. 3.
Đọc tiếp
Trong phòng thí nghiệm, bộ dụng cụ vẽ dưới đây có thể dùng điều chế bao nhiêu khí trong số các khí sau: Cl2, NH3, SO2, CO2, H2, C2H4 (các điều kiện phản ứng có đủ)
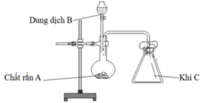
A. 2.
B. 5.
C. 4.
D. 3.
Đáp án D
Để điều chế được khí C theo bộ dụng cụ vẽ trên thì khí C phải thỏa mãn 2 điều kiện:
nặng hơn không khí và không tác dụng với N2, O2 (thành phần chủ yếu của không khí).
Vậy có Cl2, SO2 và CO2 thỏa mãn.
Các phương trình điều chế:
MnO2 r + 4HCl dd → MnCl2 + Cl2 + 2H2O.
Na2SO3 r + H2SO4 dd → Na2SO4 + SO2 + H2O.
CaCO3 r + 2HCl dd → CaCl2 + CO2 + H2O.
Đúng 0
Bình luận (0)
Trong phòng thí nghiệm, bộ dụng cụ vẽ dưới đây có thể dùng điều chế bao nhiêu khí trong số các khí sau: Cl2, NH3, SO2, CO2, H2, C2H4 (các điều kiện phản ứng có đủ) A. 2. B. 5. C. 4. D. 3.
Đọc tiếp
Trong phòng thí nghiệm, bộ dụng cụ vẽ dưới đây có thể dùng điều chế bao nhiêu khí trong số các khí sau: Cl2, NH3, SO2, CO2, H2, C2H4 (các điều kiện phản ứng có đủ)
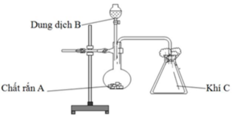
A. 2.
B. 5.
C. 4.
D. 3.
Đáp án D
Để điều chế được khí C theo bộ dụng cụ vẽ trên thì khí C phải thỏa mãn 2 điều kiện:
nặng hơn không khí và không tác dụng với N2, O2 (thành phần chủ yếu của không khí).
Vậy có Cl2, SO2 và CO2 thỏa mãn.
Các phương trình điều chế:
MnO2 r + 4HCl dd → MnCl2 + Cl2 + 2H2O.
Na2SO3 r + H2SO4 dd → Na2SO4 + SO2 + H2O.
CaCO3 r + 2HCl dd → CaCl2 + CO2 + H2O.
Đúng 0
Bình luận (0)
Trong phòng thí nghiệm, bộ dụng cụ vẽ dưới đây: Thí nghiệm trên có thể dùng điều chế bao nhiêu khí trong số các khí sau: Cl2, NH3, SO2, CO2, H2, C2H4 (các điều kiện phản ứng có đủ). A. 2 B. 5 C. 4 D. 3.
Đọc tiếp
Trong phòng thí nghiệm, bộ dụng cụ vẽ dưới đây:
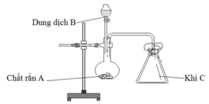
Thí nghiệm trên có thể dùng điều chế bao nhiêu khí trong số các khí sau: Cl2, NH3, SO2, CO2, H2, C2H4 (các điều kiện phản ứng có đủ).
A. 2
B. 5
C. 4
D. 3.
Chọn D.
Khí C thu bằng cách đẩy không khí, ngửa bình nên C phải nặng hơn không khí (loại NH3, H2, C2H4).
Cl2: dung dịch HCl đặc + MnO2 rắn
SO2: dung dịch H2SO4 đặc + Na2SO3 rắn
CO2: dung dịch HCl + CaCO3 rắn
Đúng 0
Bình luận (0)
Cho các chất khí sau: SO2 ; H2 .
a) Trong phòng thí nghiệm, khi điều chế các khí trên, muốn thu lại các khí đó vào các lọ sạch và khô, phải đặt lọ ống nghiệm như thế nào khi dẫn khí vào? Hãy vẽ hình minh họa?
\(d_{SO_2/kk}=\dfrac{64}{29}=2,207\)
=> SO2 nặng hơn không khí => Đặt đứng ống nghiệm
\(d_{H_2/kk}=\dfrac{2}{29}=0,069\)
=> H2 nhẹ hơn không khí => Đặt ngược ống nghiệm
Đúng 1
Bình luận (0)
Ta có:
\(d_{SO_2/kk}=\dfrac{M_{SO_2}}{M_{kk}}=\dfrac{64}{29}=2,207\)
\(\Rightarrow\) Khí SO2 nặng hơn không khí vậy đặt thẳng lọ ống nghiệm
\(d_{H_2/kk}=\dfrac{M_{H_2}}{M_{kk}}=\dfrac{2}{29}=0,069\)
⇒Khí H2 nhẹ hơn không khí vậy đặt úp lọ ống nghiệm
Đúng 1
Bình luận (0)
Bài 4. Cho 12g sắt (III) oxit phản ứng với khí Hiđro ta thu đc sắt và nước
a, Tính thể tích khí oxi (ở đktc) cần dùng
b, Tính khối lượng sắt thu đc sau phản ứng
Bài 5. Cho 19,5g Zn tác dụng với dung dịch axit sunfuric loãng thu đc kẽm sunfat và khí hiđro
a, Tính khối lượng kẽm sunfat thu đc sau phản ứng
b, Tính thể tích khí Hiđro thu đc ở (đktc)
Đọc tiếp
Bài 4. Cho 12g sắt (III) oxit phản ứng với khí Hiđro ta thu đc sắt và nước
a, Tính thể tích khí oxi (ở đktc) cần dùng
b, Tính khối lượng sắt thu đc sau phản ứng
Bài 5. Cho 19,5g Zn tác dụng với dung dịch axit sunfuric loãng thu đc kẽm sunfat và khí hiđro
a, Tính khối lượng kẽm sunfat thu đc sau phản ứng
b, Tính thể tích khí Hiđro thu đc ở (đktc)
Bài 4 câu a đề là thể tích H2 nha bạn
a)\(Fe2O3+3H2-->2Fe+3H2O\)
\(n_{Fe2O3}=\frac{12}{160}=0,075\left(mol\right)\)
\(n_{H2}=3n_{Fe2O3}=0,225\left(mol\right)\)
\(V_{H2}=0,225.22,4=5,04\left(l\right)\)
b)\(n_{Fe}=2n_{Fe2O3}=0,15\left(mol\right)\)
\(m_{Fe}=0,15.56=8,4\left(g\right)\)
Bài 6
a)\(Zn+H2SO4-->ZnSO4+H2\)
\(n_{Zn}=\frac{19,5}{65}=0,3\left(mol\right)\)
\(n_{ZnSO4}=n_{Zn}=0,3\left(mol\right)\)
\(m_{ZnSO4}=0,3.162=48,3\left(g\right)\)
b)\(n_{H2}=n_{Zn}=0,3\left(mol\right)\)
\(V_{H2}=0,3.22,4=6,72\left(l\right)\)
a)Fe2O3+3H2−−>2Fe+3H2O
0,075-------0,225---0,15 mol
nFe2O3=12/160=0,075(mol)
VH2=0,225.22,4=5,04(l)
b)
mFe=0,15.56=8,4(g)
Bài 6
a)Zn+H2SO4−−>ZnSO4+H2
0,3----------------------0,3---0,3
nZn=19,5/65=0,3(mol)
mZnSO4=0,3.162=48,3(g)
b)
=>VH2=0,3.22,4=6,72(l)
B5, Pthh: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
Số mol của 19,5g Zn là:
\(n=\frac{m}{M}=\frac{19,5}{65}=0,3\left(mol\right)\)
KL \(ZnSO_4\) sau phản ứng là:
\(m=n\times M=0,3\times\left(65+32+16\times4\right)=48,3\left(g\right)\)
Thể tích khi \(H_2\)(đktc) là
\(V=n\times22,4=0,3\times22,4=6,72\)
Xem thêm câu trả lời
1. Đốt cháy hoàn toàn 9 gam kim loại Mg trog không khí thu được 15 gam magie oxi ( MgO) . cho rằng chỉ xảy ra phản ứng giữa mg với oxi (O2) trong không khí a, viết PTHH của pưng hóa học xảy ra b, viết phương trình bảo toàn khối lượng c, tính khối lượng của oxi đã phản ứng Các bạn giúp mình nha mình đang cần gấp .........
Đọc tiếp
1. Đốt cháy hoàn toàn 9 gam kim loại Mg trog không khí thu được 15 gam magie oxi ( MgO) . cho rằng chỉ xảy ra phản ứng giữa mg với oxi (O2) trong không khí
a, viết PTHH của pưng hóa học xảy ra
b, viết phương trình bảo toàn khối lượng
c, tính khối lượng của oxi đã phản ứng
Các bạn giúp mình nha mình đang cần gấp .........![]()
1/
a) PTHH 2Mg + O2 ===> 2MgO
b) Phương trình bảo toàn khối lượng là:
mMgO + mO2 = mMgO
c) Áp dụng định luật bào toàn khối lượng theo câu b) ta có:
mO2 = mMgO - mMg
<=> mO2 = 15 - 9 = 6 gam
Đúng 0
Bình luận (0)
Thu khí hidro bằng cách đẩy không khí .Nêu hiện tượng và viết phương trình hóa hoc
- thao tác: úp ống nghiệm thứ hai lên đầu ống dẫn khí hiđro sinh ra để thu khí trong khoảng 1 phút. Sau đó, giữ nguyên tư thế ống nghiệm, đưa miệng ống nghiệm vào gần sát ngọn lửa đèn cồn.
- hiện tượng quan sát được: có tiếng nổ nhỏ phát ra do hiđro thu được chưa tinh khiết.
- phương trình: \(2H_2+O_2\underrightarrow{t^o}H_2O\)
Đúng 1
Bình luận (0)






















