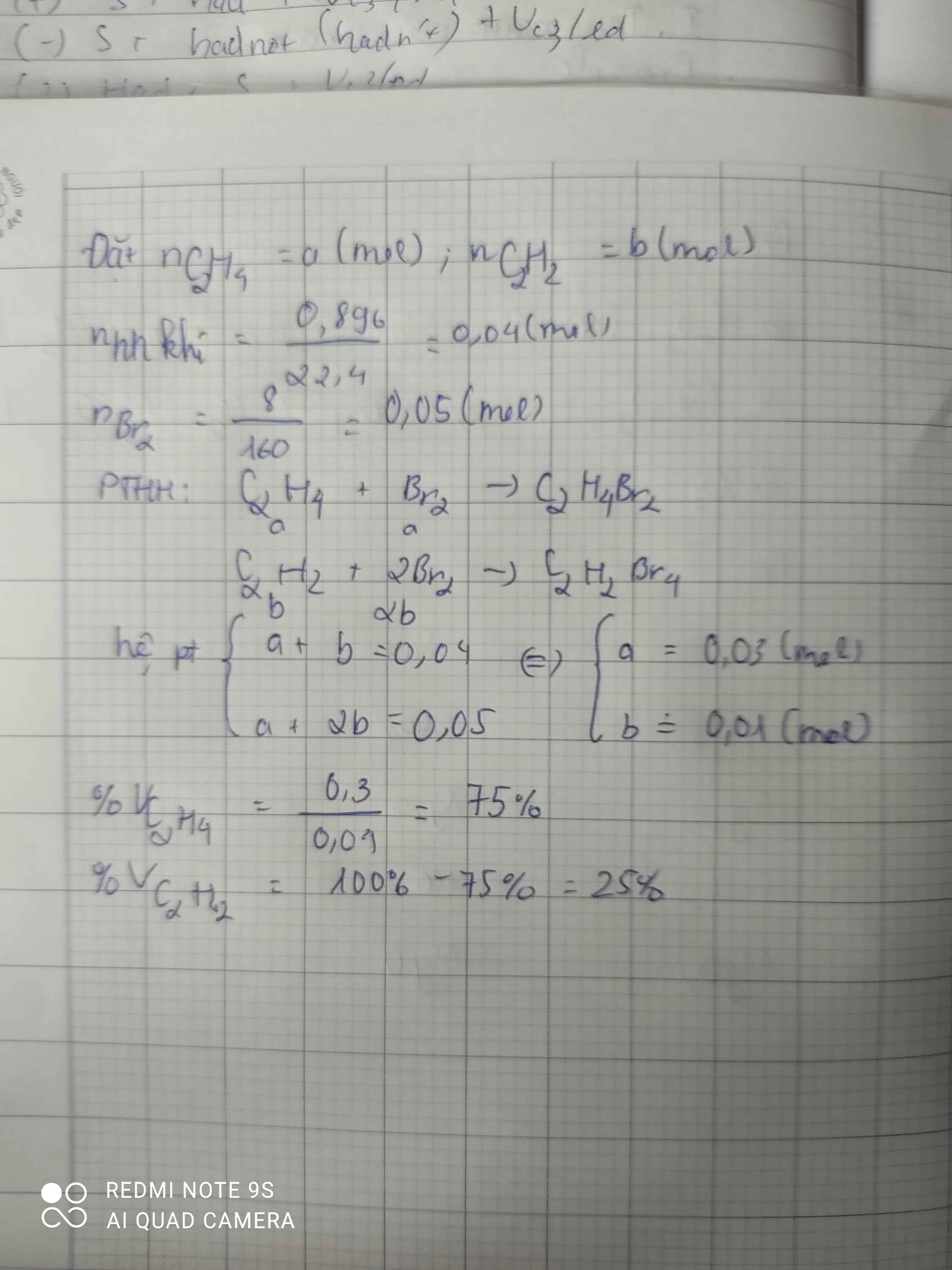Cho sản phẩm tạo thành khi dun nóng hh gồm. 16.8 g fe và 8g s vao dd h2so4 loãng thu duoc dd A và hh khí B. %V các khí trong B la?

Những câu hỏi liên quan
cho 11,8 g hh X gồm cu và fe vào dd h2so4 loãng dư đến khi pu xảy ra hoàn toàn thì thu được 0,56(l) khí ở kdtc).Cũng lượng X trên cho vào dd h2so4 đặc nóng thì thu được V lít khí so2(dktc),dẫn lượng khí thu được vào 250ml dd naoh 1M,thu được 21,9g muối
a)tính thành phần % khối lượng mỗi kl trong hh ban đầu
b)Tính V
\(n_{H_2}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\)
\(n_{NaOH}=0,25.1=0,25\left(mol\right)\)
Cho X vào dung dịch `H_2SO_4` loãng:
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,025<-----------------------0,025
a. \(\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{56.0,025.100\%}{11,8}=11,86\%\\\%m_{Cu}=\dfrac{\left(11,8-0,025.56\right).100\%}{11,8}=88,14\%\end{matrix}\right.\)
b. \(n_{Cu}=\dfrac{11,8-0,025.56}{64}=0,1625\left(mol\right)\)
Cũng lượng X trên cho vào dung dịch `H_2SO_4` đặc nóng:
Giả sử Fe tác dụng hết với dung dịch \(H_2SO_{4.đn}\)
\(2Fe+6H_2SO_{4.đn}\rightarrow Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
0,025----------------------------------->0,0375
\(Cu+2H_2SO_{4.đn}\rightarrow CuSO_4+SO_2+2H_2O\)
0,1625--------------------------->0,1625
\(\Sigma n_{SO_2}=0,0375+0,1625=0,2\left(mol\right)\)
Có: \(\dfrac{n_{NaOH}}{n_{SO_2}}=\dfrac{0,25}{0,2}=1,25\)
=> Phản ứng giữa `NaOH` và `SO_2` tạo muối axit trước (tỉ lệ 1:1)
\(SO_2+NaOH\rightarrow NaHSO_3\)
0,2---->0,2------->0,2
Xét \(\dfrac{0,2}{1}< \dfrac{0,25}{1}\Rightarrow\) NaOH dư.
\(n_{NaOH.dư}=0,25-0,2=0,05\left(mol\right)\)
\(NaOH+NaHSO_3\rightarrow Na_2SO_3+H_2O\)
0,05----->0,05---------->0,05
Xét \(\dfrac{0,05}{1}< \dfrac{0,2}{1}\Rightarrow NaHSO_3.dư\)
Sau phản ứng thu được: \(\left\{{}\begin{matrix}n_{NaHSO_3}=0,2-0,05=0,15\left(mol\right)\\n_{Na_2SO_3}=0,05\left(mol\right)\end{matrix}\right.\)
\(m_{muối}=0,15.104+0,05.126=21,9=m_{muối.thu.được.theo.đề}\)
=> Giả sử đúng.
\(\Rightarrow V=V_{SO_2}=0,2.22,4=4,48\left(l\right)\)
Đúng 1
Bình luận (0)
Cho 0,896lit hh gồm C2H4 và C2H2 phản ứng hoàn toàn với dd Br2, thấy có 8g Br2 tham gia. Tính: a/ %(V) mỗi khí trong hh các khí đo ở đkc b/ Khối lượng sản phẩm thu được
Ta có Cùng điều kiện -> Quy số lít về số mol.n(hh ban đầu) = 20 mol; n(hh sau) = 16 lít
=> H2 phản ứng mất 4 lít => C2H2 có 2 lít và CH4 có 8 lít
Đúng 1
Bình luận (0)
a.\(n_{hh}=\dfrac{V_{hh}}{22,4}=\dfrac{0,896}{22,4}=0,04mol\)
\(n_{Br_2}=\dfrac{m_{Br_2}}{M_{Br_2}}=\dfrac{8}{160}=0,05mol\)
Gọi \(n_{C_2H_2}\) là x => \(V_{C_2H_2}=22,4x\)
\(n_{C_2H_4}\) là y => \(V_{C_2H_4}=22,4y\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
x 2x x ( mol )
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
y y y ( mol )
Ta có hpt:
\(\left\{{}\begin{matrix}22,4x+22,4y=0,896\\2x+y=0,05\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,01\\y=0,03\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}V_{C_2H_2}=0,01.22,4=0,224\\V_{C_2H_4}=0,03.22,4=0,672\end{matrix}\right.\)
\(\%V_{C_2H_2}=\dfrac{0,224}{0,896}.100=25\%\)
\(\%V_{C_2H_4}=100-25=75\%\)
b.\(m_{Sp}=0,01.186+0,03.346+0,03.188=16,02g\)
( Em cảm ơn anh Kudo Sinichi rất nhiều ạ!! )
Đúng 1
Bình luận (1)
Xem thêm câu trả lời
cho 3,2g gồm hh Fe,S và FeS tác dụng với dd H2SO4 đặc, nóng dư thu được dd X và khí SO2 là sản phẩm khử duy nhất. Biết số mol H2SO4 đã pứ là 0,18mol
Cô cạn dd X thu được bao nhiêu gam muối khan?
Quy đổi hh ban đầu thành \(\left\{{}\begin{matrix}Fe:a\left(mol\right)\\S:b\left(mol\right)\end{matrix}\right.\)
=> 56a + 32b = 3,2 (1)
PTHH: 2Fe + 6H2SO4 --> Fe2(SO4)3 + 3SO2 + 6H2O
a------->3a--------->0,5a
S + 2H2SO4 --> 3SO2 + 2H2O
b---->2b
=> 3a + 2b = 0,18 (2)
(1)(2) => a = 0,04 (mol); b = 0,03 (mol)
=> \(n_{Fe_2\left(SO_4\right)_3}=0,02\left(mol\right)\)
=> mFe2(SO4)3 = 0,02.400 = 8 (g)
Đúng 4
Bình luận (0)
Quy đổi hh ban đầu thành \(\left\{{}\begin{matrix}Fe:a\left(mol\right)\\S:b\left(mol\right)\end{matrix}\right.\)
=> 56a + 32b = 3,2 (1)
PTHH: 2Fe + 6H2SO4 --> Fe2(SO4)3 + 3SO2 + 6H2O
a------->3a--------->0,5a
S + 2H2SO4 --> 3SO2 + 2H2O
b---->2b
=> 3a + 2b = 0,18 (2)
(1)(2) => a = 0,04 (mol); b = 0,03 (mol)
=> \(n_{Fe_2\left(SO_4\right)_3}=0,02\left(mol\right)\)
=> mFe2(SO4)3 = 0,02.400 = 8 (g)
Cho 20 g hh A chứa Fe và FeS vào dd H2SO4 loãng dư. Sau pứ thu đc dd X và 6,72 lít khí Y ở đktc.
Tính số mol H2SO4 đặc nóng tối thiểu dùng để hoà tan 20 g hh A ở trên. Biết sp khử của \(\overset{+6}{S}\) là \(SO_2\)
Ta có: 56nFe + 88nFeS = 20 (1)
\(n_Y=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
BT e: 2nH2 = 2nFe ⇒ nH2 = nFe
BTNT S: nH2S = nFeS
⇒ nFe + nFeS = 0,3 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Fe}=0,2\left(mol\right)\\n_{FeS}=0,1\left(mol\right)\end{matrix}\right.\)
Coi A gồm: Fe: 0,3 (mol) và S: 0,1 (mol)
BT e, có: 2nFe + 4nS = 2nSO2
⇒ nSO2 = 0,5 (mol)
BTNT Fe: nFeSO4 = nFe = 0,3 (mol)
BTNT S: nH2SO4 = 0,3 + 0,5 = 0,8 (mol)
Đúng 3
Bình luận (0)
hh khí X gồm khí O2 và khí Y sau khi thực hiện phản ứng nổ làm lạnh sản phẩm thi được khí A và chất lỏng B. Cho khí A tác dụng với Fe thu được chất rắn C.Cho B tác dụng với SO3 thu được dd D.Cho C tác dụng với dd D loãng dư thu được khí Y. Cho khí Y tác dụng với CuO thu được chất rắn G. Viết PTHH xảy ra và cho biết các chất có trong A,B,C,D,G,Y. Biết khí Y được dùng bơm vào kinh khí cầu
Đọc tiếp
hh khí X gồm khí O2 và khí Y sau khi thực hiện phản ứng nổ làm lạnh sản phẩm thi được khí A và chất lỏng B. Cho khí A tác dụng với Fe thu được chất rắn C.Cho B tác dụng với SO3 thu được dd D.Cho C tác dụng với dd D loãng dư thu được khí Y. Cho khí Y tác dụng với CuO thu được chất rắn G. Viết PTHH xảy ra và cho biết các chất có trong A,B,C,D,G,Y. Biết khí Y được dùng bơm vào kinh khí cầu
Xđ % khối lượng các chất có trong hh đầu ở các trường hợp sau:a. Cho H2SO4 loãng dư vào hh kẽm và magie cacbonat .Sau phản ứng thu 4,48 lít khí và cô cạn dd thu 28.1gam muối khanb.hh gồm Al2O3 , Na tan hết vào dd H2SO4 loãng vừa đủ tạo 7,26 g muối và giải phóng 336ml khí c.hh gồm Fe,Fe2O3 tan hết vào 92,2ml dd H2SO4 đặt,to, đủ thu đc dd chứa 100g muối .Khi cho dd thu đc tác dụng với dd Ba(OH)2 đủ cô cạn dd sau phản ứng đc a gam chất rắn B.Nung B đến khối lượng ko đổi đc x gam chất rắn C,tính a,...
Đọc tiếp
Xđ % khối lượng các chất có trong hh đầu ở các trường hợp sau:
a. Cho H2SO4 loãng dư vào hh kẽm và magie cacbonat .Sau phản ứng thu 4,48 lít khí và cô cạn dd thu 28.1gam muối khan
b.hh gồm Al2O3 , Na tan hết vào dd H2SO4 loãng vừa đủ tạo 7,26 g muối và giải phóng 336ml khí
c.hh gồm Fe,Fe2O3 tan hết vào 92,2ml dd H2SO4 đặt,to, đủ thu đc dd chứa 100g muối .Khi cho dd thu đc tác dụng với dd Ba(OH)2 đủ cô cạn dd sau phản ứng đc a gam chất rắn B.Nung B đến khối lượng ko đổi đc x gam chất rắn C,tính a,x?
a, Gọi \(\left\{{}\begin{matrix}n_{Zn}=a\left(mol\right)\\n_{MgCO_3}=b\left(mol\right)\end{matrix}\right.\)
\(n_{hhkhí\left(H_2,CO_2\right)}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH:
Zn + H2SO4 ---> ZnSO4 + H2
a a a
MgCO3 + H2SO4 ---> MgSO4 + CO2 + H2O
b b b
Hệ pt \(\left\{{}\begin{matrix}a+b=0,2\\161a+84b=28,1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,1\left(mol\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}m_{Zn}=0,1.65=6,5\left(g\right)\\m_{MgCO_3}=0,1.84-8,4\left(g\right)\end{matrix}\right.\\ \rightarrow\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{6,5}{6,5+8,4}=43,62\%\\\%m_{MgCO_3}=100\%-43,62\%=56,38\%\end{matrix}\right.\)
b, \(n_{H_2}=\dfrac{0,336}{22,4}=0,015\left(mol\right)\)
PTHH:
2Na + H2SO4 ---> Na2SO4 + H2
0,03 0,015 0,015
\(\rightarrow m_{Al_2\left(SO_4\right)_3}=7,26-0,015.142=5,13\left(g\right)\\ \rightarrow n_{Al_2\left(SO_4\right)_3}=\dfrac{5,13}{342}=0,015\left(mol\right)\)
Al2O3 + 3H2SO4 ---> Al2(SO4)3 + 3H2O
0,015 0,015
\(\rightarrow\left\{{}\begin{matrix}m_{Na}=0,03.23=0,69\left(g\right)\\m_{Al_2O_3}=0,015.102=1,53\left(g\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}\%m_{Na}=\dfrac{0,69}{0,69+1,53}=31,08\%\\\%m_{Al_2O_3}=100\%-31,08\%=68,92\%\end{matrix}\right.\)
c, Thiếu \(d_{H_2SO_4}\)
Đúng 1
Bình luận (0)
Cho 19,5 g kẽm + dd H2SO4 loãng có chứa 39,2g H2SO4
a) Tính V H2 (đktc) thu được
b) Dẫn toàn bộ lượng khí thu được ở trên qua hh A gồm CuO và Fe3O4. nung nóng hh A giảm m(g). Xác định m
nZn=\(\dfrac{19.5}{65}\)=0.3(mol)
nH2SO4=\(\dfrac{39.2}{98}\)=0.4(mol)
PTHH:
Zn + H2SO4 --> ZnSO4 + H2
B/đ`:0.3 0.4 0 0
P/ứ: 0.3-->0.3--->0.3-->0.3
SauP/ứ:0 0.1 0.3 0.3
=> PTHH => khí thu đc sau p/ứ là : H2
=> VH2(đktc)=0.3*22.4=6.72(l)
Đặt nCuO=a (mol) ; nFe3O4= b (mol)
PTHH:
CuO + H2 --> Cu + H2O (1)
P/ứ: a --------->a (mol)
Fe3O4 + 4H2 --> 3Fe + 4H2O (2)
P/ứ: b ------------> b (mol)
Vì sau khi nung hỗn hợp thì H2O thoát ra và chất còn lại là Fe và Cu
=> m hh A giảm = m H2O
Từ PTHH: (1);(2)
=> nH2O=nH2= 0.3(mol)
=> mH2O=0.3*18=5.4(g)
=> m = 5.4 (g)
Đúng 0
Bình luận (0)
cho 3,2 g hh fe fes s td với h2so4 đn thu đc dd X và so2 sản phẩm khí duy nhất . cô cạn dd thu đc bao nhiêu g muối khan
Hh X gồm Fe,Cu,Ag.Chia 110,4g X thành 3 phần bằng nhau.Cho phần 1 tác dụng với Cl2 dư,thu đc m gam chất rắn.Phần 2 cho tác dụng với dd H2SO4 loãng dư thu được 2,24 lít khí H2 đktc.Hòa tan phần 3 trong 120g dd H2SO4 98% đun nóng thu được dd Y và 8,96 lít khí SO2 đktc a)Tính m b)Tính C% các chất trong dd Y